Současný stav diagnostiky a léčby ischemické choroby dolních končetin
The current situation in the diagnosis and treatment of lower‑limb ischemia
Peripheral arterial obstructive disease (PAOD) refers to the class of cardiovascular diseases that are the main ca use of mortality in developed countri es. As atherosclerosis is the ca use in almost 98 %, PAOD is considered to be the marker of the general cardiovascular risk. The pitfall of this disease lies in the fact that it remains unrecognized in the majority of our patients and that is why it remains without appropriate treatment for a long time. The goal of our therapeutic approach is to reduce general cardiovascular risk and improve the quality of life of our pati ents. The underestimated part of our treatment is regular exercise training, which is as effective as modern revascularisation techniques in the intermediate stages of the disease. Patients with severe forms of ischemi a should be treated urgently, preferably in speci alized vascular centres, which are equipped to use all modern revascularisation methods.
Key words:
peripheral arteri al obstructive disease – atherosclerosis – early di agnosis – exercise training – pharmacotherapy – therapeutic vasculogenesis – revascularisation – vascular centres
Autoři:
E. Maděrová
Vyšlo v časopise:
Kardiol Rev Int Med 2008, 10(4): 177-182
Souhrn
Ischemická choroba dolních končetin (ICHDK) patří mezi kardiovaskulární onemocnění, která jso u hlavní příčino u mortality ve vyspělých zemích. Příčino u je až v 98 % obliterující ateroskleróza (AS). ICHDK lze považovat za marker celkového kardi ovaskulárního rizika. Zrádnost onemocnění spočívá v tom, že u velké části paci entů zůstává nerozpoznáno a tedy dlo uho bez odpovídající léčby. V léčbě máme za cíl zejména snížení celkového kardi ovaskulárního rizika a zlepšení kvality života nemocných. Podceňovano u složko u léčby je pravidelná pohybová aktivita, která se u středně pokročilých stadi í vyrovná moderním revaskularizačním postupům. Péče o nemocné s těžší formo u ischemi e by měla být řešena urychleně, a to přednostně ve speci alizovaných angi ocentrech, která nabízejí všechny moderní revaskularizační metody.
Klíčová slova:
ischemická choroba dolních končetin – ateroskleróza – včasná di agnostika – pohybová aktivita – farmakoterapi e – terape utická vaskulogeneze – revaskularizace – angiocentra
Úvod
Příčino u ICHDK je ve většině případů (až 98 %) aterosklerotické postižení [1]. Bohužel stále velká část paci entů zůstává nerozpoznána (je asymptomatická, oligosymptomatická či nevyhledá lékařsko u pomoc) a nedostane se jim včasné léčby. Dle TASC (TransAtlantic Inter - Soci ety Consensus, z r. 2000) dokonce převažují asymptomatičtí paci enti (na více než 300 asymptomatických je 100 kla udikujících a 100 kla udikujících, kteří však nevyhledají lékaře). ICHDK je indikátorem systémové aterosklerózy. Podle některých a utorů více než 50 % paci entů s ICHDK trpí so učasně ischemicko u chorobo u srdeční (ICHS), 10 – 15 % (někde až 40 %) má postižení mozkových tepen. Pětiletá mortalita bývá udávána okolo 28 % (20 – 50 %), její příčino u je nejčastěji (v 50 %) ICHS, asi v 15 % cévní mozková příhoda (CMP). Proto je třeba po těchto postiženích u paci entů s ICHDK aktivně pátrat. Prognózu výrazně zhoršuje přítomnost di abetes mellitus (DM) – u cca 12 – 17 % nemocných –, zejména pro přidruženo u mikro angi opatii a ne uropatii (časté asymptomatické formy ICHDK) [2].
Rozlišujeme stadi um asymptomatické, kla udikační a stadi um kritické končetinové ischemi e: tato může být z časového hlediska rozdělena na akutní (doba trvání akutních příznaků do 1 – 2 týdnů), subakutní a chronicko u formu (příznaky trvající déle než 3 měsíce) (obr. 1).
![Přirozený vývoj ICHDK [24,13].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/95709bbb961dff87362a358518f1e6c9.jpg)
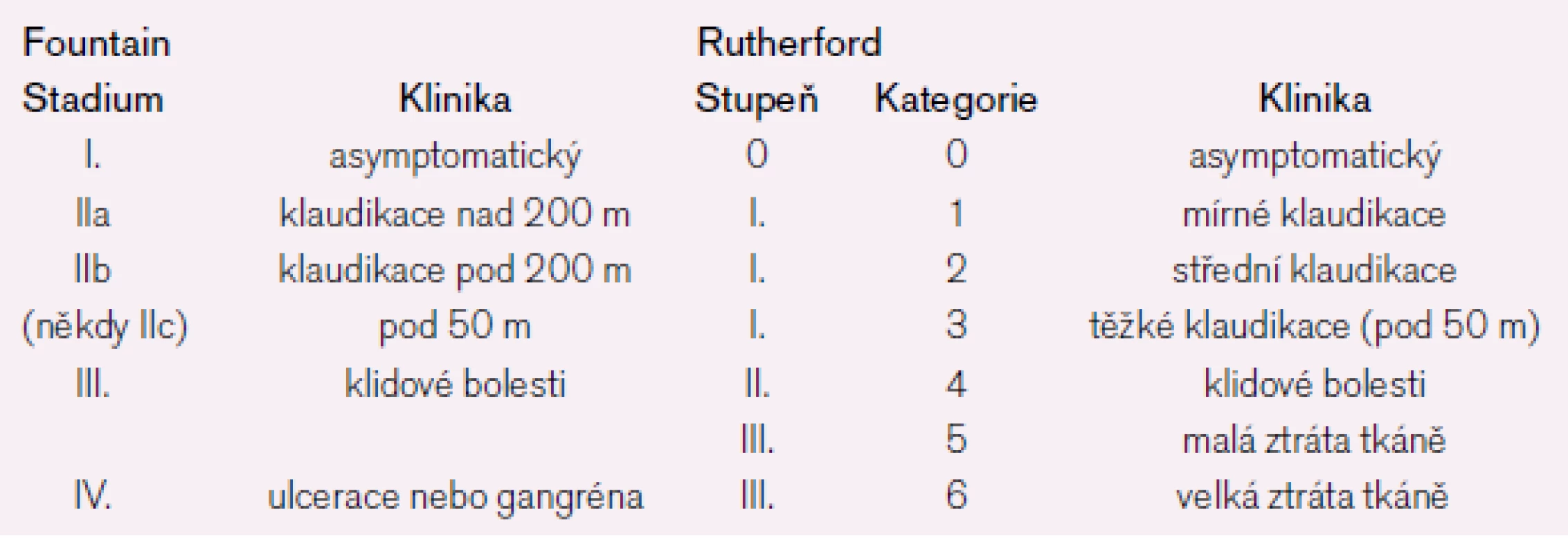
V klasifikaci ICHDK se doposud nejčastěji po užívá funkční klasifikace dle Fontaina z roku 1954 [3], která rozděluje nemocné do čtyř stadi í. V anglosaských zemích bývá nověji po užívána klasifikace dle Rutherforda [4] (viz tab. 1).
Di agnostika ICHDK
Základem di agnostiky i v dnešní době zůstává správně odebraná anamnéza. Věnujeme pozornost přítomnosti rizikových faktorů (pět základních – ko uření (třikrát vyšší riziko než u nekuřáků), di abetes mellitus (zde je pětkrát vyšší riziko kritické ischemi e oproti nedi abetikům), věk (incidence méně než 3 % u osob pod 60 let, až 20 % u osob nad 70 let), hypertenze a dyslipidemi e). Onemocnění častěji postihuje muže (u těžších forem až třikrát častěji). Hyperhomocysteinemi e zvyšuje riziko aterosklerózy 2 – 3krát a mechanizmus jejího účinku není jasný. Dále bývá popisována mírná elevace C‑re aktivního proteinu (CRP), zejména u pokročilých stadi í choroby [5].
Správně interpretujeme symptomy onemocnění – intermitentní kla udikace, klidové ischemické bolesti, vývoj funkčního omezení, trofických změn a prodělané chirurgické či intervenční terapi e. Podle lokalizace kla udikací uso udíme, které úseky tepenného systému jso u postiženy (bolesti v plantě – postižení tepen bérce a nohy, v lýtku – postižení femoropolite álního segmentu, bolest v hýždích obvykle spojená se slabostí a únavností i distálnějších svalových skupin – postižení aorto ilického úseku). Musíme odlišit pse udokla udikace. Klidové ischemické bolesti jso u téměř vždy lokalizovány v oblasti nohy a přicházejí či se zhoršují v noci, vleže. Při svěšení končetiny či po postavení se jejich intenzita zmenšuje či dokonce vymizí.
Fyzikální vyšetření (viz tab. 2) pomáhá zpřesnit klinické podezření, chybo u bývá, že se neprovádí dostatečně často. Fyzikální vyšetření srdce a plic provádí 95 % lékařů, palpaci pulzu na a. dorsalis pedis jen 60 % lékařů [6].
Třetím jednoduchým vyšetřením, které může ve své ambulanci provádět každý lékař, je polohový test dle Ratschowa – jednoduchý test, který se může uplatnit jak při di agnostice, tak při sledování progrese onemocnění. Test spočívá v provádění plantární a dorzální flexe vleže po vteřinových intervalech, a to maximálně po dvě minuty, hodnotí se doba cvičení, příčina ukončení a lokalizace bolestí a poté po svěšení končetin rychlost zčervenání (normálně do 5 s, difuzně na celé noze do 15 s) a čas žilní náplně (do 10 s).
Přesto si v moderní di agnostice nevystačíme bez přístrojové techniky. Uplatňují se jak neinvazivní, tak invazivní techniky. Zásado u je neprovádět di agnostické invazivní vyšetření, pokud lze stejno u informaci obdržet neinvazivně.
Ke známým a velmi cenným vyšetřením patří měření kotníkových tlaků (s výpočtem indexu ABI – Ankle - Brachi al Index, resp. index kotník - paže). Provádíme jej pomocí dopplerovského měřiče, vyšetření je jednoduché, rychlé a přitom velmi citlivé – senzitivita tohoto vyšetření je 95 – 97 %, specificita 100 % a výsledky dobře korelují s angi ografickými nálezy [5]. Užívá se jak v epidemi ologických studi ích, tak při rutinním cévním vyšetření, slo uží jako screeningová metoda i jako metoda k monitoraci progrese choroby a efektu léčby. Přesto toto jednoduché vyšetření bývá málo po užíváno. Do budo ucna lze počítat s tím, že ABI by měl být měřen všem paci entům nad 50 let s přítomností rizikových faktorů ICHDK a všem paci entům nad 70 let s přítomností ICHS či cévního onemocnění mozku (COM) [7].
Stanovení ABI je jednoduché [16], pozor bychom si však měli dávat na chyby při měření a interpretaci výsledků. Nejčastěji bývá po užívána nesprávná šíře manžety či tlak bývá měřen příliš rychle. Vyšetření nemůžeme po užít při patologicky změněných rigidních tepnách (Moenckebergova kalcinóza, chronická di alýza).
Normální hodnota ABI je 1 – 1,29 (za hraniční se považuje 0,9 – 0,99), jednoznačně patologická hodnota ABI – svědčící pro ICHDK – je pod 0,9. Hodnota pod 0,5 svědčí pro významné postižení končetinových tepen a je spjata se závažno u prognózo u nemocného (až 15násobné riziko mortality) [7].
Někdy u paci entů s typickými kla udikacemi zjistíme normální ABI. Potom se doporučuje objektivizovat potíže zátěžovým testem – například na běžeckém trenažeru – vyšetřením kla udikační vzdálenosti. Vyšetření slo uží hlavně k poso uzení funkčního stavu a efektu léčby [8].
Elegantní a dnes již rutinní neinvazivní di agnostiko u je barevná duplexní sonografi e – umožňuje zobrazit anatomické struktury (cévy, jejich okolí), jejich velikost, přítomnost a uložení aterosklerotických plátů, přítomnost kalcifikací ve stěně tepen, barevné mapování a pulzní dopplerovské vyšetření umožňují mapovat krevní tok tepno u, jeho směr, kvalitu (laminární, turbulentní) a rychlost. Nevýhodo u je, že podrobné vyšetření tepen dolních končetin (na rozdíl od vyšetření např. magistrálních mozkových tepen) je časově náročné. Také bývá limitováno tortuózním průběhem tepen, kalcifikacemi, obezito u, edémem okolní tkáně, zpomalením krevního pro udění za a před proximálními uzávěry a obvykle je nutné potvrzení nálezu invazivním vyšetřením.
Základní standardní metodo u k zobrazení tepen DK nadále zůstává digitální subtrakční angi ografie (DSA). Je relativně bezpečná, přesto vzhledem ke své invazivitě by měla být vyhrazena pro případy plánované intervenční léčby nebo chirurgického řešení. Je vhodné zvolit přístup tak, aby bylo možno případně provést endovaskulární léčbu v jedné době s di agnosticko u angi ografi í. V so učasnosti není stanoven jednoznačný kla udikační interval, který by byl kritéri em endovaskulární léčby. Při indikaci angi ografi e u kla udikujících paci entů se řídíme jejich subjektivním pocitem významné limitace a snížení kvality života. So učasně posuzujeme celkový zdravotní stav nemocného.
Poslední dobo u se stále více v di agnostice uplatňuje angi ografi e pomocí magnetické rezonance (magneticko‑rezonanční angi ografi e – MRA), což je neinvazivní vyšetření s možností ambulantního provádění, kde není využíváno i onizujícího záření, umožňuje poso uzení nejen lumina tepny, ale i stěny a přilehlých struktur. V zahraničí pomalu vytlačuje di agnostické DSA, u nás širší využití zatím limituje špatná dostupnost a vyšší cena vyšetření. MRA má navíc tendenci k nadhodnocování významnosti stenóz, hlavně u tepen malého kalibru (bércové, pedální) jso u výsledky méně přesné ve srovnání s angi ografi í. Respektovat musíme klasické kontraindikace MRI (nemožnost užití u paci entů s kovovými pomůckami v tělě). Při po užití kontrastní látky (CE MRA) se senzitivita metody pohybuje mezi 71 až 100 % [9], specificita se udává 75 – 100 %.
Alternativně lze po užít CT angi ografii (CTA) již bez výhody absence i onizujícího záření, ale s možností provedení 3D rekonstrukce. Nevýhodo u je zhoršená možnost hodnocení za přítomnosti kalcifikací ve stěně nebo kovového materi álu (stenty, spirály), taktéž zobrazení bércových tepen má zatím ve srovnání s digitální angi ografi í nižší kvalitu. U tepen většího kalibru se senzitivita i specificita metody udává přes 96 % [10].
K hodnocení mikrocirkulace lze využít fotoplethysmografii a také laser doppler (sledování perfuzních změn po různých provokacích – chlad, okluze, léky, polohové změny apod.).
Plethysmografi e (vodní, vzduchová, strain ga uche, impedanční – techniky založené na měření změny objemu či impedance končetiny) dnes již patří mezi méně po užívaná vyšetření v di agnostice ICHDK.
Léčba ischemické choroby dolních končetin
Základní léčebné cíle jso u dva: snížení kardi ovaskulárního rizika (sekundární prevence aterosklerózy, prevence ztráty končetiny a prognosticky závažných kardi ovaskulárních příhod) spolu se zlepšením kvality života (ovlivnění potíží nemocného) [7].
Snížení kardi ovaskulárního rizika
Moderní léčba by měla zahrnovat jak režimová opatření – zanechání kuřáckých návyků, ne aterogenní di etu, udržování správné tělesné hmotnosti a pravidelno u pohybovo u aktivitu – tak farmakologicko u intervenci (především správná léčba hypertenze a dyslipidemi e, kontrola di abetu a dále protidestičková léčba).
V případě nikotinizmu u paci enta bychom neměli zůstávat jen u jednorázového doporučení, ale paci enta opakovně intervenovat a odesílat do speci alizovaných center. Často je nutná farmakologická podpora (nikotinové náhražky, event. psychofarmaka – bupropi on, vareniklin). Při léčbě hypertenze by cílový TK měl činit 130/ 80 a nižší, preferovaným antihypertenzivem jso u ACE‑inhibitory (ramipril ve studii HOPE snížil riziko vážné cévní příhody u těchto paci entů o 25 %). Neplatí již kontraindikace podávání beta‑blokátorů [11]. Rovněž bychom měli intervenovat dyslipidemii s důrazem na ovlivnění hladiny LDL‑cholesterolu k cílovým hodnotám pod 2,5 mmol/ l. Zásadním lékem v této léčbě jso u statiny. Jso u však indikovány nejen u paci entů s dyslipidemi í, ale u všech paci entů s ICHDK bez ohledu na inici ální výši cholesterolu. Kromě ovlivnění progrese aterosklerózy (zejména snížením LDL‑cholesterolu) statiny snižují riziko vzniku či zhoršení kla udikací (simvastatin) a jejich dlo uhodobé podávání (atorvastatin, 80 mg denně, 12 měsíců) prokázalo prodlo užení kla udikační vzdálenosti o 63 % oproti placebu, kde prodlo užení činilo 38 %. Předpokládaným mechanizmem účinku je pozitivní ovlivnění funkce endotelu [12].
V léčbě di abetu mellitu by měl být důraz kladený na těsno u kompenzaci (glykovaný hemoglobin pod 5 %), prevenci komplikací a dobro u podi atricko u péči (správná obuv, péče o kůži, ošetřování poranění). Obézní paci enti by měli redukovat svo u hmotnost.
Další nutno u terapi í u paci entů s ICHDK je protidestičková léčba. Snižuje riziko infarktu myokardu (IM), CMP a úmrtí z cévních příčin (snížení fatálních i nefatálních kardi ovaskulárních příhod o 25 %), je indikována u všech nemocných s ICHDK (s respektováním kontraindikací). Dle evidence‑based medicine má úroveň doporučení IA. Doporučována je kyselina acetylsalicylová (ASA) (v malé dávce 75 – 325 mg denně, u nás 100 mg / den). V amerických doporučeních se objevuje i clopidogrel (úroveň doporučení IB), u nás zatím není v této indikaci schválen pojišťovno u a je rezervován pro případy intolerance ASA. Perorální antiko agulační léčba není rutinně doporučována pro paci enty s ICHDK (IIIC) [13].
Neexistuje jednoznačné doporučení pro podávání látek snižujících hladinu homocysteinu (kyselina listová a vitamin B12) [13].
Zlepšení kvality života (ovlivnění potíží nemocného)
Největší efekt ve stadi u kla udikací má pohybová léčba (trénink chůzí, zátěžová terapi e). Vliv pravidelné aerobní zátěže na zlepšování kla udikačního intervalu je vysvětlován intermitentním zvyšováním tlakového gradi entu v postiženém úseku tepny, posílením vazodilatační funkce endotelu, redistribucí krevního toku, změno u metabolizmu kosterního svalu, snížením krevní viskozity a zvýšením extrakce kyslíku. Potencuje se novotvorba kolaterál. Dochází také k poklesu celkového a LDL ‑cholesterolu a systolického krevního tlaku, a tím se zmírňuje progrese aterosklerotických změn. Kla udikační interval se může po šesti měsících pohybové léčby prodlo užit až přibližně třikrát (podobně jako po chirurgické léčbě) [14].
Existuje celá řada doporučení a režimů stran pravidelného tréninku. Obecně doporučujeme paci entům chodit co nejvíce až do nástupu bolesti, minimálně třikrát týdně po dobu 30 minut po 3 – 6 měsíců. Nejefektivnější bývá cvičení pod dozorem (v zahraničí bývá doporučována chůze na „běhátku“ – tre admill, v našich podmínkách zatím takováto rehabilitace nebývá prováděna).
Jednodušším zátěžovým programem je intervalový svalový trénink. Paci ent ho provádí sám – opakovaně krátce zatěžuje různé svalové skupiny dle lokalizace tepenného uzávěru (při pánevním postižení trénuje dřepy, při femoropoplite álním postižení výstupy na špičky), cvičí po jedné vteřině až do vzniku bolesti [15].
V případě farmakologického ovlivnění kla udikací bývala historicky podávána řada léků působících jako vazodilatanci a (alkohol, rezerpin, tolazolin, nitráty, isoproterenol, nifedipin, flunarizin, cinarizin, isoxsuprin a další), jejich pozitivní účinek však nikdy prokázán nebyl, spíše se projevoval efekt negativní – odčerpání krevního toku od ischemických oblastí (ste al fenomén). I léky po užívané v so učasné době mají po uze malý efekt na prodlo užení kla udikačního intervalu (což ne odpovídá jejich rozsáhlé preskripci) a měly by být doporučovány po uze u nemocných s krátkými kla udikacemi, u kterých není možná či vhodná chirurgická nebo intervenční léčba [15,16].
Nejvíce důkazů pozitivního účinku bylo podáno pro inhibitor fosfodi esterázy 3 – cilostazol. Vykazuje aktivitu protidestičkovo u, antitromboticko u, vazodilatační, dále zvýšení krevního průtoku, HDL ‑cholesterolu, pokles triglyceridů a inhibici buněk hladkého svalu cévní stěny. Průměrně bylo po jeho podání prokázáno prodlo užení kla udikační vzdálenosti na tre admillu o 50 – 70 m za 24 týdnů. V porovnávací studii s pentoxifylinem prokázal větší účinnost cilostazol. Bohužel v České republice zatím lék není registrovaný. Naftidrofuryl je antagonista 5 - hydroxytryptamin‑2 receptoru s vazodilatačním efektem. Oproti placebu bylo po jeho podávání prokázáno průměrné prodlo užení maximální kla udikační vzdálenosti o 71 m (u pentoxifylinu o 44 m). Časté však bývá jeho poddávkování (doporučovaná dávka je 600 mg denně, tj. třikrát 2 tbl.) [16]. Pentoxifylin je zařazován mezi hemore ologika pro svo u schopnost zlepšovat deformabilitu červených i bílých krvinek a zlepšovat tak možnost průniku skrze kapiláry. Po jeho podání byl zjištěn i pokles hladiny fibrinogenu a agregační aktivity trombocytů. Má silný vazodilatační účinek. Některé studi e prokázaly, že po jeho podání došlo k prodlo užení maximální kla udikační vzdálenosti o 44 – 48 m, jindy se konstatuje, že jeho efekt je po uze marginální nebo žádný. Proto byl zařazen mezi léky s nedostatečným průkazem efektivity u nemocných s intermitentní kla udikací [14].
Na symptomu intermitentní kla udikace se částečně také podílí změněný svalový metabolizmus. Posílení oxidativního metabolizmu může zlepšit funkci kosterního svalu i bez zvýšení krevního průtoku. L - karnitin a propi onyl - L - karnitin slo uží jako zdroj karnitinu pro Krebsův cyklus, moho u zlepšit oxidaci glukózy. Perorální podávání propi onyl - L - karnitinu v dávce dvakrát denně 1 g dle některých a utorů zlepšilo kla udikační vzdálenost na tre admillu o 54 – 73 % [16], ovšem důkazy o prospěšnosti jeho podávání zůstávají nejednoznačné (doporučení IIb dle ACC/ AHA guidelines) [13].
Existuje celá řada dalších preparátů a technik, u kterých potřebný účinek na prodlo užení kla udikační vzdálenosti nebyl spolehlivě prokázán nebo studi e s nimi probíhají. Naděje jso u vkládány do léčby pomocí angi ogenních růstových faktorů a kmenových buněk podporujících tvorbu kolaterál. První z metod je založena na novotvorbě cév prostřednictvím stimulace růstovými faktory, druhá spočívá v aplikaci vlastních kmenových buněk (schopných další diferenci ace, odebraných z vlastní kostní dřeně) do ischemické oblasti s předpokladem diferenci ace v nové cévy [17,18]. I když existuje celá řada menších pilotních studi í s nadějnými výsledky v zahraničí i v České republice [19], doposud žádná z dvojitě slepých, placebem kontrolovaných klinických studi í neprokázala přesvědčivý klinický přínos těchto metod [20]. Zatím nejso u so učástí rutinně doporučovaných postupů a zůstávají předmětem dalšího výzkumu.
Intervenční léčba
Konzervativní léčba zpravidla nepřináší potřebný efekt tam, kde je končetina ohrožena (chronická kritická ischemi e, závažná akutní ischemi e). Zde je třeba vždy zvážit možnost endovaskulární či chirurgické intervence. Endovaskulární léčba má výsledky srovnatelné s chirurgickými postupy a výrazně nižší riziko. Může poso uvat okamžik, kdy bude třeba léčby angi ochirurgické, a provádíme ji i u nemocných s kla udikačním intervalem delším nežli 200 m.
Nejčastěji bývá prováděna perkutánní transluminální angi oplastika (PTA) a implantace intravaskulárních stentů (stent - graftů). Vzácně (asi v 1 % případů) jso u využívány i jiné techniky, např. perkutánní aterektomi e, pulzní farmakomechanická trombolýza, laserová rekanalizace. Vari antami balónkové dilatace jso u subintimální PTA, „cutting ballo on“ a kryoplastika. K nejčastěji prováděným chirurgickým rekonstrukcím patří aortobifemorální bypass, aortobiili akální bypass, ile ofemorální bypass, femoropoplite ální bypass a profundoplastika. K chirurgické léčbě patří i embolektomi e Fogartyho katetrem v léčbě akutní končetinové ischemi e a – stále méně prováděná – lumbální sympatektomi e.
Některé typy tepenných lézí je z hlediska dlo uhodobé účinnosti vhodnější léčit chirurgicky, jiné endovaskulárně a u dalších lze využít způsoby oba. Nejvhodnější typ léčby by vždy měl poso udit erudovaný cévní tým v angi ocentru, kromě lokalizace a typu léze je také potřeba zhodnotit riziko výkonu s ohledem na celkový stav paci enta a jeho kvalitu života (obr. 2).
![Vodítko pro rozhodování o postupu u nemocných s ICHDK [16].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/eacc7625862dd748e4daa837af80f451.jpg)
Léčba kritické končetinové ischemi e by jednoznačně měla být směřovaná do angi ocentra, kde lze provést urychleně angi ografii a následně revaskularizační výkon. Pokud technicky revaskularizaci nelze provést, pak k zabránění amputace bývá tradičně po užívána parenterální vazodilatační léčba. Nadějnými léky v této indikaci jso u prostano idy (prostaglandin E1 (PGE1) a prostacyklin s jeho analogy – iloprost, beraprost), které mají účinek vazodilatační a endoteli álně protektivní, potlačují aktivaci trombocytů a le ukocytů, zlepšují erytrocytární deformabilitu a zvyšují fibrinolyticko u aktivitu. V so učasné době však neexistuje dostatečně velká studi e, která by prokázala snížení počtu amputací a zlepšené přežívání bez amputace (některé menší studi e s PGE1 prokázaly zmenšení vředů a snížení intenzity klidových bolestí, event. prodlo užení kla udikačního intervalu, jindy byl prokazován pozitivní efekt v hospitalizační době, avšak po šesti měsících již nebyl patrný rozdíl oproti skupině s placebem v mortalitě a počtu amputací) [16,21]. Dlo uhodobá a opakovaná léčba prostano idy je opodstatněná jen tehdy, když lze pozorovat příznivý efekt (ústup klidových bolestí, tvorba granulační tkáně v oblasti tkáňových defektů, prodlo užení kla udikační vzdálenosti apod.).
U řady nemocných dochází k většímu zlepšení prokrvení prostým svěšením končetiny. Vhodné je omezení fyzické zátěže a chůze (nízké distální tlaky mají tendenci při chůzi poklesno ut). Důležito u so učástí léčby kritické končetinové ischemi e je i lokální léčba. K čištění defektu je možno využít enzymatických lokálních přípravků či aplikaci hyperosmolárních roztoků. Granulační tkáň nemá zaschno ut (vhodné překrytí mastí). Existuje celá řada výrobků, které se zaměřují na lokální léčbu různých stadi í defektů. V poslední době vešla ve známost metoda mechanického očištění rány, po užívaná zejména u infikovaných ischemických defektů – léčba „červy“. Jedná se o larvy mo uchy Lucili a sericata, které jso u umístěny do defektu na tři až čtyři dny a mají schopnost pozřít nekroticko u a infikovano u tkáň, zatímco zdravá tkáň zůstane uchráněna. Poté jso u larvy odstraněny. Jedná se o léčbu velice elegantní, na druho u stranu lze stejných výsledků dosáhno ut i jinými metodami, které jso u dostupnější i levnější [22]. Pokud je přítomný edém v oblasti defektu (zhoršuje hojení), pak je oprávnění po užití bi oflavono idů. Někdy je nutné držet končetinu v horizontální poloze. Bolest ovlivňujeme intenzivní analgeticko u léčbo u, někdy je nutné až provedení peridurální blokády. Infekci v defektu sanujeme systémově podávanými antibi otiky. Příznivě může působit hyperbarická oxygenoterapi e nebo míšní stimulace. Existují i metody, pro které nebyl pozitivní léčebný účinek spolehlivě a dostatečně prokázán (hemodiluční terapi e, tlaková kompresivní a imunomodulační terapi e).
Závěr
Onemocnění periferních tepen je důležitým markerem generalizované aterosklerózy. Poznání choroby v časných stadi ích, ale také asymptomatických forem, je důležité pro další osud paci enta. Tato včasná léčba je zaměřena na důsledné ovlivnění rizikových faktorů a zpomalení progrese choroby. Je diskutováno doporučení, aby se v populaci nad 50 let rutinně vyšetřoval tlakový index kotník - paže a byla poso uzena přítomnost asymptomatické ICHDK. ICHDK je spojena se zvýšeným rizikem postižení jiných oblastí, které dominantně určují mortalitu a závažno u morbiditu (koronární a cerebrovaskulární oblast, břišní aorta, renální tepny). Po těchto onemocněních je u našich paci entů potřeba aktivně pátrat a léčit je.
Zvýšená pozornost by měla být věnována nemocným s nejtěžšími formami ischemi e – akutními tepennými uzávěry a chronicko u kriticko u ischemií. Trendem je budování angi ologických týmů v angi ocentrech, kde je možnost kvalitní a rychlé di agnostiky s následno u adekvátní intervenční a angi ochirurgicko u léčbo u. Ve světě se budují také tzv. vaskulární centra, kde je poskytována komplexní péče o cévní paci enty (kromě angi ologa a angi ochirurga také kardi olog, ne urolog, di abetolog, hematolog, revmatolog a další). Taková centra se stávají také centry výzkumu a vzdělávání. Pro zlepšení péče o nemocné s ICHDK je kromě budování těchto center třeba také zlepšit erudici u lékařů prvního kontaktu a spolupráci mezi těmito lékaři a vaskulárním centrem [23].
Doručeno do redakce 21. 7. 2008
Přijato k otištění po recenzi 21. 11. 2008
MUDr. Eva Maděrová,
Interní kardiologická klinika, FN Brno
edufkova@yahoo.com
Zdroje
1. Karetová D, Staněk F. Angi ologi e pro praxi. Maxdorf 2001.
2. Criqui MH, Fronek A, Barrett - Connor E et al. The prevalence of peripheral arteri al dise ase in a defined populati on. Circulati on 1985; 71 : 510 – 515.
3. Fontaine R, Kirn M, Ki eny R. Di e chirurgische Behandlung der peripheren Durchblutungsstörungen. Helv Chir Acta 1954; 5/ 6 : 499 – 533.
4. Rutherford RB. Standards for evalu ating results of interventi onal therapy for peripheral vascular dise ase. Circulati on 1991; 83: I6 – I11.
5. Fowkes FG, Ho usley E, Ri emersma RA et al. Smoking, lipids, glucose intolerance, and blo od pressure as risk factors for peripheral atherosclerosis compared with ischemic he art dise ase in the Edinburgh Artery Study. Am J Epidemi ol 1992; 135 : 331 – 340.
6. Mohler ER 3rd. Peripheral arteri al dise ase: identificati on and implicati ons. Arch Intern Med 2003; 163 : 2306 – 2314.
7. Karetová D, Ingrischová M, Vojtíšková J. Ischemická choroba dolních končetin – marker celkového kardi ovaskulárního rizika. Practicus 2008; 7 : 9 – 13.
8. Musil D. Ischemická choroba dolních končetin. Interní Med 2007; 4 : 170 – 174.
9. Eiberg JP, Lundorf E, Thomsen C et al. Peripheral vascular surgery and magnetic resonance arteri ography – a revi ew. Eur J Vasc Endovasc Surg 2001; 22 : 396 – 402.
10. Fleischmann D, Hallett RL, Rubin GD. CT angi ography of peripheral arteri al dise ase. J Vasc Interv Radi ol 2006; 17 : 3 – 26.
11. Cífková R, Býma S, Češka R et al. Prevence kardi ovaskulárních onemocnění v dospělém věku. Společné doporučení českých odborných společností. Vnitr Lek 2005; 51 : 1021 – 1036.
12. Mohler ER 3rd, Hi att WR, Cre ager MA. Cholesterol reducti on with atorvastatin improves walking distance in pati ents with peripheral arteri al dise ase. Circulati on 2003; 108 : 1481 – 1486.
13. Hirsch AT, Laskal ZJ, Hertzer NR et al. ACC/ AHA 2005 guidelines for the management of pati ents with peripheral arteri al dise ase (lower extremity, renal, mesenteric, and abdominal aortic): executive summary a collaborative report from the American Associ ati on for Vascular Surgery/ Soci ety for Vascular Surgery, Soci ety for Cardi ovascular Angi ography and Interventi ons, Soci ety for Vascular Medicine and Bi ology, Soci ety of Interventi onal Radi ology, and the ACC/ AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Pati ents With Peripheral Arteri al Dise ase) endorsed by the American Associ ati on of Cardi ovascular and Pulmonary Rehabilitati on; Nati onal He art, Lung, and Blo od Institute; Soci ety for Vascular Nursing; TransAtlantic Inter - Soci ety Consensus; and Vascular Dise ase Fo undati on. J Am Coll Cardi ol 2006; 47 : 1239 – 1312.
14. Norgren L, Hi att WR, Dormandy JA et al. Inter - Soci ety Consensus for the Management of Peripheral Arteri al Dise ase (TASC II). Eur J Vasc Endovasc Surg 2007; 33: S1 – S75.
15. Roztočil K (ed). Trendy so udobé angi ologi e. Galén 2006.
16. Bulvas M. Doporučení pro di agnostiku a léčbu ischemické choroby dolních končetin. Česká angi ologická společnost 2008. [http://www.angi ologi e.cz].
17. Novotný T. So učasnost a budo ucnost buněčné terapi e. Medical Tribune 16/ 2008; A11.
18. Simons M. Angi ogenesis: where do we stand now? Circulati on 2005; 111 : 1556 – 1566.
19. Chochola M, Pytlík P, Kobylka P et al. Terape utická vaskulogeneze u paci entů s kriticko u končetinovo u ischemi í dolních končetin. Supplementum Cor Vasa 2007; 49 : 38.
20. Hirsch AT. Critical limb ischemi a and stem cell rese arch: anchoring hope with informed adverse event reporting. Circulati on 2006; 114 : 2581 – 2583.
21. Prostano ids for chronic critical leg ischemi a. A randomized, controlled open - label tri al with prostaglandin E1. The ICAI Study Gro up. Ischemi a Cronica degli Arti inferi ori. Ann Intern Med 1999; 130 : 412 – 421.
22. Kasalová Z. Syndrom di abetické nohy. [http:/ / www.zdravotnickenoviny.cz/ scripts/ detail.php?id=163121].
23. Eliška O, Spáčil J, Štvrtinová V et al. Angi ologi e 2008. Trendy so udobé angi ologi e. Galén 2008.
24. Weitz JI, Byrne J, Clagett GP et al. Di agnosis and Tre atment of Chronic Arteri al Insuffici ency of the Lower Extremiti es: A Critical Revi ew. Circulati on 1996; 94 : 3026 – 3049.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2008 Číslo 4
-
Všechny články tohoto čísla
- Nordic walking
-
Studie Hyvet a HYVET-COG
Léčba velmi starých hypertoniků - Centrální a periferní krevní tlak a jejich ovlivnění léčbou
- Studie ACCOMPLISH
- Hypertenzní choroba a tepová frekvence
- Srdeční frekvence a kardiovaskulární riziko: Co říká studie BEAUTIFUL
- Abdominal obesity – an epidemic of the 21st century
- Trombolytická terapie mozkového infarktu
- Současný stav diagnostiky a léčby ischemické choroby dolních končetin
- Klinické studie Prezentované na sjezdu Evropské kardiologické společnosti – ESC v Mnichově 2008
- Galerie autorů
- Rejstřík k ročníku 10 (2008)
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Hypertenzní choroba a tepová frekvence
- Trombolytická terapie mozkového infarktu
- Abdominal obesity – an epidemic of the 21st century
- Centrální a periferní krevní tlak a jejich ovlivnění léčbou