Není perikarditida jako perikarditida – kazuistika
Pericarditis is not always the same
The presented case study presents the diagnostic methods used in a 42‑year ‑ old patient with atypical course of exudative pericarditis. The definitive diagnosis is angiosarcoma of the heart. Angiosarcoma of the heart is a rare malignant tumor that most often affects the right atrium. The treatment of angiosarcomas is surgical. The prognosis of heart sarcomas is poor.
Keywords:
acute pericarditis – angiosarcoma – echocardiography
Autoři:
J. Havelková; Lajos Gergely
Působiště autorů:
Interní oddělení, Nemocnice Písek, a. s.
Vyšlo v časopise:
Kardiol Rev Int Med 2015, 17(1): 37-40
Kategorie:
Kardiologická revue
Souhrn
V kazuistice je popsán diagnostický proces dvaačtyřicetiletého nemocného s atypickým průběhem exudativní perikarditidy. Definitivní diagnóza je angiosarkom srdce. Angiosarkom srdce je vzácný maligní tumor postihující zpravidla pravou síň. Léčba angiosarkomů srdce je chirurgická. Prognóza všech sarkomů srdce je špatná.
Klíčová slova:
akutní perikarditida – angiosarkom srdce – echokardiografie
Vlastní popis případu
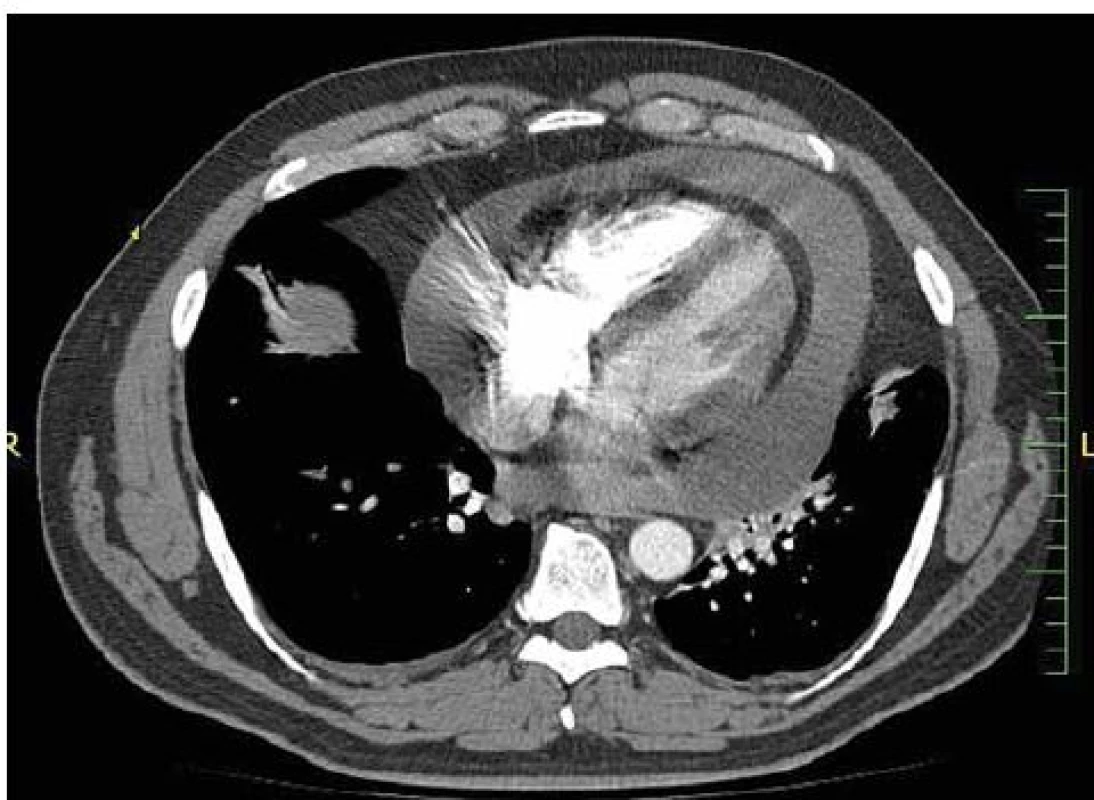
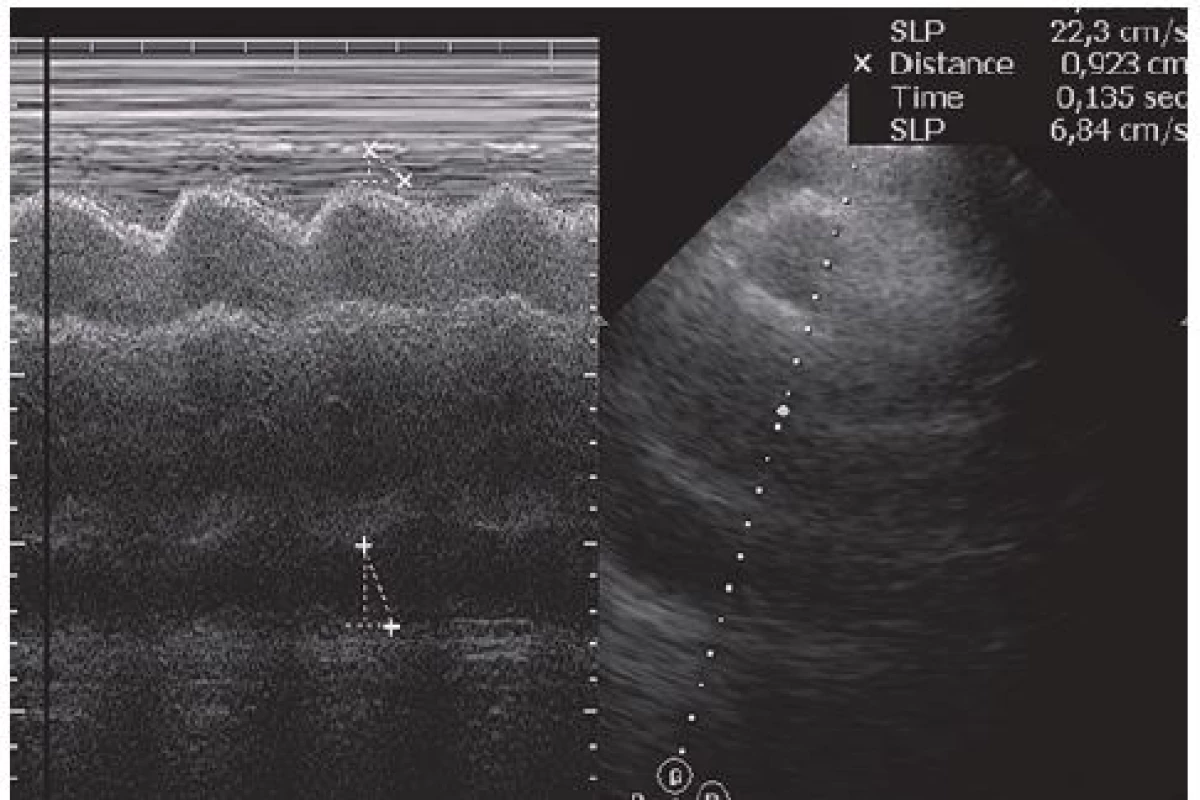
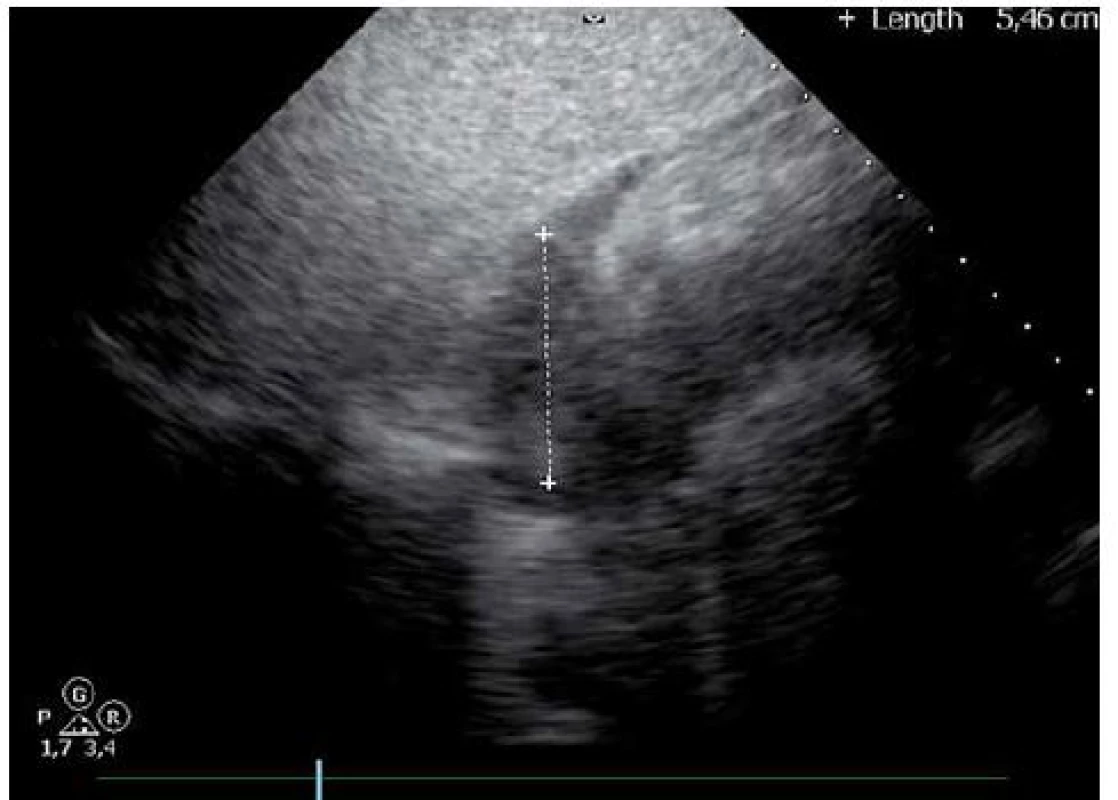
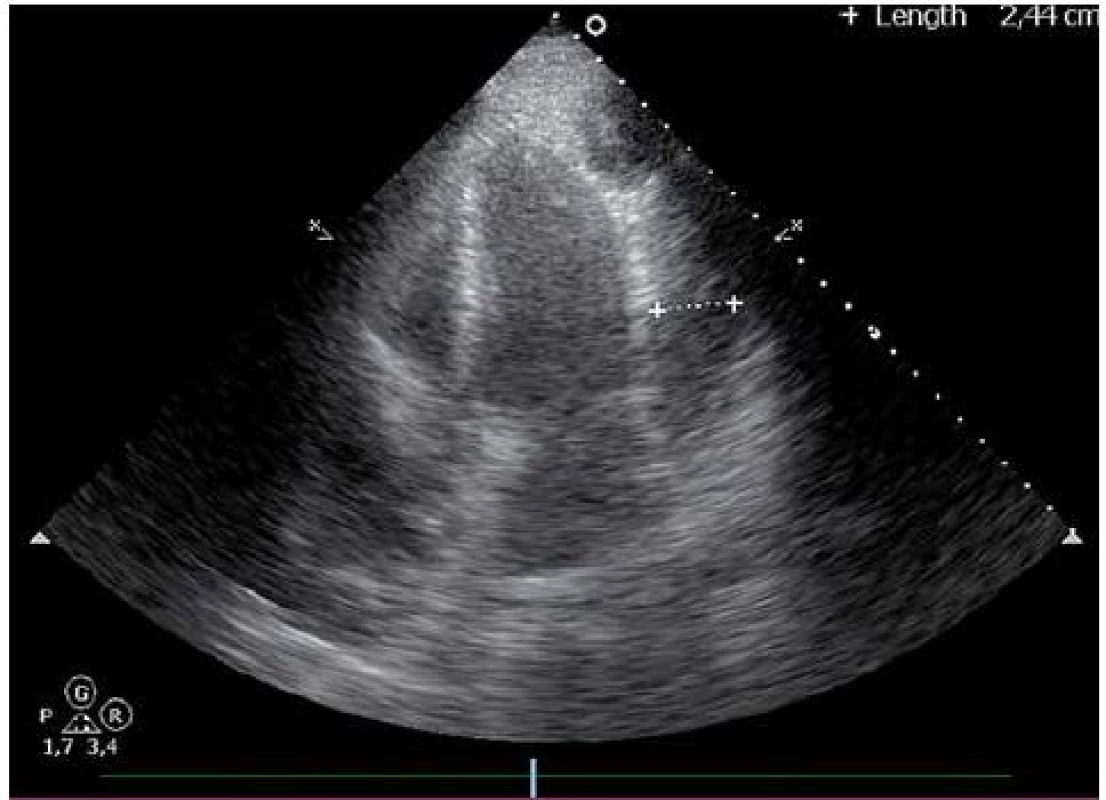
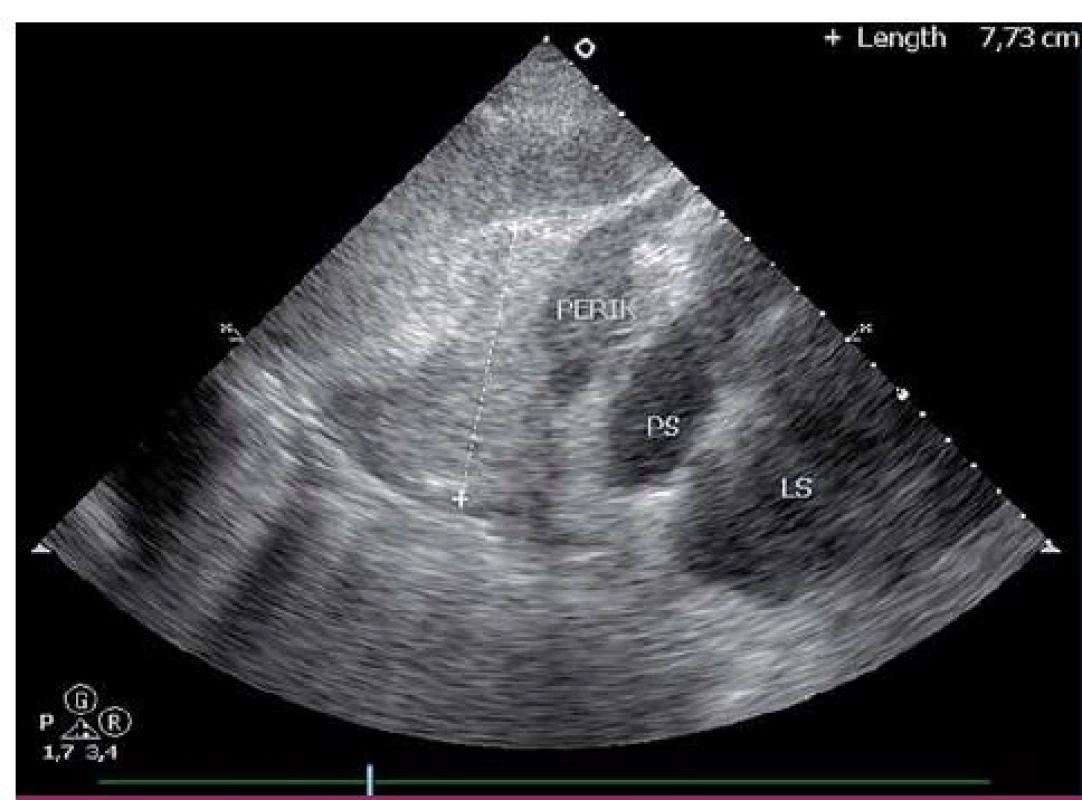
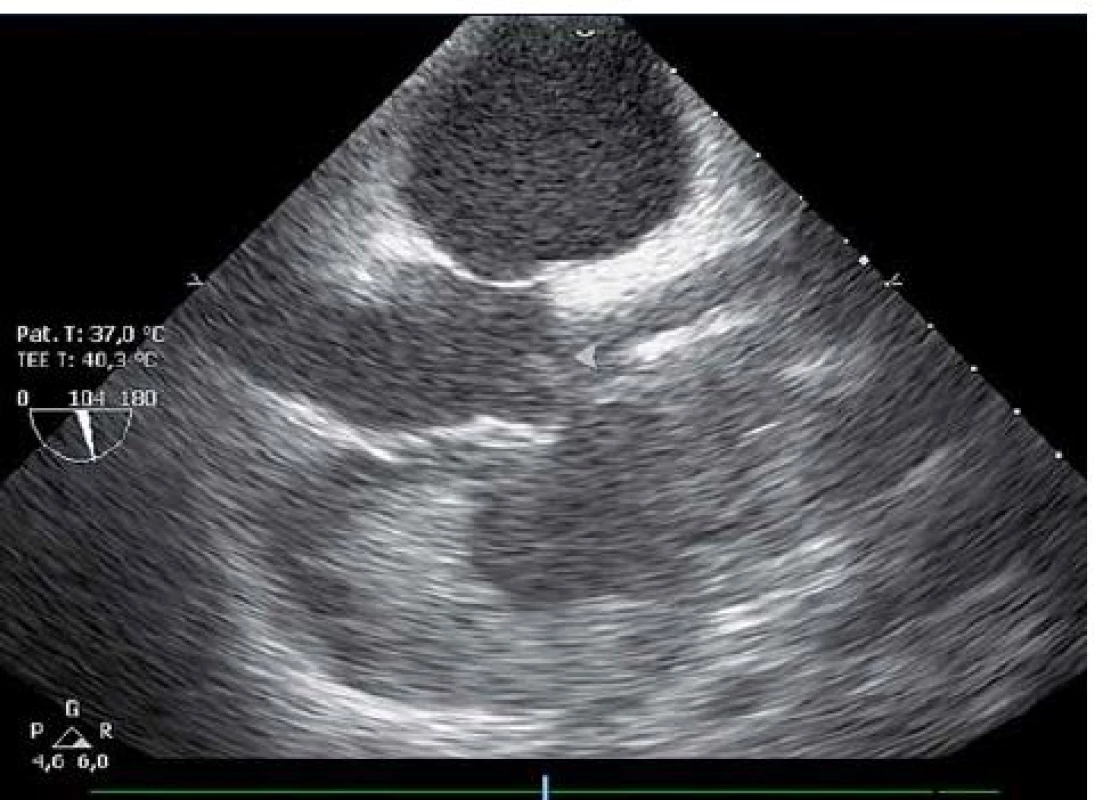
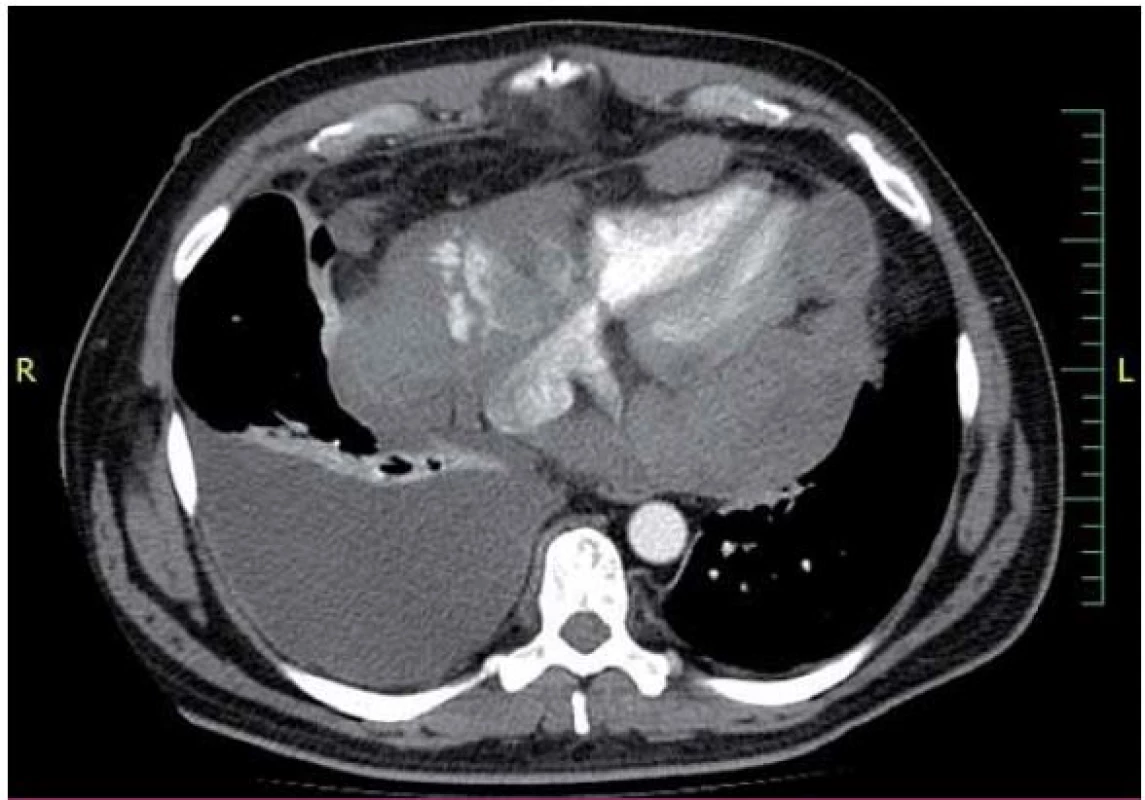
Dvaačtyřicetiletý nemocný byl přijat na Interní oddělení Nemocnice Písek v březnu 2013 pro progredující dušnost a pleurální bolesti. Z osobní anamnézy u pacienta bylo zjištěno, že byl v dětství léčen pro recidivující akutní bronchitidy. Pacient byl nekuřák, alkohol pil příležitostně. V roce 2006 byla provedena cirkumcize. Z rodinné anamnézy byl otec sledován pro diabetes mellitus 2. typu na PAD. Iniciálně byl týden léčen praktickým lékařem pro anginu, nasazen Duomox 1 000 mg po 12 hod. Po týdnu se objevila námahová dušnost a pleurální bolesti vlevo, zhoršující se v noci, teplotu si neměřil, užíval opakovaně Coldrex, v posledních dvou dnech před přijetím se objevil pocit nadýmání, pálení žáhy negoval, váha stabilní, krvácivé projevy nepozoroval. Při vstupním vyšetření auskultačně na srdci zjištěna tepová frekvence 110/ min, šelest nediferencován, zvětšená játra 2 cm pod oblouk, ostatní somatický nález bez nápadností. V úvodu jsme měli podezření na plicní embolii, proto jsme provedli CT AG plicnice (obr. 1), kde byl diagnostikován perikardiální výpotek, oboustranně malé pleurální výpotky, vedlejším nálezem při vyšetření byl zjištěn emfyzém P plíce. Na EKG při přijetí byla sinusová tachykardie. Laboratorně byly prokázány zvýšené zánětlivé markery CRP maximálně 176 mg/ l, FW 85/ 105, leukocytóza, autoprotilátky a virologie s negativním nálezem. Echokardiograficky byl zjištěn rozsáhlý perikardiální výpotek (obr. 2). Při vstupním echokardiografickém vyšetření přítomny některé ze známek srdeční tamponády, zjištěna patologická respirační variace vlny E nad 25 %, P síň systolicky kolabovala, nebyl diastolický kolaps P síně a P komory, dilatovaná dolní dutá žíla a omezená respirační variace dolní duté žíly. Při průběžných kontrolách docházelo ke zlepšení hemodynamických parametrů, přetrvávala patologická respirační variace vlny E. Příčinou byl pravděpodobně vliv emfyzému P plíce. Při dalších echokardiografických kontrolách se objevil hypoechogenní útvar v oblasti P síně (obr. 3). V diferenciální diagnostice byla i úvaha o autoimunitní perikarditidě v rámci polyserositidy vzhledem k tomu, že sonograficky byly zjištěny diskrétní pleurální výpotky, ale imunologická vyšetření neukázala na žádné onemocnění pojiva. Autoimunitní perikarditida byla vyloučena, proto byla další úvahou idiopatická exudativní perikarditida se sekundárními fibrinovými nálety vzhledem k hypoechogennímu útvaru kolem P síně. Pacient byl léčen nesteroidními antirevmatiky a antibiotiky. Laboratorně došlo k poklesu zánětlivých markerů, pacient byl opakovaně echokardiograficky sledován v průběhu hospitalizace a jeden měsíc po propuštění, postupně došlo k úplné regresi perikardiálního výpotku a částečné regresi hypoechogenního útvaru v oblasti P síně. Plánovány další echokardiografické kontroly a dovyšetření plicního emfyzému P plíce na vyšším pracovišti. Pacient se bohužel na další doporučené kontroly nedostavil. V diferenciální diagnostice samozřejmě byla úvaha i o nádorovém onemocnění, v rámci onkologického screnningu byla provedena sonografie břicha, kde byla zjištěna steatóza jater, ostatní orgány bez patologie, onkomarkery B2 – mikroglobulin, LD, Ca19 – 9, CEA byly negativní. O osm měsíců později (listopad 2013) byl přijat na naše oddělení s dušností NYHA III trvající tři týdny, nechutenství a hubnutí poslední měsíc. Týden byl léčen praktickým lékařem antibiotiky z důvodu podezření na akutní bronchitidu. V objektivním nálezu byla dušnost při malé námaze (NYHA III), zvýšená jugulární náplň, tachykardie 110/ min, zvětšená játra, nebyl patrný pulsus parodoxus ani Kusmaulovo znamení, krevní tlak stabilně 110/ 80, poslechově na plicích oslabené dýchání vpravo po úhel lopatky, tepová frekvence 100/ min, zvětšená játra 2 cm pod oblouk. Laboratorně jsme prokázali zvýšené zánětlivé markery CRP s maximem 100 mg/ l, jinak bez patologie. Na EKG byla sinusová tachykardie. V této době byl echokardiograficky diagnostikován rozsáhlý perikardiální výpotek s infiltracemi (obr. 4), v oblasti P síně 8cm heterogenní útvar (obr. 5), podobně intraperikardiální masy i kolem dalších oddílů s perikardiálním výpotkem. Byl přítomen kolaps pravé síně, nebyl diastolický kolaps pravé komory, patologicky vysoká transmitrální a transtrikuspidální variace průtoků (přičemž poměr vlnek E/ A nad chlopněmi byl nad 1), dilatovaná a málo kolapsibilní dolní dutá žíla. Naznačený byl tzv. septal bounce – který mohl být podmíněn konstrikcí, tkáňovým dopplerem byla zjištěna fyziologická diastolická rychlost septálního mitrálního anulu (nad 8 cm/ s) a také poměr maximální rychlosti transmitrální E vlny k maximální rychlosti septálního anulu byl fyziologický. Jícnovou echokardiografií po podání kontrastní látky (agitovaná glukóza 10 %) byla zjištěna perforace stěny pravé síně a komunikace s perikardiálním vakem (obr. 6), doplerovským mapováním nebyla komunikace zřejmá. Dále byl proveden USG pleury vpravo, kde byl diagnostikován velký pleurální výpotek vpravo. Dle CT hrudníku (obr. 7) byly diagnostikovány objemné tumorózní masy v oblasti perikardu a velký pleurální výpotek. U pacienta bylo vysloveno podezření na primární tumor srdce. V průběhu hospitalizace byly opakovaně prováděny punkce pleurálního výpotku vpravo. Kultivace a cytologie výpotku byla negativní. V rámci vyšetřovacího programu byla doplněna kontrolní sonografie břicha, kde byla popsána echogenní ložiska v oblasti jater a sleziny. Indikováno CT břicha a malé pánve, v játrech a slezině byly nalezeny susp. metastázy, vedlejším nálezem byla vícečetná ložiska v plicním parenchymu při obou bazích. Pacient byl dále vyšetřován na vyšším pracovišti, kde bylo doplněno PET/ CT. Dle PET/ CT byly zjištěny objemné tumorózní hmoty perikardu, komunikace s P síní, lymfadenopatie mediastina a jaterním hilu, metastatické postižení jater, sleziny, změny v oblasti plic nejspíše kombinací zánětlivých změn a metastatického postižení, pravděpodobně přítomná infiltrace kostní dřeně, lymfadenopatie na krku velmi suspektně reaktivní. Indikována biopsie z tonsily, při biopsii nebyly zjištěny nádorové buňky, dále provedena trepanobiopsie kostní dřeně, histologicky drobná sekundární dysplazie. U pacienta docházelo ke zhoršování klinického stavu, byly přítomny počínající známky srdeční tamponády, v laboratoři vzestup zánětlivých markerů, bez zjevného infektu, dále rozvoj trombocytopenie a mírné koagulopatie. Po konzultaci s hematology bylo indikováno podání dvou trombokoncentrátů a kanavit. Vzhledem k nejasnému procesu a vyčerpaným vyšetřovacím možnostem ke zjištění diagnózy bylo rozhodnuto o provedení chirurgické excize vzorku z perikardu k identifikaci tumoru. Pooperačně došlo u pacienta k rozvoji multiorgánového selhání. Dva dny poté pacient zemřel. Definitivní diagnóza byla stanovena histologicky. Jednalo se o angiosarkom srdce s generalizací do plic, jater, sleziny a kostní dřeně, vedlejším nálezem byl lobulární emfyzém P plíce.
Diskuze
Exudativní perikarditida je často diagnostikované onemocnění na interních odděleních. Nejčastější formou perikarditidy je idiopatická perikarditida klinicky se projevující perikardiální bolestí, teplotou, může se vyvinout perikardiální výpotek. Základem terapie jsou nesteroidní antirevmatika a klid na lůžku. Dále se vyskytuje virová perikarditida, na kterou máme podezření zejména v případech, kdy zánět navazuje na respirační infekt. Bakteriální perikarditida je onemocnění, kdy je přítomen purulentní výpotek. Infekce se do perikardu šíří hematogenně při sepsi anebo per continuitam z pleury plic nebo při infekční endokarditidě s abscesy. Klinicky jde o septický stav s velmi vážnou prognózou. Léčba spočívá v perikardiální drenáži, určení agens a podání intravenózního ATB + lokální ATB laváži dle citlivosti. Dále je nutno zvažovat perikarditidu u systémových onemocnění pojiva. Do této kategorie patří revmatoidní artritida, systémový lupus erythematodes nebo sklerodermie. Perikarditida ustupuje po nasazení kortikoterapie. Dříve byla častá perikarditida u revmatické horečky, kterou dnes nevídáme. Perikarditidy se také vyskytují u metabolických onemocnění. U rozvinutého obrazu hypothyreozy se najde perikardiální výpotek, který pomalu narůstá, není ale hemodynamicky významný. Terapií je specifická terapie hypotyreózy. Perikarditida u dialyzovaných se pozoruje cca u 10 % nedostatečně dialyzovaných pacientů. V diferenciální diagnostice perikarditid je také nádorové onemocnění [1]. Sekundární nádory se šíří do srdce přímo prorůstáním z okolních orgánů (mezihrudí či plic) či se šíří hemotogenně nebo lymfogenně. Nejčastěji metastazuje do srdce maligní melanom, karcinom plic, karcinom prsu, lymfomy či leukemie. Metastatické postižení je 20 – 40krát častější oproti primárním nádorům srdce. Primární nádory srdce jsou velmi vzácné [2,3]. Sarkomy srdce tvoří 75 % primárních nádorů srdce. Angiosarkom srdce je nejčastější z primárních nádorů srdce, tvoří 30 % všech maligních nádorů srdce. Větší výskyt angiosarkomu srdce je u mužů mezi 30. a 50. rokem (jako u našeho pacienta) [2,4]. Klinicky se může angiosarkom srdce manifestovat jako námahová dušnost, bolesti na hrudi, kašel, synkopa, arytmie či jako projevy srdeční tamponády/ konstrikce [5]. Typicky je angiosarkom lokalizován v oblasti P síně. Častá je invaze do perikardiálního vaku, která vede k rozvoji perikardiálního výpotku, může dojít až k rozvoji srdeční tamponády. U pokročilejších nádorů může být vzácně i ruptura srdeční stěny. Při stanovení diagnózy je již velmi často metastatický proces do jater a do plic [6 – 10]. Základem diagnostiky je transtorakální a transezofageální echokardiografie. Echokardiograficky v principu můžeme vidět tumorózní masy vycházející ze stěny myokardu, resp. masy v perikardu anebo také perikardiální výpotek. Hemodynamicky mohou být tyto nálezy neutrální anebo později mohou způsobovat tamponádu, konstrikci, resp. kombinaci obou [11,12]. Ze zobrazovacích metod se v současné době využívá MR srdce [9,11]. Ke stanovení rozsahu generalizace indikujeme CT či PET/ CT vyšetření. K definitivní identifikaci tumoru se provádí chirurgická excize vzorku z perikardu. U našeho pacienta byla utlačena pravá síň, všeobecné známky tamponády nebyly jasně vyvinuté klinicky ani echokardiograficky. Byla naznačena konstrikce (tzv. septal bounce, což je atypický pohyb interventrikulárního septa podmíněný časným plněním zejména pravé komory v inspiriu), i když echokardiografické vyjádření znesnadňoval současný perikardiální výpotek s modifikací obrazu a plicní emfyzém (nedořešené etiologie), který se také podílel na zvýraznění transmitrálních a transtrikuspidálních průtokových variacích [13]. K jasně vyvinuté tamponádě srdečních oddílů mohly bránit tumorózní srůsty mezi viscerálním a parietálním perikardem nejen v oblasti pravé síně, ale i dalších oddílů, zejména levé komory. Hemodynamické změny hodnocené echokardiograficky se později zvýrazňovaly (při hodnocení vyšším pracovištěm již byl více vyvinutý útlak na pravou síň i známky konstrikce). Restriktivní porucha plnění levé komory nebyla pravděpodobná (nebyla přítomna žádná infiltrativní kardiomyopatie ani známá diastolická dysfunkce levé komory z minulosti, i když by se dalo teoretizovat o tom, že poměrně rozsáhlé tumorózní infiltrace kolem levé komory by mohly výrazně ovlivnit její plnění až ve smyslu restriktivní hemodynamiky, ale toto vylučují fyziologické nálezy tkáňovým dopplerem v oblasti septálního mitrálního anulu). Vyvinula se také perforace v oblasti pravé síně, kterou jsme diagnostikovali pomocí bublinkového kontrastu. Dopplerovským mapováním (color flow mode) nebyla komunikace zřejmá. Je to pochopitelné, protože rychlost toků perforací z dutiny a do dutiny perikardu byla nízká, tedy barevným dopplerovským mapováním při nutnosti nastavení nízkého Nyquistova limitu vznikaly nepřijatelné artefakty vzniklé pohybem srdce a obraz byl nečitelný, v případě nastavení vyššího Nyquistova limitu komunikace pochopitelně nemohla být viditelná. V případě časné diagnózy angiosarkomu je základem chirurgická léčba, která je následována adjuvantní chemoterapií. Ve fázi generalizace je možné použít paliativní chemoterapii. Využívají se čtyři chemoterapeutické režimy CAD (cyklofosfamid, adriamycin/ doxorubicin, dacarbazin), AD (adriamycin), CYVADIC (cyclofosfamid, vinkristin, doxorubicin, dacarbazin) a VAC (vincristin, doxorubicin, cyklofosfamid). V druhé volbě je možné také využít docetaxel (paclitaxel) nebo gemcitabin, dále v případě rezistence na antracykliny se nově využívá multikinázový inhibitor – sorafenib [2,11,14]. Využití radioterapie je omezené z důvodu kardiotoxicity. Reakce na chemoterapii či radioterapii je nepříznivá [10,14,15]. Prognóza pacientů s angiosarkomem je velmi závažná, medián přežití se pohybuje v rozmezí mezi 7 a 12 měsíci [6,7].
Závěr
V našem sdělení demonstrujeme kazuistiku nemocného středního věku s atypickým průběhem angiosarkomu srdce. Jedná se o onemocnění, které je velmi vzácné, ale i přesto je nutno o této diagnóze přemýšlet v diferenciální diagnostice perikarditid. V našem případě byla diagnostika svízelná tím, že průběh onemocnění byl dvoufázový. V první fázi bylo velmi zajímavé, že došlo k úplné regresi perikardiálního výpotku i postupné regresi hypoechogenního útvaru v oblasti P síně a oboustranných pleurálních výpotků. Otázkou tedy je, zda se již při první fázi nejednalo o generalizované onemocnění.
Doručeno do redakce: 10. 11. 2014
Přijato po recenzi: 11. 1. 2015
MUDr. Jana Havelková
www.nemopisek.cz
j.prokopiusova@seznam.cz
Zdroje
1. Maisch B, Seferovič PM, Ristič AD et al. ESC Guidelines. Guidelines on the diagnosis and management of pericardial diseases. Eur Heart J 2004; 25 : 587 – 610.
2. Vaporciyan A, Reardon MJ. Right heart sarcomas. Methodist Debakey Cardiovasc J 2010; 6 : 44 – 48.
3. Burke A, Jeudy J, Virmani R. Cardiac tumours: An update. Heart 2008; 94 : 117 – 123.
4. Shapiro L. Cardiac tumours: diagnosis and management. Heart 2001; 85 : 218 – 222.
5. Vander Salm TJ. Unusual primary tumors of the heart. Semin Thorac Cardiovasc Surg 2000; 12 : 89 – 100.
6. Šteiner I. Kardiopatologie pro patology i kardiology. Praha: Galén 2010 : 116 – 118.
7. Mladosievičová B et al. Kardionkologie. Praha: Grada Publishing 2014 : 175 – 178.
8. Adam Z, Vorlíček J, Vaníček J et al. Diagnostické a léčebné postupy u maligních chorob. Praha: Grada Publishing 2012 : 331.
9. Mašek M, Vaněčková M, Burgetová A et al. Angiosarkom pravé síně. Cesk Radiol 2010; 64 : 226 – 229.
10. Handl L, Hromádka M, Hájek T et al. Angiosarkom pravé síně. Cor Vasa 2011; 53 : 722 – 725.
11. Kakizaki S, Takagi H, Hosaka Y. Cardiac anoagisarcoma responding to multidisciplinary treatment. Int J Cardiol 1997; 62 : 273 – 275.
12. Peters PJ, Reinhardt S. The echocardiographic evaluation of intracardiac masses: a review. J Am Soc Echocardiogr 2006; 19 : 230 – 240.
13. Paleček T, Němeček E, Fikrle M et al. Echokardiografie konstriktivní perikarditidy. Postgraduální medicína. 2012; 14, příloha 1/ 2012 : 26 – 29.
14. Ostrowski S, Macinkewicz A, Kosmider A et al. Sarcomas of the heart as a difficult interdisciplinary problem. Arch Med Sci 2014; 10 : 135 – 148. doi: 10.5114/ aoms.2014.40741.
15. Leja MJ, Shah DJ, Reardon MJ. Primary cardiac tumors. Tex Heart Inst J 2011; 38 : 261 – 262.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2015 Číslo 1
-
Všechny články tohoto čísla
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- Nové studie dávají naději na zlepšení terapie aterosklerózy
-
Hlavolamy 2015
Propojení kardiologie a diabetologie - Vyhlášení výsledků autorské soutěže O nejlepší kazuistiku v roce 2014
- Vývoj a úkoly klinické farmakologie ve zdravotnické péči v ČR
- TDM antibiotik v klinické praxi
- prof. MUDr. Josef Veselka, CSc., FESC, FSCAI, FICA (*23. 3. 1965)
- TDM digoxinu v klinické praxi
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
