Katetrizační léčba fibrilace síní
Catheter ablation of atrial fibrillation
Catheter ablation of atrial fibrillation is currently the most effective specific antiarrhythmic therapy. The technique of the procedure is steadily developing and its safety and efficacy is growing. The article presents an overview of the basic aspects of catheterization treatment, including the indications, pathophysiology, new technologies and techniques of catheter ablation of atrial fibrillation.
Keywords:
atrial fibrillation – catheter – ablation – history – pathophysiology – technique – complications – indications
Autoři:
V. Durdil
Působiště autorů:
Kardiologická klinika 2. LF UK a FN v Motole, Praha
Vyšlo v časopise:
Kardiol Rev Int Med 2015, 17(1): 28-31
Kategorie:
Kardiologická revue
Souhrn
Katetrizační léčba fibrilace síní je v současnosti nejúčinnější metodou léčby této arytmie. Technika výkonu se trvale vyvíjí, zvyšuje se jeho bezpečnost a efektivita. Přehledně jsou uvedeny základní aspekty katetrizační léčby včetně indikací, patofyziologického podkladu, nových technologií a technik katetrizační ablace fibrilace síní.
Klíčová slova:
fibrilace síní – katetrizační – ablace – historie – patofyziologie – technika – komplikace – indikace
Fibrilaci síní lze nazvat civilizačním onemocněním. Její prevalence ve vyspělých zemích v posledních desetiletích neustále stoupá a v současné době dosahuje až 2 %. Fibrilace síní významně zvyšuje morbiditu i mortalitu a její léčba je cenově nákladná. Katetrizační metody terapie fibrilace síní patří v posledních letech mezi nejdynamičtěji se rozvíjející oblasti kardiologie. Narůstá jak počet provedených výkonů, tak počet center, která výkony provádějí. V České republice je provedeno přibližně 2 500 výkonů ročně, a patří tak v počtu výkonů na počet obyvatel na přední místa v Evropě a na světě.
Historie
První katetrizační ablace v léčbě fibrilace síní v podstatě kopírovaly přístup chirurgický a spočívaly v tvorbě lineárních lézí v síních. Tento přístup byl technicky náročný a byl zatížen velkým rizikem komplikací. Přelomovou prací v oblasti katetrizační léčby fibrilace síní byla publikace Haissaguerra et al z pracoviště v Bordeaux z roku 1998, která popisuje plicní žíly jako nejčastější zdroj ektopie spouštějící fibrilaci síní a katetrizační ablaci těchto zdrojů jako účinnou metodu prevence rekurence této arytmie [1]. Stejná skupina rozpracovala metodu segmentální izolace plicních žil pod skiaskopickou kontrolou. Dalším milníkem pak bylo Papponem et al v roce 2000 publikované užití trojrozměrných mapovacích systémů, které umožňovalo vytvoření široce obkružujících lézí okolo plicních žil [2]. Tento postup zůstává v různých modifikacích základem katetrizační léčby dodnes. V posledních letech začala být používána řada postupů zpřesňující anatomickou orientaci, tvorbu léze a mapování substrátu.
Patofyziologický podklad
Porozumění patofyziologii fibrilace síní je limitováno možnostmi mapování tak komplexního jevu, jakým fibrilace svaloviny síní je. Zjednodušeně lze říci, že ke vzniku a udržení fibrilace je třeba spouštěč, substrát a případně zevní modulující faktory.
Spouštěčem fibrilace síní je ektopická síňová aktivita. Nejčastějším zdrojem této ektopie jsou ostia plicních žil. Svalová vlákna mají v těchto oblastech různou orientaci a vzájemně se překrývají. Zároveň mají kratší refrakterní periodu než okolní myokard síní. Mapování a následná ablace ektopické aktivity je za použití současné technologie relativně efektivní.
Substrát arytmie může být definován anatomicky nebo elektrofyziologicky. Anatomickým korelátem substrátu mohou být ložiska fibrózy. Metody katetrizační ablace cílené na fibrózu detekovatelnou například pomocí magnetické rezonance se zdají být relativně úspěšné. Limitací nicméně zůstává možnost zobrazení fibrózy, kdy detekce pozdního sycení Gadoliniem při magnetické rezonanci má nízkou reproducibilitu. V oblasti elektrofyziologického mapování substrátu bylo v posledních letech dosaženo velkého pokroku. Iniciální teorie mnohočetných reentry okruhů jsou postupně nahrazovány teorií rotorů – jakýchsi vln depolarizace kroužících okolo jednoho bodu. Zobrazení rotoru je možné pomocí mapování fáze elektrického signálu získaného buď intrakardiálně multipolárním katetrem, nebo pomocí zevní multielektrodové vesty. Mapováním bylo zjištěno, že rotory jsou u daného jedince poměrně stabilní. Celkem se může vyskytovat až několik rotorů a často se vyskytují v oblastech anter plicních žil. Používané jsou též metody ablace zaměřené na okrsky frakcionovaných potenciálů detekovatelných klasickým mapováním, jenž se zdají být jakýmsi korelátem rotorů.
Z řady modulujících faktorů podílejících se na vzniku fibrilace síní lze katetrizačně ovlivnit například autonomní nervový systém ablací v oblasti gangliových plexů detekovatelných rychlou elektrickou stimulací.
Technika
Základem většiny metod katetrizační léčby fibrilace síní je izolace plicních žil obkružujícími lézemi. Toho lze dosáhnout jak aplikací radiofrekvenčí energie bod po bodu nebo multielektrodovými ablačními katetry, tak pomocí speciálních balonů za využití kryoablace či laseru. Zatímco v průběhu radiofrekvenční ablace je využíváno systémů trojrozměrného mapování, ablaci balony lze provádět pouze za skiaskopické kontroly. Efektivita všech uvedených metod je přibližně srovnatelná. Izolace plicních žil obkružujícími lézemi zasahuje jak spouštěč, tak částečně i substrát arytmie a je metodou volby u paroxysmální fibrilace síní. Při perzistenci arytmie i po izolaci plicních žil se v případě tzv. stupňovité strategie přistupuje k lineárním lézím, nejčastěji na stropu levé síně a v oblasti mezi mitrálním anulem a ablační linií u levé dolní plicní žíly. Za určitých podmínek může být efektivní i elektrická izolace ouška levé síně. Data z poslední doby však zpochybňují efektivitu lineárních lézí, které navíc mohou působit proarytmogenně. Na obr. 1 je zobrazena elektroanatomická mapa při izolaci plicních žil široce obkružujícími lézemi za použití radiofrekvenční energie ablací bod po bodu.
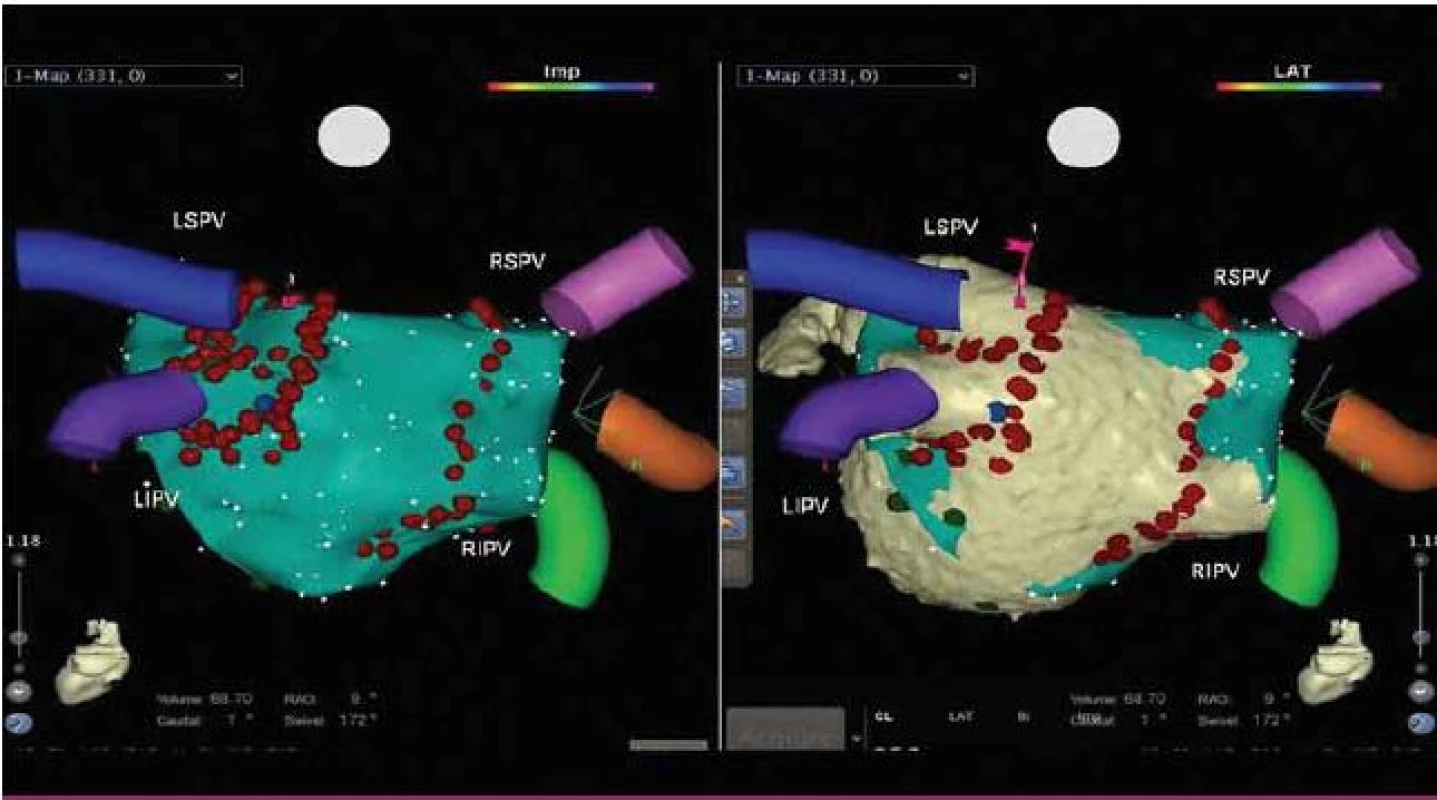
S rozvojem možností mapování fibrózy a rotorů v oblasti síní jsou do praxe zaváděny výkony cílící přímo na substrát arytmie. První data z jednotlivých center ukazují podstatně vyšší efektivitu takto vedených výkonů než v případě výkonů standardních.
Ke zvýšení účinnosti a zejména bezpečnosti významně přispívá též řada ostatních metod, které jsou již v klinické praxi běžně užívány. V oblasti zobrazovacích metod jsou to zejména integrace elektroanatomické mapy s obrazem z výpočetní tomografie či magnetické rezonance. Významným přínosem je použití intrakardiální echokardiografie, která kromě využití při transseptální punkci umožňuje jak zpřesnění lokalizace ostií plicních žil, tak kontrolu ablace a případných komplikací v průběhu výkonu. Další z metod využívaných k integraci s elektroanatomickou mapou je rotační angiografie. Její výhodou je její vysoká kvalita a možnost záznamu přímo na katetrizačním sále v průběhu výkonu.
Řada systémů je zaměřena na zlepšení možností manipulace s katetry. V současnosti užívané systémy stereotaktické magnetické navigace či robotické navigace pomáhají zvýšit přesnost a bezpečnost manipulace katetrem, zjednodušit výkon pro operatéra a snížit radiační expozici personálu. Velkým přínosem pro bezpečnost a účinnost katetrizační ablace je technologie měření síly přítlaku katetru, která začala být v poslední době široce užívána.
Efektivita
V současnosti je k dispozici velké množství dat z klinických studií s pacienty, kteří podstupují katetrizační ablaci pro fibrilaci síní. Řada z nich srovnává katetrizační ablaci s antiarytmickou terapií. U pacientů s paroxysmální i perzistentní formou je v tomto srovnání katetrizační ablace významně účinnější. V míře účinnosti se však dostupná data výrazně liší dle pracoviště, techniky výkonu, léčené populace i zvolené následné monitorace pacientů. U pacientů s paroxysmální formou fibrilace síní je po izolaci plicních žil bez recidivy arytmie přibližně 60 – 70 % z nich při standardní monitoraci. V případě perzistentní fibrilace síní je po dobu jednoho roku od výkonu při užití stupňovité strategie ablace bez arytmie přibližně 40 – 50 % pacientů. Při dlouhodobém sledování je nutnost opakování procedury přibližně u 30 % pacientů v průběhu dvou let [3].
Chybí data srovnávající katetrizační léčbu se strategií kontroly frekvence. Na toto téma v současnosti studie probíhají a výsledky se očekávají v horizontu několika let.
Bezpečnost
Katetrizační ablace fibrilace síní je výkon komplexní a může být zatížen řadou komplikací. Mortalita spojená s tímto výkonem se pohybuje obdobně jako v případě jiných katetrizačních výkonů okolo 0,1 %. V průběhu výkonu je vždy nutno nalézt rovnováhu mezi bezpečností a účinností. Mezi nejobávanější akutní komplikace patří perforace srdce a systémová embolizace. Každá z těchto komplikací má incidenci přibližně 1 %. Perforace srdce bývá nejčastěji způsobena při vlastní aplikaci ablační energie, zejména v případě déletrvající aplikace v místech s výrazným přítlakem katetru. Méně často dochází k perforaci srdce při transseptální punkci. Perforace srdce je život ohrožující stav a vyžaduje často urgentní perikardiální punkci a případně kardiochirurgickou suturu místa perforace. Systémová embolizace se nejčastěji projevuje jako tranzitorní ischemická ataka, méně často jako ischemická cévní příhoda s trvalými následky. Řada embolizací je zcela asymptomatická a je detekovatelná pouze zobrazovacími metodami či laboratorně za použití markerů poškození centrálního nervového systému (CNS). Prevencí kardioembolizačních komplikací je kromě intravenózní antikoagulace heparinem v průběhu výkonu též ponechání perorální antikoagulační terapie perioperačně, a to jak warfarinu, tak přímých orálních antikoagulancií. Tento postup nezvyšuje riziko pro pacienta při perforaci srdce, naopak překrývání nízkomolekulárním heparinem v případě vysazení perorální antikoagulace je spojeno s vyšším rizikem krvácení v období po výkonu. Prevencí kardioembolizačních komplikací je též pečlivá příprava pacienta s vyloučením trombózy v oblasti ouška levé síně obdobně jako v případě přípravy před elektrickou kardioverzí.
V průběhu ablace může též dojít k poškození tkání přilehlých k srdci, jako jsou jícen, pleteně gastrických nervů či brániční nerv. Obávaná atrioezofageální píštěl je velmi vzácná, avšak může docházet dle lokalizace poškození k různé míře porušení sliznice jícnu, poruše motility jícnu nebo žaludku či paréze bránice. Prevencí této skupiny komplikací je omezení použité ablační energie v oblasti zadní stěny levé síně a monitorace teploty uvnitř jícnu. K paréze bránice dochází častěji při používání kryoablace pomocí balonu, kdy je pozorovaná incidence až 6 %. Paréza bývá v těchto případech nejčastěji přechodná. V průběhu kryoablačních výkonů je proto kontrolována funkce bráničního nervu jeho kontinuální elektrickou stimulací zavedeným katetrem. Jako reakce na poškození perikardu ablací může mít část pacientů po výkonu reaktivní perikarditidu s klinickými projevy, jako jsou bolesti na hrudi či perikardiální výpotek. Stenózy plicních žil jsou od zavedení široce obkružujících ablačních lézí jen sporadické. Tab. 1 uvádí souhrnně nejčastější komplikace katetrizační ablace fibrilace síní a jejich frekvenci dle publikovaného souboru 20 000 výkonů z let 2003 – 2006 [4].
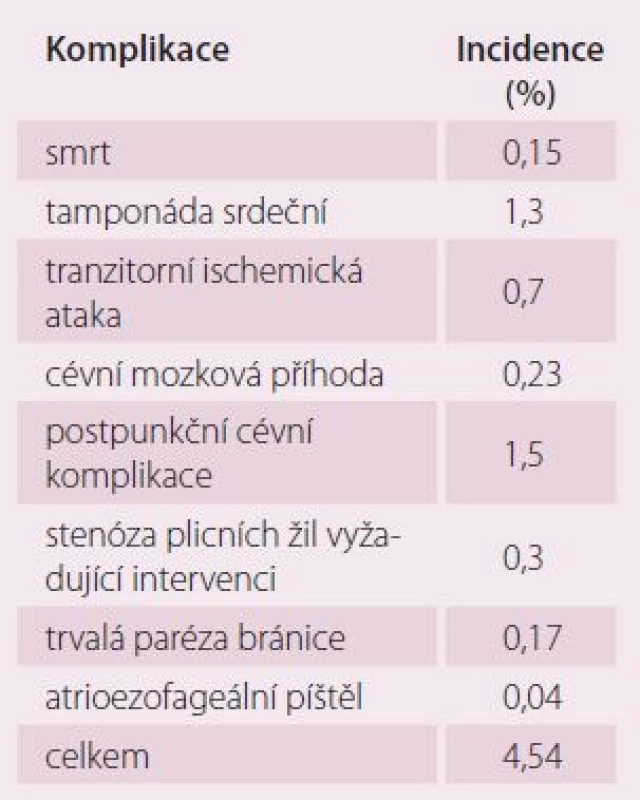
K redukci počtu komplikací přispívá jak pečlivá selekce a příprava pacienta před výkonem, tak opatrnost při vlastním výkonu, zejména omezení aplikované energie v oblasti zadní stěny levé síně, maximální přehled o anatomii v místech ablace a vyvarování se výrazného přítlaku katetru s dlouhými aplikacemi ablační energie. Toho se v řadě případů daří dosáhnout za použití nových technologií monitorace, mapování nebo kontroly přítlaku katetru.
Indikace
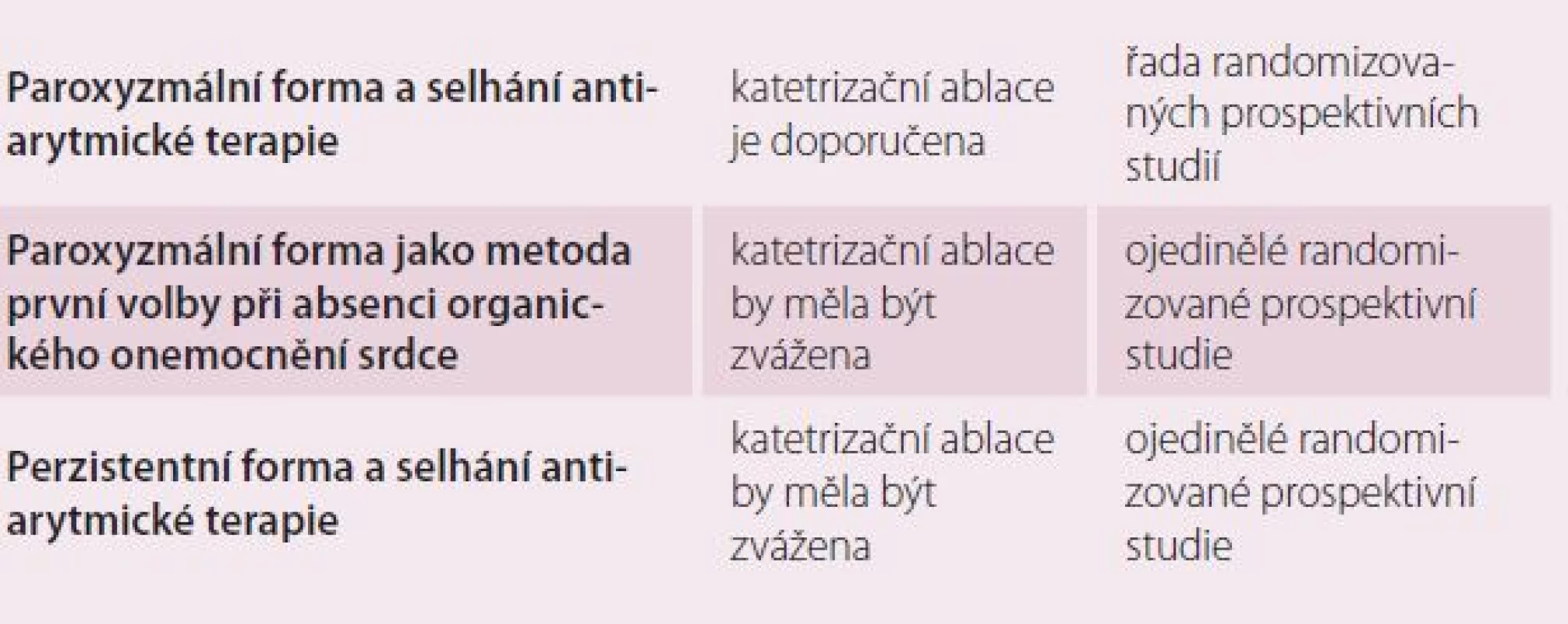
Výkon je indikován ke snížení symptomů pacienta. Dosud nebylo prokázáno snížení mortality či rizika tromboembolických komplikací po katetrizační ablaci fibrilace síní. Řada pacientů však fibrilaci síní špatně toleruje a má výrazně sníženou kvalitu života. Zejména se jedná o mladší aktivní pacienty bez jiných limitujících komorbidit. V takovýchto případech je katetrizační ablace metodou volby. Po dohodě s pacientem lze před případným katetrizačním výkonem nejprve začít s terapií antiarytmiky. Antiarytmická terapie bývá však jen omezeně účinná, často hůře tolerovaná a v neposlední řadě zatížená řadou nežádoucích účinků, zejména v předpokládaném dlouhodobém užívání u mladších pacientů. Několik klinických studií v poslední době prokázalo katetrizační ablaci fibrilace síní jako metodu první volby srovnatelnou s přístupem katetrizační ablace až po selhání antiarytmické terapie. V tab. 2 jsou uvedena indikační kritéria ke katetrizační ablaci fibrilace síní dle aktuálních doporučených postupů Evropské kardiologické společnosti z roku 2012 [5]. V případě indikace hraje výraznou roli též očekávaná efektivita a bezpečnost výkonu. Nejefektivnější je katetrizační ablace v případě paroxyzmální formy, kdy ataky arytmie spontánně terminují. V případě forem, kdy fibrilace síní vyžaduje opakované kardioverze, je očekávaný benefit ablační léčby nižší. Konečně u dlouhodobě perzistentní arytmie, kdy se předpokládá rozsáhlá remodelace myokardu levé síně, je efektivita výkonu nejmenší a v procesu rozhodování o další terapii se spíše postupuje konzervativně. Obdobně vyšší věk pacientů a významná přidružená onemocnění limitují indikaci ke katetrizační ablaci vzhledem k vyššímu očekávanému riziku výkonu. Ke každému pacientovi je však nutno přistupovat individuálně a řádně s ním konzultovat přínosy a rizika výkonu stejně jako možnost nutnosti opakování výkonu v budoucnu. V současné době neexistuje pro katetrizační ablaci fibrilace síní věkový limit. V případě starších, rizikových a výrazně symptomatických pacientů však zůstává alternativou ke katetrizační ablaci fibrilace síní ablace atrioventrikulární junkce s implantací trvalého kardiostimulátoru.
Sledování pacientů po výkonu
V období po výkonu je nutno se zaměřit na možné pozdní komplikace, jako jsou atrioezofageální píštěl, parézy bránice či poruchy motility gastrointestinálního traktu. Mezi klinické projevy atrioezofageální píštěle řadíme hematemézu nebo projevy septikemie, jako jsou horečka, zimnice či třesavka. Supraventrikulární arytmie v období tří měsíců po výkonu mohou být projevem hojení léze a vytváření jizvy a nemusejí znamenat vyšší riziko arytmií v budoucnu. V tomto časném období je snaha o kontrolu rytmu pomocí kardioverze či antiarytmik, avšak jen zřídka je indikována katetrizační ablace. Obdobně, pokud pacient užíval před katetrizační ablací antiarytmika, je vhodné je po tuto přechodnou dobu po výkonu ponechat, případně pouze redukovat jejich dávku.
Antikoagulační terapii ponecháváme minimálně dva měsíce po výkonu u všech pacientů a pokračování terapie po této době určujeme dle standardně stanoveného rizika tromboembolických komplikací. Případné vysazení antikoagulační léčby u pacientů s vyšším rizikem tromboembolie je možné až po vyloučení recidiv fibrilace síní nejlépe dlouhodobými formami monitorace, jako jsou monitorace epizodním záznamníkem či opakované vícedenní elektrokardiografické monitorace.
Perspektivy
Vzhledem ke stoupající prevalenci fibrilace síní lze očekávat pokračování nárůstu počtu katetrizačních ablací v této indikaci jako zatím suverénně nejúčinnější antiarytmické terapie. Současně je velmi pravděpodobné, že bude pokračovat zdokonalování stávajících technik výkonu a vývoj technik nových, zejména s ohledem na rozvíjející se možnosti mapování vlastního substrátu arytmie. Případnou změnu stávajících indikací je pak možné očekávat na základě výsledků aktuálně probíhajících klinických studií zaměřených na mortalitu pacientů.
Doručeno do redakce: 10. 1. 2015
Přijato po recenzi: 22. 1. 2015
MUDr. Václav Durdil
www.fnmotol.cz
vdurdil@gmail.com
Zdroje
1. Haissaguerre M, Jais P, Shah DC et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998; 339 : 659 – 666. doi: 10.1056/ NEJM1998.09033391003.
2. Pappone C, Rosanio S, Oreto G et al. Circumferential radiofrequency ablation of pulmonary vein ostia: A new anatomic approach for curing atrial fibrillation. Circulation 2000; 102 : 2619 – 2628. doi: 10.1161/ 01.CIR.102.21.2619.
3. Shah RU, Freeman JV, Silane D et al. Procedural complications, rehospitalizations, and repeat procedures after catheter ablation for atrial fibrillation. J Am Coll Cardiol 2012; 59 : 143 – 149. doi:10.1016/ j.jacc.2011.08.068.
4. Cappato R, Calkins H, Chen SA et al. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010; 3 : 32 – 38. doi: 10.1161/ CIRCEP.109.859116.
5. Camm AJ, Lip GY, De Caterina R et al. 2012 focused update od the ESC Guidelines for the management of atrial fibrillation. Eur Heart J 2012; 33 : 2719 – 2747. doi: 10.1093/ eurheartj/ ehs253.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2015 Číslo 1
-
Všechny články tohoto čísla
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- Nové studie dávají naději na zlepšení terapie aterosklerózy
-
Hlavolamy 2015
Propojení kardiologie a diabetologie - Vyhlášení výsledků autorské soutěže O nejlepší kazuistiku v roce 2014
- Vývoj a úkoly klinické farmakologie ve zdravotnické péči v ČR
- TDM antibiotik v klinické praxi
- prof. MUDr. Josef Veselka, CSc., FESC, FSCAI, FICA (*23. 3. 1965)
- TDM digoxinu v klinické praxi
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
