Carvedilol v léčbě kardiovaskulárních onemocnění
Carvedilol as a treatment option for cardiovascular diseases
At present, beta‑blockers represent the basic and life ‑ saving treatment modality used for many diseases of the cardiovascular system, particularly for hypertension, ischemic heart disease, heart rhythm disorders and heart failure. Many of them had been a subject to clinical testing that has proven not just their effi cacy but also their safety. Carvedilol is one of the clinically tested and frequently used beta‑blockers, particularly in the treatment of chronic heart failure. This is a non‑selective beta‑blocker with vasodilatatory effects. The paper describes its pharmacological and clinical effects in the treatment of cardiovascular diseases.
Key words:
carvedilol – beta‑blockers – heart failure – hypertension – IHD – arrhythmias
Autoři:
J. Jež; J. Vítovec
Působiště autorů:
I. interní kardioangiologická klinika LF MU a FN u sv. Anny v Brně
Vyšlo v časopise:
Kardiol Rev Int Med 2010, 12(1): 28-31
Souhrn
Betablokátory dnes patří mezi základní a život zachraňující léky používané u mnoha onemocnění kardiovaskulárního systému, především hypertenze, ischemické choroby srdeční, poruch srdečního rytmu a srdečního selhání. Řada z nich prošla klinickými studiemi, které nejen prokázaly jejich účinnost, ale také jejich bezpečnost. Jedním z klinicky prověřených a často používaných betablokátorů, a to především v léčbě chronického srdečního selhání, je carvedilol. Patří mezi neselektivní betablokátory s vazodilatačními účinky. V článku je popsán jeho farmakologický a klinický účinek v léčbě kardiovaskulárních onemocnění.
Klíčová slova:
carvedilol – betablokátory – srdeční selhání – hypertenze – ICHS – arytmie
Úvod
V rozvinutých zemích dosahuje výskyt kardiovaskulárních onemocnění bezesporu epidemického rozměru. Mnoho pacientů je odkázáno na doživotní medikamentózní léčbu a opakované hospitalizace. Nemocnost a invalidizace nemocných s sebou přináší také značné ekonomické náklady na lékařskou a ošetřovatelskou péči. Byly nasazeny nemalé prostředky na vývoj a výzkum preparátů určených k léčbě a potlačení příznaků kardiovaskulárních onemocnění. Jedním z důležitých léků, nalézajících své uplatnění především v léčbě chronického srdečního selhání, je carvedilol – betablokátor, který svým účinkem vede ke snížení morbidity i mortality. Tento lék byl v září roku 1995 v USA nejprve schválen pro léčbu pacientů s esenciální hypertenzí a od května roku 1997 na základě výsledků několika klinických studií [1 – 5] byl jako první betablokátor v USA schválen pro léčbu symptomatického srdečního selhání. U nás je indikován hlavně pro léčbu srdečního selhání, u nemocných po srdečním infarktu se sníženou funkcí levé komory, stabilní anginy pectoris a hypertenze [6].
Farmakologické vlastnosti carvedilolu
Carvedilol je neselektivní blokátor beta‑adrenoreceptorů a současně také blokátor α‑1‑adrenoreceptorů (obr. 1). Carvedilol patří k betablokátorům bez vnitřní sympatomimetické aktivity (intrinsic sympathomimetic activity –ISA), má antioxidační aktivitu a membrány stabilizující účinek. Většina vazodilatační aktivity spočívá v jeho schopnosti blokovat alfa‑1‑receptory, ve vyšších koncentracích zabraňuje vstupu vápníku do hladkých svalových buněk cév a také do myokardiálních buněk.
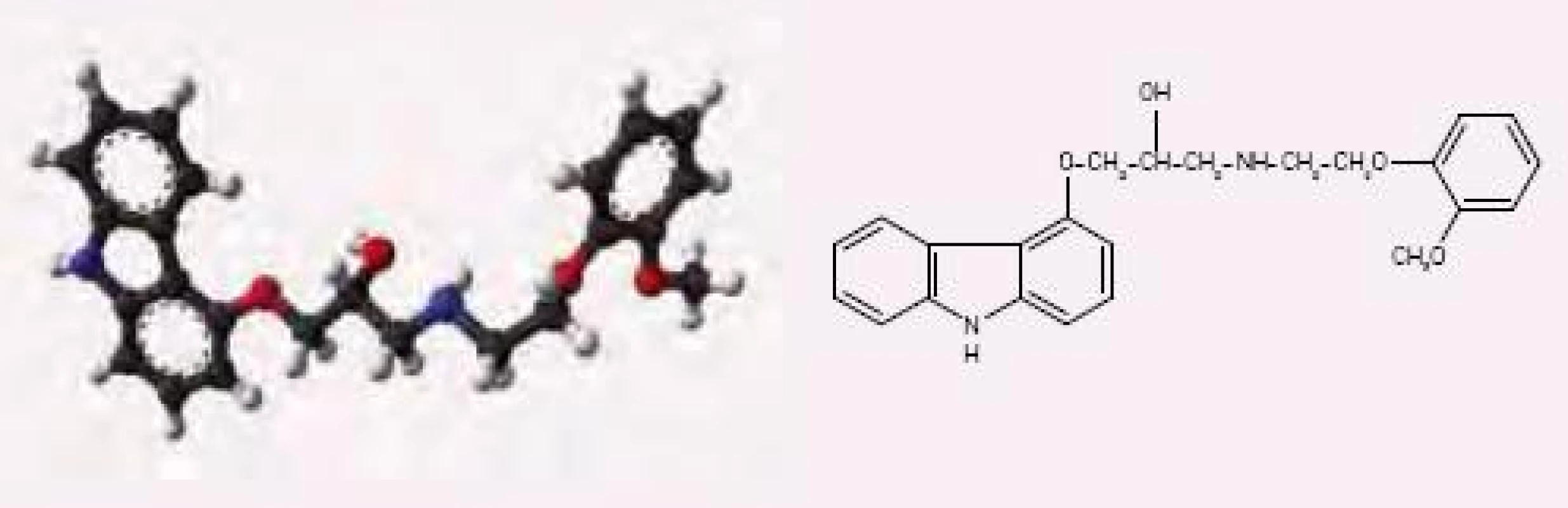
Po perorálním podání se rychle a kompletně vstřebává [7]. Maximální plazmatická koncentrace je dosažena asi za 1 až 2 hod, při podání s jídlem se absorpce zpožďuje o 60 – 135 min [9]. Carvedilol je z větší části stereoselektivně metabolizován při prvním průchodu játry [10]. V plazmě je z 98 % vázán na krevní bílkoviny, převážně na albumin, biologický poločas carvedilolu je asi 7 až 10 hod [7].
Carvedilol je metabolizován v játrech v aromatickém oxidativním cyklu a dále glukuronidací [10]. Metabolity jsou vylučovány do žluče a následně do stolice; jen asi 16 % se vylučuje močí. I některé metabolity si zachovávají betablokační aktivitu, přičemž jedenz nich je dokonce asi 13krát účinnější než samotný carvedilol [8]. Metabolizmus carvediloluje ovlivněn genetickými polymorfizmy cytochromu P‑450 2D6 [11]. Vylučování carvedilolu je zpomaleno u pacientů starších 65 let, v průměru je u nich plazmatická koncentrace o 50 % vyšší než u mladších. Také u jaterních onemocnění se plazmatická koncentrace zvyšuje, nicméně biologický poločas léku je nezměněn. Při onemocnění ledvin bývá nepatrně vyšší plazmatická hladina carvedilolu, jeho farmakokinetika není ovlivněna hemodialýzou. Z důležitých léků metabolizmem carvedilolu není ovlivněna farmakokinetika warfarinu, mírně se zvyšuje plazmatická koncentrace digoxinu.
Městnavé srdeční selhání způsobuje intestinální edém, čímž dochází k redukci absorpce léku. Nicméně pacienti se srdečním selháním (zvláště funkční třídy NYHA IV) mají často vyšší plazmatickou koncentraci carvedilolu než jejich zdraví vrstevníci, protože srdeční selhání snižuje srdeční výdej, klesá perfuze jater, dochází k jaterní kongesci a tak k zpomalení jaterního metabolizmu léků a samozřejmě také farmakokinetiky carvedilolu [9].
Hypertenze a carvedilol
I když na základě výsledků klinických studií [8,12] byl carvedilol schválen k léčbě lehké až středně těžké systémové hypertenze, přece jen zůstává jeho role v této indikaci spíše okrajová. Bývá použit buď v monoterapii v dávce od 6,25 mg do 25 mg dvakrát denně, nebo v kombinaci s ostatními antihypertenzivy. Také s ohledem na vyšší cenu a nová doporučení pro léčbu hypertenze nebývá lékem první volby u nekomplikované hypertenze, i když ve srovnávacích klinických zkouškách byl antihypertenzivní účinek carvedilolu o něco výhodnější než u jiných betablokátorů [6,13].
Ischemická choroba srdeční a carvedilol
Carvedilol podobně jako ostatní betablokátory redukuje frekvenci anginózních záchvatů a zátěží indukované ischemie myokardu u pacientů s chronickou stabilní anginou pectoris. Výhodné je tedy jeho použití především u ischemického postižení myokardu s depresí systolické funkce, u nichž se vedle příznivého ovlivnění průběhu srdečního selhání uplatňuje ještě antianginózní účinek. V malých srovnávacích studiích byla účinnost carvedilolu v této indikaci stejná v porovnání s jinými betablokátory a nifedipinem [14 – 15]. Ve studii se 151 pacienty s akutním infarktem myokardu snižoval carvedilol signifikantně frekvenci srdečních příhod včetně úmrtí, recidiv infarktu a počet urgentních kardiochirurgických revaskularizací ve srovnání s placebovou skupinou [16]. Ve studii CAPRICORN byl prokázán příznivý vliv carvedilolu u nemocných po IM s porušenou funkcí levé komory [17].
Chronické srdeční selhání a carvedilol
Vzhledem ke známému negativně inotropnímu účinku betablokátorů se lékaři po mnoho let domnívali, že jsou pro léčbu srdečního selhání nevhodné [18]. Ale jako první je použil F. Waagstein a spolupracovníci již v roce 1975, což zpočátku vyvolalo v odborných kruzích negativní reakce. Vycházel z předpokladu, že průběh tohoto onemocnění je nepříznivě ovlivněn aktivací neurohumorální osy renin‑angiotenzin‑aldosteron a aktivací sympatického nervového systému [19 – 21]. Proto modulace sympatického nervového systému beta‑adrenergní blokádou příznivě ovlivňuje průběh srdečního selhání [20] a společně s použitím inhibitorů angiotenzin konvertujícího enzymu zlepšuje přežití a snižuje morbiditu pacientů.
Zvýšená aktivita sympatiku je spojena s intolerancí zátěže [20], hemodynamickými abnormalitami [22] a zvýšenou mortalitou. Nárůst sympatikotonie může potencovat aktivitu reninu a angiotenzinu vedoucí k retenci vody a solí, arteriální a venokonstrikci a zvyšuje srdeční předtížení i dotížení [20]. Nadměrná aktivita katecholaminů může vést ke zvýšení srdeční frekvence, vazokonstrikci v koronárním řečišti a snížení průtoku krve myokardem, navíc katecholaminy mohou snížit kontraktibilitu myokardu i na celulární úrovni [23]. Také mohou stimulovat růst a provokovat oxidační stres u terminálně diferencovaných kardiomyocytů; tyto dva faktory vedou k procesu programované buněčné smrti (apoptózy). A konečně, katecholaminy díky nepříznivému ovlivnění elektrofyziologických procesů selhávajícího srdce snižují práh pro komorovou fibrilaci a tím zvyšují riziko náhlé smrti u pacientů se srdečním selháním [24 – 25].
Důkaz účinnosti carvedilolu u pacientů se srdečním selháním přinesl poprvé tzv. U. S. Carvedilol Heart Failure Program spojující čtyři koordinované studie s celkově 1 904 pacienty funkční třídy NYHA II ‑ IV a s ejekční frakcí levé komory pod 35 % [1 – 4]. I když mortalita nebyla předem plánovaným primárním cílem ani jedné ze čtyř studií, byl U. S. Carvedilol Heart Failure Program na doporučení bezpečnostní monitorovací komise předčasně ukončen v roce 1995 na základě dat právě o snížení mortality pacientů léčených carvedilolem [26].
Studie probíhající v Austrálii a na Novém Zélandě si kladla za cíl vyhodnotit klinické a fyziologické důsledky léčby carvedilolem u pacientů s lehkým až středně těžkým srdečním selháním ischemické etiologie, kteří již byli léčeni diuretiky a inhibitory angiotenzin konvertujícího enzymu (ACE) a jejichž klinický stav byl stabilizovaný nejméně jeden měsíc před zařazením. Primární cíl bylo úmrtí nebo hospitalizace z jakéhokoliv důvodu. Výsledkem bylo, že po 18 a více měsících léčby byl počet úmrtí či hospitalizací o 26 % nižší v carvedilolové skupině v porovnání s placebem (P = 0,02) [5].
Na základě výsledků U. S. Carvedilol Heart Failure Program a studie v Austrálii a na Novém Zélandě, které prokázaly účinnost carvedilolu u pacientů se srdečním selháním lehkého až středně těžkého stupně, byl lék v USA schválen pro léčbu pacientů se srdečním selháním [27].
Ne všechny léky ze skupiny betablokátorů jsou účinné v léčbě srdečního selhání. Studie BEST s bucindololem, což je neselektivní betablokátor s mírným vazodilatačním účinkem a ISA, naznačila, že tento lék nebyl pro srdeční selhání vhodný, hlavně pro afroamerickou populaci a nemocné s těžkou poruchu srdeční funkce NYHA III ‑ IV [28].
Další studie COPERNICUS, CIBIS II, MERIT_HF a SENIOR potvrdily naopak účinek carvedilolu, bisoprololu, metoprololu ZOK a nebivololu na snížení celkového i kardiovaskulárního rizika úmrtí u chronického srdečního selhání [6]. Zatímco předchozí práce se věnovaly efektu betablokátorů v léčbě lehkého až středně těžkého srdečního selhání, studie COPERNICUS s carvedilolem rozšířila pole působnosti i na léčbu těžkého srdečního selhání, přičemž i zde bylo dosaženo statisticky významného snížení mortality i morbidity. Vyloučeni byli z této studie jen nemocní vyžadující inotropní podporu a intenzivní péči.
V teoriích, který betablokátor je v léčbě srdečního selhání nejúčinnější, se mnoho očekávalo od srovnávací studie COMET, která porovnávala účinnost carvedilolu a neretardovaného metoprolol tartarátu u srdečního selhání a jejíž výsledek vyzněl lépe pro komplexnější carvedilol [29]. Bohužel v tomto případě je poněkud problematická interpretace výsledků pro volbu ve studii použité nižší dávky neretardované formy metoprolol tartarátu a ne v této indikaci výhodnější selektivní beta‑1 retardované formy metoprololu ZOK v plné doporučené dávce. Nicméně zbývá konstatovat, že jak neselektivní carvedilol s vazodilatačním účinkem, tak kardioselektivní metoprolol ZOK a stejně tak bisoprolol či nebivolol jsou léky vhodnými a účinnými při léčbě chronického srdečního selhání [30 – 32].
Léčba betablokátory, včetně carvedilolu, nemá žádný známý účinek na ovlivnění diastolické dysfunkce levé komory u pacientů se srdečním selháním. Nejsou také dostupná žádná data, která by doporučovala použití carvedilolu nebo jiného betablokátoru u asymptomatických pacientů s poruchou funkce levé komory, nicméně výsledky studií u pacientů po infarktu myokardu naznačují prospěšnost i u těchto pacientů [33 – 34].
Samotný mechanizmus, kterým betablokátory zpomalují progresi srdečního selhání, není dosud přesně vyjasněn. Mezi možnými se uvažuje up‑regulace beta‑adrenergních receptorů v srdci, modulace postreceptorových inhibičních proteinů G, účinek na remodelaci levé komory a zlepšení funkce baroreceptorů, které přirozeně mohou inhibovat zvýšenou sympatickou aktivitu [23,33]. Navíc betablokátory mohou snížit riziko apoptózy, procesu úzce souvisejícího s progresí srdečního selhání [35].
Klinické použití carvedilolu u srdečního selhání
Carvedilol je součástí komplexní léčby srdečního selhání. Dle výsledků výše uvedených studií zpomaluje klinickou progresi srdečního selhání, přidání carvedilolu ke konvenční léčbě srdečního selhání snižuje počet hospitalizací, mortalitu a potřebu zvyšování ostatní medikace u stabilizovaných pacientů s lehkou až závažnou formou tohoto onemocnění bez ohledu na jeho etiologii. Lék je dostupný v tabletách s obsahem 3,125; 6,25; 12,5 a 25 mg. Carvedilol je stejně účinný u pacientů afroamerické i kavkazské populace, účinnost nezávisí na věku nemocných [36]. Dávka pro léčbu srdečního selhání by měla být volena individuálně a léčba velmi pozorně kontrolována. Před nasazením carvedilolu se doporučuje dosáhnout ustálené dávky ACE inhibitoru či sartanu a diuretika, popřípadě digoxinu. Doporučená úvodní dávka carvedilolu je 3,125 mg dvakrát denně po dobu dvou týdnů. V případě dobré tolerance je možno dávku léku zvyšovat na dvojnásobek v minimálně dvoutýdenním intervalu až do maximální doporučené dávky 2 × 25 mg denně u pacientů do 85 kg, případně 2 × 50 mg u pacientů s vyšší hmotností. Před každým zvýšením dávky se doporučuje provést kontrolu klinického stavu – posoudit oběhovou kompenzaci, včetně krevního tlaku, zhodnotit vitální funkce a aktuální hmotnost pacienta, abychom vyloučili příznaky (většinou přechodné) zhoršení srdečního selhávání, popřípadě závratě navozené či zhoršené v důsledku vazodilatace. Nadměrnou retenci tekutin a zhoršování dušnosti lze řešit zvýšením dávky diuretika, současně je ovšem vhodné snížit přechodně dávku, není vhodné náhle přerušit podávání carvedilolu pro nebezpečí rebound fenoménu. Hypotenze a související vertiginózní obtíže lze často ovlivnit snížením dávky diuretika nebo ACE inhibitoru, ovšem pokud k vymizení potíží ani tímto zásahem nedojde, je pak nutno opět sáhnout ke snížení dávky carvedilolu. Dokud těmito opatřeními nedokážeme stav nemocného stabilizovat, nesmíme dávku zvyšovat. U části pacientů, u nichž nedochází ke zlepšování, ale ani ke zhoršování symptomů, se doporučuje v léčbě carvedilolem pokračovat především s ohledem na data prokazující prodloužení doby přežívání nemocných. V tomto případě je vhodný individuální přístup, zohlednění kvality života nemocných, a to i z důvodu udržení dobré compliance k léčbě [6,12].
Vedlejší účinky
Během trvání US Carvedilol Heart Failure Program byla léčba carvedilolem přerušena asi u 5 % pacientů, a to z důvodu zhoršení srdečního selhání, závratí nebo bradykardie [26]. Nejčastější nežádoucí reakcí v této i v ostatních studiích byl vznik otoků, závrať, bradykardie, hypotenze, nevolnost, průjem a rozmazané vidění [26]. Incidence nežádoucích reakcí nezávisela na věku pacientů. Vzácně byl carvedilol příčinou přechodného zhoršení ledvinných funkcí, obvykle při současné hypotenzi a většinou na podkladě již známé ledvinné nedostatečnosti. Pacienty s rizikem poškození ledvinných funkcí je vhodné pečlivě monitorovat. Výjimečně bylo zjištěno lehké zhoršení jaterních funkcí, ale nebylo dokumentováno žádné jaterní selhání v souvislosti s léčbou carvedilolem. Incidence abnormalit jaterních funkcí v klinických studiích s carvedilolem se udává kolem 1 % a je stejná jako u placeba.
Při předávkování carvedilolem může vzniknout těžká hypotenze, bradykardie, srdeční selhání, kardiogenní šok a srdeční zástava. Může dojít k bronchospazmu, zvracení, poruše vědomí a křečím. V tomto stavu je nutná monitorace a léčba na jednotce intenzivní péče pomocí inotropik [6,12].
Kontraindikace
Carvedilol je kontraindikován u těžkého dekompenzovaného srdečního selhání, zejména pak u nemocných vyžadujících inotropní podporu. Tito pacienti jsou závislí na sympatické stimulaci a netolerují blokádu beta‑adrenoreceptorů. Navíc i stav tělesných tekutin není v této fázi stabilizovaný a nežádoucí známky vazodilatace nebo zhoršení srdečního selhání se mohou projevit snáze. Použití carvedilolu je nevhodné u nemocných s významnou bradykardií, sick sinus syndromem a atrioventrikulární blokádou vyššího stupně. Carvedilol nemá u nedisponovaných jedinců žádný nežádoucí vliv na plicní funkce, nicméně podobně jako ostatní beta‑blokátory není doporučován u pacientů s těžkou obstrukcí dýchacích cest. U astmatiků je přísně kontraindikován. Také u diabetiků je třeba obezřetnosti, neboť léčba carvedilolem může maskovat příznaky hypoglykemie. Bezpečnost použití carvedilolu u těhotných nebo kojících žen a dětí se srdečním selháním nebyla předmětem žádné studie, tudíž není stanovena a nelze jej proto v těchto případech doporučovat [6,12].
Závěr
Carvedilol je antagonistou alfa ‑ i beta‑adrenoreceptorů, který prokázal svou terapeutickou hodnotu především jako součást komplexní léčby srdečního selhání v kombinaci s diuretiky a ACE inhibitory, popř. s digoxinem, a to u pacientů všech stupňů závažnosti srdečního selhání. Jak dokázaly studie i bohaté klinické zkušenosti, při léčbě carvedilolem dochází u nemocných k prokazatelnému zpomalení progrese srdečního selhání, což reflektuje snížení kombinovaného rizika kardiovaskulární morbidity (potřeba hospitalizace a navyšování další medikace srdečního selhání) a snížení počtu úmrtí z kardiovaskulární příčiny. Mimoto carvedilol má své uplatnění také v jiných indikacích u ischemické choroby srdeční a v léčbě hypertenze.
Práce byla vypracována v rámci Výzkumného záměru MŠMT ‑ MSM0021622402.
MUDr. Jiří Jež
prof. MUDr. Jiří Vítovec, CSc., FESC
I. interní kardioangiologická klinika LF MU
a FN u sv. Anny v Brně
jiri.jez@fnusa.cz
Zdroje
1. Bristow MR, Gilbert EM, Abraham WT et al. Carvedilol produces dose‑related improvements in left ventricular function and survival in subjects with chronic heart failure. Circulation 1996; 94 : 2807 – 2816.
2. Packer M, Colucci WS, Sackner ‑ Bernstein JD et al. Double‑blind, placebo ‑ controlled study of the effects of carvedilol in patients with moderate to severe heart failure. The PRECISE trial. Prospective Randomized Evaluation of Carvedilol on Symptoms and Exercise. Circulation 1996; 94 : 2793 – 2799.
3. Colucci WS, Packer M, Bristow MR et al. Carvedilol inhibits clinical progression in patients with mild symptoms of heart failure. US Carvedilol Heart Failure Study Group. Circulation 1996; 94 : 2800 – 2806.
4. Cohn JN, Fowler MB, Bristow MR et al. Safety and efficacy of carvedilol in severe heart failure. The U.S. Carvedilol Heart Failure Study Group. J Card Fail 1997; 3 : 173 – 179.
5. Australia/ New Zealand Heart Failure Research Collaborative Group. Randomised, placebo ‑ controlled trial of carvedilol in patients with congestive heart failure due to ischaemic heart disease. Lancet 1997; 349 : 375 – 380.
6. Vítovec J, Špinar J. Farmakoterapie kardiovaskulárních onemocnění. 2. vyd. Praha: Grada 2004.
7. Morgan T. Clinical pharmacokinetics and pharmacodynamics of carvedilol. Clin Pharmacokinet 1994; 26 : 335 – 346.
8. Dunn CJ, Lea AP, Wagstaff AJ. Carvedilol: a reappraisal of its pharmacological properties and therapeutic use in cardiovascular disorders. Drugs 1997; 54 : 161 – 185.
9. Louis WJ, McNeil JJ, Workman BS et al. A pharmacokinetic study of carvedilol (BM 14.190) in elderly subjects: preliminary report. J Cardiovasc Pharmacol 1987; 10: S89 – S93.
10. Neugebauer G, Akpan W, von Mollendorff E et al. Pharmacokinetics and disposition of carvedilol in humans. J Cardiovasc Pharmacol 1987; 10: S85 – S88.
11. Zhou HH, Wood AJ. Stereoselective disposition of carvedilol is determined by CYP2D6. Clin Pharmacol Ther 1995; 57 : 518 – 524.
12. Frishman WH. Carvedilol. N Eng J Med 1998; 339 : 1759 – 1765.
13. Hall S, Prescott RI, Hallman RJ et al. A comparative study of carvedilol, slow ‑ release nifedipine, and atenolol in the management of essential hypertension. J Cardiovasc Pharmacol 1991; 18: S35 – S38.
14. van der Does R, Eberhardt R, Derr I et al. Treatment of chronic stable angina with carvedilol in comparison with nifedipine s.r. Eur Heart J 1991; 12 : 60 – 64.
15. Freedman SB, Jamal SM, Harris PJ et al. Comparison of carvedilol and atenolol for angina pectoris. Am J Cardiol 1987; 60 : 499 – 502.
16. Basu S, Senior R, Raval U et al. Beneficial effects of intravenous and oral carvedilol treatment in acute myocardial infarction: a placebo ‑ controlled, randomized trial. Circulation 1997; 96 : 183 – 191.
17. The CAPRICORN Investigators. Effect of carvedilol on outcome after myocardial infarction in patients with left ‑ ventricular dysfunction: the CAPRICORN randomised trial. Lancet 2001; 357 : 1385 – 1390.
18. Frishman WH, Charlap S. Alpha ‑ and beta‑adrenergic blocking drugs. In: Frishman WH, Sonnenblick EH (eds). Cardiovascular pharmacotherapeutics. New York: McGraw ‑ Hill 1997 : 59 – 94.
19. Packer M, Lee WH, Kessler PD et al. Role of neurohormonal mechanisms in determining survival in patiens with severe chronic heart failure. Circulation 1987; 75: IV80 – IV92.
20. Sackner ‑ Bernstein JD, Mancini DM. Rationale for treatment of patiens with chronic heart failure with adrenergic blockade. JAMA 1995; 274 : 1462 – 7 (Erratum. JAMA 1996; 275 : 686).
21. Waagstein F, Hjalmarson A, Varnauskas E et al. Effect of chronic beta‑adrenergic receptor blockade in congestive cardiomyopathy. Br Heart J 1975; 37 : 1022 – 1036.
22. Viquerat CE, Daly P, Swedberg K et al. Endogenous catecholamine levels in chronic heart failure: relation to the severity of hemodynamic abnormalities. Am J Med 1985; 78 : 455 – 460.
23. Henderson EB, Kahn JK, Corbett JR et al. Abnormal I ‑ 123 metaiodobenzylguanidine myocardial washout and distribution may reflect myocardial adrenergic derangement in patients with congestive cardiomyopathy. Circulation 1988; 78 : 1192 – 1199.
24. Zimmer HG, Kolbeck ‑ Ruhmkoff C, Zierhut W. Cardiac hypertrophy induced by alpha ‑ and beta‑adrenergic receptor stimulation. Cardioscience 1995; 6 : 47 – 57.
25. Podrid PJ, Fuchs T, Candinas R. Role of the sympathetic nervous system in the genesis of ventricular arrhythmia. Circulation 1990; 82: I103 – I113.
26. Packer M, Bristow MR, Cohn JN et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. N Engl J Med 1996; 334 : 1349 – 1355.
27. Roden DM. Cardiovascular and Renal Advisory Panel of the US Food and Drug Administration considers four drugs. Circulation 1997; 95 : 2335.
28. BEST Trial Investigators. A trial of beta‑blocker bucindolol in patients with advanced chronic heart failure. N Engl J Med 2001; 344 : 1659 – 1667.
29. Poole ‑ Wilson PA, Swedberg K, Cleland JGF et al. Carvedilol Or Metoprolol European Trial Investigators. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure in the Carvedilol Or Metoprolol European Trial (COMET): randomised controlled trial. Lancet 2003; 362 : 7 – 13.
30. Wolert KC, Drexler H. Carvedilol Prospective Randomized Cumulative Survival (COPERNICUS) Trial: Carvedilol as the Sun and Center of the b ‑ Blocker World? Circulation 2002; 106 : 2164 – 2166.
31. Packer M, Coats AJ, Fowler MB et al. Effect of Carvedilol on Survival in Severe Chronic Heart Failure. N Engl J Med 2001; 344 : 1651 – 1658.
32. Vítovec J, Špinar J. Který betablokátor u srdečního selhání? Studie COMET – dala jasnou odpověď? Cor Vasa 2003; 45 : 527 – 528.
33. Hjalmarson A, Kneider M, Waagstein F. The role of beta‑blockers in left ventricular dysfunction and heart failure. Drugs 1997; 54 : 501 – 510.
34. The Beta‑Blocker Pooling Project Research Group. The Beta‑Blocker Pooling Project (BBPP): subgroup findings from randomized trials in post infarction patients. Eur Heart J 1988; 9 : 8 – 16.
35. Olivetti G, Abbi R, Quaini F et al. Apoptosis in the failing human heart. N Engl J Med 1997; 336 : 1131 – 1141.
36. Yancy C, Fowler MB, Colucci WS et al. Response of black heart failure patients to carvedilol. J Am Coll Cardiol 1997; 29 : 284A abstract.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2010 Číslo 1
-
Všechny články tohoto čísla
- Reziduální vaskulární riziko a celosvětová aktvita R3I (Residual Risk Reduction Initiative)
- Deprese u pacientů s kardiologickým onemocněním
- Studie CORD – analýza nemocných starších 80 let a nemocných s izolovanou systolickou hypertenzí
- Carvedilol v léčbě kardiovaskulárních onemocnění
- Ivabradin v léčbě ischemické choroby srdeční – výsledky klinické studie BEAUTIFUL
- Noví hráči na šachovnici protidestičkové léčby – co můžeme očekávat?
- Tenektepláza v současné klinické praxi
- Neléčíme příliš?
- Jsou rozdíly v účinku inhibitorů ACE klinicky významné? Co říkají výsledky studií ONTARIO
- Heart Failure 2009 – NICE
- Galerie autorů
- Možnosti léčebného ovlivnění tepenné tuhosti
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Carvedilol v léčbě kardiovaskulárních onemocnění
- Deprese u pacientů s kardiologickým onemocněním
- Tenektepláza v současné klinické praxi
- Jsou rozdíly v účinku inhibitorů ACE klinicky významné? Co říkají výsledky studií ONTARIO
