Co zaznělo v HOT lines na ČKS 2015
Autoři:
P. Janský 1; J. Vítovec 2; J. Špinar 3,4
Působiště autorů:
Klinika kardiovaskulární chirurgie 2. LF UK a FN v Motole, Praha
1; I. interní kardioangiologická klinika LF MU a FN u sv. Anny v Brně
2; Interní kardiologická klinika, LF MU a FN Brno
3; Mezinárodní centrum klinického výzkumu, FN u sv. Anny v Brně
4
Vyšlo v časopise:
Kardiol Rev Int Med 2015, 17(3): 262-268
Kategorie:
Kardiologická revue
Na kongresu České kardiologické společnosti v květnu 2015 v Brně byl jako tradičně jeden z nejlépe navštívených bloků blok pracovní skupiny Farmakoterapie o nejvýznamnějších klinických studiích prezentovaných v předchozím roce – blok HOT lines.
Studie PARADIGM-HF
Chronické srdeční selhání je nepochybně pandemií současné kardiologie. Přesto v posledních letech nedošlo k žádné zásadní změně v terapeutických postupech. V tomto smyslu jsou první výsledky studií s tzv. ARNI (angiotenzin‑receptor neprilysin inhibitory) velmi nadějné. Duální inhibice AT1 receptorů a neprilyzinu blokuje osu renin‑angiotenzin‑aldosteron (RAS) a zároveň podporuje přirozený vazodilatační a diuretický efekt natriuretických peptidů. Rozsáhlá prospektivní randomizovaná multicentrická studie PARADIGM-HF u více než 8 000 nemocných se stabilizovaným chronickým srdečním selháním se systolickou dysfunkcí levé komory (LK) (EF LK ≤ 40 %, posléze ≤ 35 %), většinou ve funkční třídě NYHA II – III a s elevací BNP/ NT ‑ proBNP prokázala 20% snížení primárního endpointu (úmrtí + hospitalizace pro dekompenzaci srdečního selhání) ve skupině léčené ARNI (lék LCZ696 firmy Novartis). Výsledky studie ukazuje tab. 1.

Z tabulky je patrné, že primární cíle vyzněly vysoce statisticky významně ve prospěch LCZ696, a to jak pro složený cíl kardiovaskulární (KV) úmrtí a první hospitalizace pro srdeční selhání (p < 0,001), tak pro oba jednotlivé podcíle, tedy jak pro KV mortalitu (p < 0,001), tak pro první hospitalizace pro srdeční selhání (p < 0,001). Statisticky významně byla nižší i celková mortalita (p < 0,001). Naopak pokles renálních funkcí a nový výskyt fibrilace síní byl v obou skupinách podobný. Léčba byla bezpečná, typickým nežádoucím účinkem byla hypotenze, která nicméně nevedla ke zvýšené nutnosti přerušení léčby. Možnost duální inhibice RAS a neprilyzinu se tak možná po dlouhé době stane první zásadnější změnou „paradigmatu“ v léčbě stabilizovaného chronického srdečního selhání se systolickou dysfunkcí LK.
ČR přispěla významným způsobem k úspěšnému uskutečnění studie Paradigm-HF a všem aktivním centrům patří velký dík a uznání za vysoce kvalitně odvedenou práci. Národní koordinátor studie Paradigm-HF v ČR byl doc. MU Dr. Jan Bělohlávek, Ph.D.
Studie SIGNIFY
Ivabradin je blokátor kanálů If v sinoatriálním uzlu, jehož takřka jediným farmakologickým účinkem je zpomalení srdeční frekvence při sinusovém rytmu. Na základě výsledků předcházejících klinických studií je v Evropě registrován a používán jednak pro léčbu stabilní anginy pectoris (AP), jednak pro léčbu chronického srdečního selhání se sníženou ejekční frakcí.
Z placebových větví dřívějších studií s ivabradinem víme, že nemocní s klidovou srdeční frekvencí (SF) ≥ 70/ min mají významně vyšší riziko KV příhod než nemocní s klidovou SF < 70/ min (HR = 1,46; p = 0,007). Klinická studie BEAUTIFUL pak prokázala, že u nemocných s chronickou ischemickou chorobou srdeční (ICHS) a systolickou dysfunkcí LK, kteří mají sinusový rytmus a klidovou SF ≥ 70/ min, snižuje ivabradin významně riziko fatálních i nefatálních infarktů myokardu (IM) (HR = 0,64; p < 0,001). Proto byla navržena klinická studie SIGNIFY, která měla otestovat hypotézu, že snížení SF ivabradinem sníží výskyt KV příhod i u nemocných s chronickou ICHS včetně stabilní AP, kteří nemají ani srdeční selhání ani systolickou dysfunkci levé LK (EF > 0,40) a přitom mají sinusový rytmus s klidovou SF ≥ 70/ min.
Do studie SIGNIFY bylo randomizováno 19 102 nemocných z 51 zemí po celém světě buď k přidání ivabradinu k dosavadní medikaci v denní dávce titrované podle tolerability až do 2 × 10 mg, nebo k přidání placeba. Průměrná doba sledování byla 28 měsíců a primárním sledovaným ukazatelem byl součet KV úmrtí a nefatálních IM. Protokol předem specifikoval i analýzu u podskupiny nemocných se stabilní AP stupně ≥ 2 podle CCS.
Výsledky: ivabradin ve srovnání s placebem snížil klidovou SF v průměru o 9,7/ min. Toto snížení SF však nevedlo ke snížení výskytu primárního sledovaného klinického ukazatele (HR = 1,08; p = 0,20) ani jeho jednotlivých složek – KV úmrtí (HR = 1,10; p = 0,25) a nefatálních IM (HR = 1,04; p = 0,60). U velké podskupiny nemocných se stabilní AP stupně ≥ 2 podle CCS (n = 12 049) ivabradin dokonce významně zvýšil výskyt primárního sledovaného klinického ukazatele (HR = 1,18; p = 0,018) rovnoměrným zvýšením výskytu obou jeho složek – KV úmrtí (HR = 1,16; p = 0,11) i nefatálních IM (HR = 1,18; p = 0,09). Ivabradin přitom významně snížil symptomy AP (< 0,01) a na hranici statistické významnosti snížil také nutnost elektivních koronárních revaskularizací (HR = 0,82; p = 0,058).
Interpretace těchto neočekávaných a překvapivých výsledků je obtížná. Jsou v příkrém rozporu s výsledky dřívějších klinických studií s ivabradinem, klinickou zkušeností i patofyziologickými mechanizmy. Jejich vysvětlení není jasné. Obviňuje se příliš vysoká denní dávka ivabradinu (až 2 × 10 mg), která často vedla k významné bradykardii – symptomatické u 7,9 % a asymptomatické u 11 % nemocných. Podílet se mohly i lékové interakce s bradykardizujícími blokátory kalciových kanálů diltiazemem a verapamilem. Výsledky studie SIGNIFY však podle Evropské lékové agentury (EMA) i podle našeho SÚKL nijak neovlivňují registrované indikace ivabradinu a jeho stávající doporučené dávkování (max. 2 × 7,5 mg).
Studie IMPROVE‑ IT
Studie začala před osmi lety a ČR byla od začátku studie jednou z velmi aktivních zemí (26 center, 371 zařazených nemocných = 6,7 %, doba trvání v ČR osm let, národní koordinátor prof. Špinar). Výsledky studie vyvolávaly napětí a mnozí řešitelé již přestávali věřit, že tak dlouho trvající studie přinese pozitivní výsledky a že se potvrdí teorie hladiny cholesterolu „čím níže, tím lépe“ a že přidání ezetimibu je účinné a bezpečné.
Studie sledovala 18 144 pacientů, kteří měli vysoké riziko koronárního syndromu ve 1 158 centrech v 39 zemích. Ezetimib selektivně inhibuje intestinální absorpci cholesterolu a příbuzných rostlinných sterolů v enterocytu (inhibicí specifického transportního systému – Niemann‑Pick C1‑like 1 proteinu – – NPC1L1), a snižuje tak přísun cholesterolu ze střev do jater. Vzhledem k rozdílnému mechanizmu účinku dochází při současném podávání se statiny k potenciaci hypolipidemického účinku. V kontrolovaných klinických studiích u pcientů s hypercholesterolemií ezetimib v monoterapii nebo v kombinaci se statinem významně snižoval hladinu celkového cholesterolu, LDL cholesterolu (LDL-c) apolipoproteinu B a triglyceridů a zvyšoval hladinu HDL cholesterolu.
Mezi základní vstupní kritéria patřila hospitalizace pro STEMI/ nonSTEMI < 10 dnů, věk > 50 let + alespoň jedno z následujících kritérií: nové ST změny, pozitivní troponin, diabetes mellitus, předchozí IM, cerebrovaskulární onemocnění, předchozí CABG, vícečetné postižení koronárních artérií a současně LDL‑c 1,3 – 3,2 mmol/ l (1,3–2,6 mmol/ l, pokud byla předchozí hypolipidemická léčba).
Mezi vylučovací kritéria patřilo CABG pro kvalifikující příhodu, užívaní statinu > 40 mg simvastatinu, kreatinová clearance < 30 ml/ l a aktivní onemocnění jater.
Nemocní byli randomizováni na léčbu 40 mg simvastatinu nebo na kombinaci 40 mg simvastatinu + 10 mg ezetimibu.
LDL-c poklesl o předpokládaných 20 %. Graf 1 ukazuje pokles jednotlivých součástí primárního cíle – KV úmrtí, nefatální IM, nefatální cévní mozková příhoda, hospitalizace pro nestabilní AP a revaskularizace po více než 30 dnech. Ezetimib v kombinaci se simvastatinem ve srovnání se simvastatinem samotným snížil KV riziko primárního cíle o 6,4 % u nemocných po akutním koronárním syndromu. Samotné srdeční příhody byly sníženy o 13 % a cévní mozkové příhody (CMP) o 20 %. Úmrtí z KV příčiny se nelišilo v obou skupinách. Průměrná doba sledování byla šest let, nejdelší doba sledování 8,5 let. Průměrně dva pacienti ze 100 byli kombinovanou léčbou ochráněni před KV příhodou za sedm let. (Number Needed to Treat (NNT) = 50).

Co se týká bezpečnosti a nežádoucích účinků, nebyl pozorován žádný specifický nežádoucí účinek po přidání ezetimibu k simvastatinu. Jaterní testy se nezměnily, rabdomyolýza v 0,2 % po simvastatinu a v 0,1 % po kombinaci, myopatie v 0,1 po simvastatinu a 0,2 % po kombinaci a jakákoli forma malignity v 10,2 % v obou skupinách.
Během studie byly získány další informace o výhodnosti vyšších dávek simvastatinu, proto bylo v roce 2011 na doporučení FDA (Food and Drug Administration) speciálním dodatkem (ammendment 4) povoleno zvýšit dávku simvastatinu na 80 mg, pokud nebylo dosaženo cílových hodnot LDL-c, což bylo provedeno u 27 % nemocných léčených monoterapií simvastatinem a pouze u šesti nemocných léčených kombinací simvastatin ++ ezetimib.
Studii na studijní medikaci dokončilo 58 % nemocných, což je vzhledem k délce studie přiměřené. Důvody přerušení léčby nebyly doposud prezentovány. V podskupinách se jasně ukázalo, že největší efekt můžeme očekávat u diabetiků.
Studie IMPROVE-IT plně potvrdila hypotézu o významu snižování LDL-c co nejníže, a tím snížení výskytu KV příhod. Výsledky této studie by měly být co nejdříve zaneseny do budoucích guidelines léčby a prevence KV onemocnění.
Studie EXAMINE
Diabetes mellitus 2. typu (DM2) je nejčastější formou cukrovky v ČR. Souvisí spíše s vyšším věkem, obezitou, nedostatkem pohybu a nezdravým životním stylem. Tělo nemocného inzulin sice vytváří, ale neumí jej efektivně využít. DM2 má pozvolné projevy a často je diagnostikován při preventivním vyšetření hladiny krevní glukózy. DM2 je závažné chronické onemocnění, jehož výskyt ve vyspělých zemích neustále narůstá. V ČR nyní trpí diabetem přibližně 8 % obyvatel, přičemž cca 90 % tvoří právě diabetici 2. typu. Na rozdíl od DM 1. typu je maximum výskytu DM2 u věkové skupiny nad 45 let, ale dnes se vyskytuje již i u dětí a dospívajících.
DM je chronická, zatím nevyléčitelná nemoc, jejímž hlavním příznakem je hyperglykemie. Čím vyšší je glykemie a čím delší dobu hyperglykemie působí na organizmus, tím vyšší je riziko výskytu pozdních komplikací. Jejich společným jmenovatelem je zejména poškození cév (odtud komplikace mikrovaskulární a makrovaskulární). Obecným cílem léčby diabetu je snížení morbidity a mortality pacientů. Cestou k dosažení tohoto cíle je účinná komplexní nefarmakologická i farmakologická intervence hyperglykemie, hypertenze a dyslipidemie (hyperlipidemie), ale i hypoglykemie.
Zlepšení možností terapie (nová léčiva a zejména selfmonitoring) ještě více akcentuje diabetologii jako obor zejména ambulantní. Až na speciální problematiku komplikací a recentní záchyt diabetu s těžkou dekompenzací lze v současnosti řešit naprostou většinu problémů bez nutnosti hospitalizace. Pro tento přístup je však nutno vytvořit předpoklady, z nichž nejdůležitější je dostatek času lékaře, případně celého týmu k řešení složitějších případů.
Léčba diabetu je velmi náročná a komplikovaná, je vždy doživotní a vyžaduje značnou spolupráci pacienta. Co nejlepší kontrola a udržování hladiny glykemie v normálním rozmezí je však určující pro vznik a rozvoj chronických komplikací neboli čím lépe je diabetes léčen a glykemie udržována v optimálním rozmezí, tím později k těmto komplikacím dochází.
Léčba DM2 je v současnosti účinná, ale bohužel ještě není ideální. Jistému ideálu se již blíží terapie založená na inkretinech, která je významným kvalitativním pokrokem.
Alogliptin je nový, účinný a vysoce selektivní inhibitor DPP-4, který je vhodný do monoterapie i do kombinační léčby. Výbor pro humánní léčivé přípravky Evropské lékové agentury (EMA) doporučil ke schválení léčivo alogliptin (Vipidia®) v kombinaci s metforminem (Vipdomet®) a pioglitazonem (Incresync®) pro léčbu pacientůs DM2.
Studie EXAMINE (Alogliptin after Acute Coronary Syndrome in Patiens with Type 2 Diabetes) byla prezentována na ESC 2013 a publikována v prestižním časopise New England Journal of Medicine. Jednalo se o multicentrickou, randomizovanou, mezinárodní, dvojitě slepou studii. Vstupními kritérii byly:
- DM2 na zavedené léčbě (monoterapie i kombinovaná terapie),
- akutní koronární syndrom prodělaný v rozmezí uplynulých 15 – 90 dnů,
- standardní způsob léčby DM2 a sekundární prevence po akutním koronárním syndromu (s výjimkou DPP-4 inhibitorů a GLP agonistů).
Pacienti byli randomizováni do skupiny užívající buď alogliptin, nebo placebo, kdy dávka alogliptinu (placeba) byla upravována podle renálních funkcí. Primární cíl byl složený a zahrnoval KV úmrtí, nefatální IM a nefatální CMP. Mezi bezpečností cíle patřil výskyt angioedému, hypoglykemie, zánětu slinivky břišní, změn funkce ledvin či změn na EKG. Randomizováno bylo 2 701 nemocných na alogliptin a 2 679 na placebo, léčbu předčasně ukončilo 564 (20,9 %) nemocných v aktivní léčbě a 606 (22,6 %) na placebu. Hlavní příčinou předčasného ukončení terapie byly nežádoucí účinky, včetně úmrtí, které se vyskytly v 10,0 % u nemocných na aktivní léčbě a v 10,3 % u nemocných na placebu.
Výskyt primárního cíle lze vidět v grafu 2.Výskyt nežádoucích účinků ukazuje tab. 2.

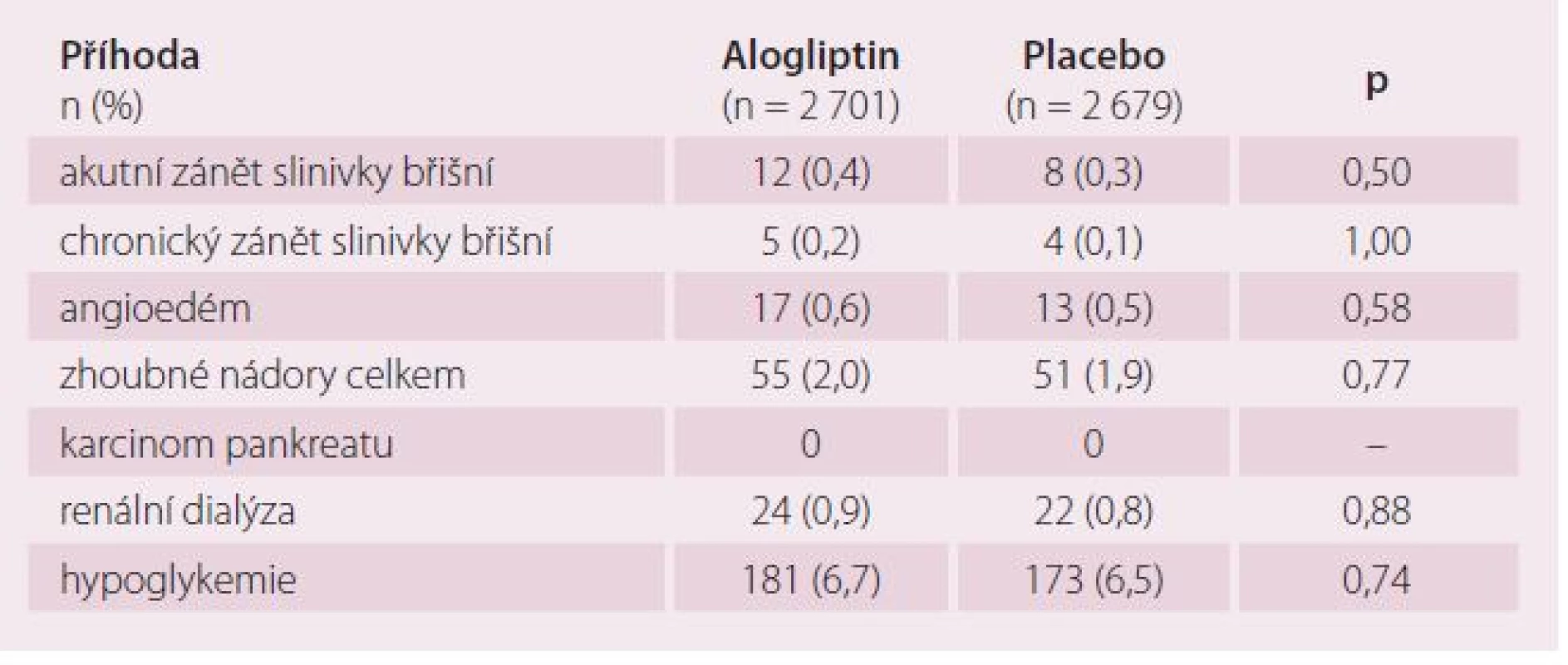
Na závěr tedy můžeme shrnout, že při srovnání alogliptinu s placebem u nemocných s DM2 a čerstvě prodělaným akutním koronárním syndromem byl srovnatelný výskyt KV příhod za současného významného snížení glykovaného hemoglobinu, což svědčí pro lepší kontrolu DM. Nebyl pozorován vyšší výskyt nežádoucích účinků, včetně hypoglykemií a onemocnění slinivky břišní. Studie EXAMINE prokázala KV bezpečnost alogliptinu a nenaznačila žádné jiné možné nežádoucí účinky.
Studie PEGASUS TIMI 54
Inhibitory receptorů P2Y12 máme dvojího typu: nepřímo působící, tj. vyžadující bioaktivaci – thienopyridiny (klopidogrel, tiklopidin a prasugrel), a přímé – většinou typu analog ATP (ticagrelor, cangrelor či elinogrel). Prvá skupina má výhodu ireverzibilní vazby na receptor a protidestičkovým účinkem po celou dobu cirkulace trombocytu, daní však je nutnost bioaktivace a pomalejší nástup účinku. Naopak předností přímých inhibitorů receptorů P2Y12 je rychlejší nástup účinku, krátká doba působení však vyžaduje přesnější spolupráci, při krvácení může být odeznění efektu přínosem. Ticagrelor je perorálně účinné protidestičkové léčivo; chemickou strukturou patří mezi cyklopentyl ‑ triazolo ‑ pyrimidiny (CPTP) (není tedy thienopyridin!). Přidání ticagreloru vedlo ke snížení trombotických příhod do jednoho roku po akutním IM např. ve studii PLATO.
Studie PEGASUS TIMI 54 testovala hypotézu, že přidání tikagreloru k malé dávce kyseliny acetylsalicylové sníží výskyt KV příhod u stabilních pacientů více než rok po IM. Testovány byly dvě dávky, a to 2 × 60 mg a 2 × 90 mg. Jednalo se o dvojitě slepou, randomizovanou mezinárodní studii prováděnou v 1 161 centrech v 31 zemích, včetně ČR. Zařazeni mohli být nemocní 1 – 3 roky po IM s dalším vysokým rizikem jako věk na 65 let, DM na medikaci, předchozí IM, vícečetné postižení na koronarografii či kreatinová clearance pod 60 ml/ min. Doprovodnou mediací byla kyselina acetylsalicylová v dávce 75 – 150 mg.
Primární cíl byl kombinace KV úmrtí, IM a CMP. Randomizováno bylo 21 162 nemocných v době od října 2010 do března 2013. Základní charakteristiku nemocných ukazuje tab. 3.
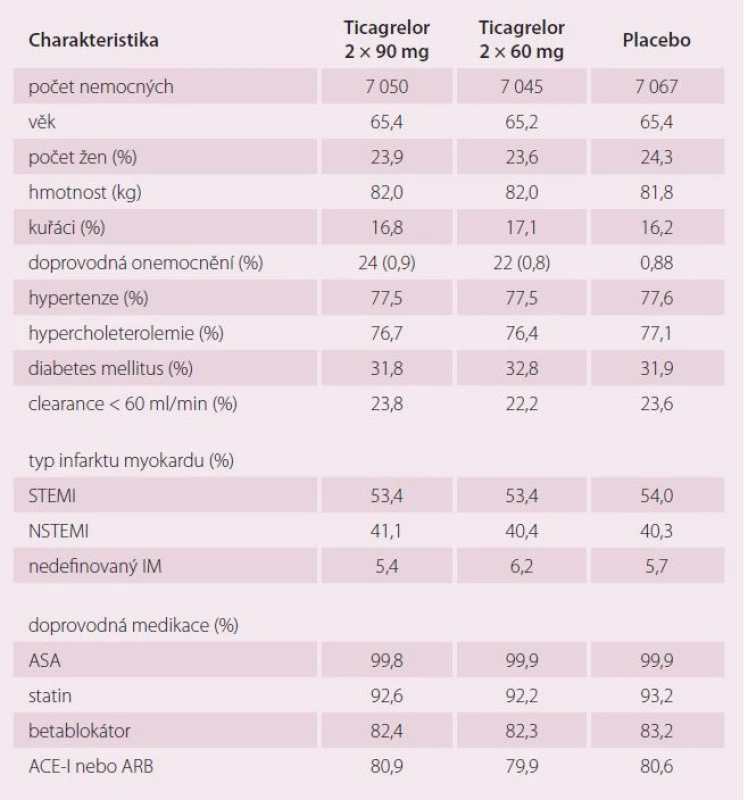
Průměrná doba od posledního IM byl 1,7 let, ST elevace infarkty tvořily nadpoloviční většinu. Většina pacientů (83 %) byla léčena primární angioplastikou, u 59 % bylo postižení více tepen. Tab. 3 ukazuje velmi kvalitní farmakologickou léčbu splňující současná doporučení.
Alespoň jednu dávku studijního léku dostalo 20 942 nemocných (99,0 %), během studie ukončilo léčbu 32,0 % na 2 × 90 mg, 28,7 % na 2 × 60 mg a 21,4 % na placebu (p < 0,001 pro obě dávky vs. placebo).
Obě dávky tikagreloru statisticky významně snížily primární cíl – KV úmrtí, IM a ICHS (graf 3). Účinek ticagreloru byl konzistentní na každý z primárních podcílů, kdy na obou dávkách byl výskyt primárního cíle 7,81 %, výskyt KV úmrtí 2,90 % vs. 3,39 % na placebu (p = 0,57), IM 4,47 % vs. 5,25 % (p = 0,0055) a výskyt CMP 1,54 % vs. 1,94 % (p = 0,034). Nebyl pozorován žádný rozdíl podle věku, pohlaví, typu IM či dávce kyseliny acetylsalicylové.

Primární bezpečnostní cíl – TIMI velké krvácení byl vyšší na obou dávkách ticagreloru s výskytem po třech letech 2,60 % na 2 × 90 mg, 2,30 % na 2 × 60 mg a 1,06 % na placebu (p < 0,001 pro obě dávky vs. placebo). TIMI malé krvácení bylo podobné na obou dávkách i na placebu. Výskyt smrtelného krvácení byl pod 1 % a nelišil se mezi skupinami. Dušnost byla častější na obou dávkách a pro dušnost byla významně častěji léčba ukončena na obou dávkách.
Výsledky studie PEGASUS TIMI 54 přinášejí jasný průkaz prospěchu z dlouhodobého podávání ticagreloru u pacientů s předchozím akutním koronárním syndromem, a to na KV mortalitu. Podobné výsledky přinesla i studie DAPT (viz níže).
Studie PEGASUS pravděpodobně přepíše doporučení pro antiagregační terapii po IM. Do budoucna můžeme očekávat především diskuzi, jak s duální antiagregací po roce od IM. Velká diskuze bude pravděpodobně vedena i o doporučené dávce ticagreloru, protože dávka 2 × 60 mg se ukázala minimálně rovnocenná (ne‑li lepší) dávce 2 × 90 mg.
Studie DAPT
Studie DAPT (Dual Antiplatelet Therapy) randomizovala téměř 10 000 nemocných po implantaci koronárního stentu. Základní otázka, kterou studie řešila, bylo srovnání výsledků následné 12 - či 30měsíční léčby duální antiagregací. Ta se skládala buď z kombinace kyseliny acetylsalicylové a klopidogrelu, nebo z kombinace kyseliny acetylsalicylové a prasugrelu. Studie zahrnovala jak pacienty se stabilní formou ischemické choroby srdeční, tak s akutním koronárním syndromem (30,7 %). Zároveň byli vyloučeni jak pacienti s vysokým rizikem ischemických, tak krvácivých komplikací.
Výsledky studie prokázaly snížení ischemických cílových ukazatelů (trombóza stentu o 1 %, IM o 2 %) ve větvi dlouhodobé léčby za cenu zvýšeného rizika nefatálního krvácení (o 0,7 %). Velmi zjednodušeně lze tedy shrnout, že prodloužení duální protidestičkové léčby za hranici 12 měsíců má význam hlavně v rámci sekundární prevence ischemické choroby srdeční, zatímco studie s podáváním duální protidestičkové léčby 12 měsíců a kratším (např. ISAR ‑ SAFE, ITALIC) se zaměřují primárně na prevenci trombózy stentu.
Výzkumné programy s PCSK9
Přibližně před deseti lety byl objeven nový protein označený proprotein‑subtilisin kexin konvertáza 9 (PCSK9) významně ovlivňující hladiny sérového LDL-c. Ve velmi krátké době výzkum vyústil v přípravu specifických monoklonálních protilátek blokujících tento protein. V důsledku toho se zvyšuje počet recirkulujících LDL receptorů na povrchu hepatocytu a to vede k poklesu LDL-c (i dalších aterogenních lipidů) v séru o 50 – 70 % nad rámec dosažitelný ostatními dostupnými terapiemi. Bezpečnost a účinnost inhibitorů PCSK9 je testována v rozsáhlém výzkumném programu několika výrobců. Tato nová terapeutická možnost představuje naději pro obtížně léčitelné nemocné s familiární hypercholesterolemií nebo intolerancí statinů a do budoucna možná i pro další pacienty s velmi vysokým a vysokým KV rizikem nedosahujícím cílových hodnot LDL-c běžnými postupy.
Klinické testování monoklonálních protilátek blokujících PCSK9 probíhá nezvykle rychle a rozsáhle. Už dnes můžeme říci, že jde o největší výzkumný farmaceutický program v současné kardiologii. Tři nejpokročilejší zástupci PCSK9 inhibitorů – alirokumab (Sanofi/ Regeneron), evolokumab (Amgen) a bokocizumab (Pfizer) procházejí zkoušením v rozsáhlých výzkumných programech. Alirokumab testují klinické studie programu ODYSSEY, evolokumab prochází zkoušením v programu PROFICIO, třetí nejpokročilejší zástupce v klinických testech, bokocizumab, je testován ve výzkumném programu s akronymem SPIRE.
Alirokumab je podáván subkutánně jedenkrát za dva nebo čtyři týdny v základní dávce 150 mg. U pacientů s familiární hypercholesterolemií snižuje koncentraci LDL-c o 36 – 58 % v monoterapii nebo v kombinaci se statinem. Obdobné výsledky dokumentovali autoři nedávno prezentované studie ODYSSEY long term, která sledovala více než 2 000 nemocných ve vysokém riziku KV komplikací s nedostatečně kontrolovanou hladinou LDL‑c. Výsledky studie sledující vliv alirokumabu na výskyt KV příhod (ODYSSEY Outcomes) očekáváme v roce 2018.
Podobně jako alirokumab prokázal i evolokumab se základní dávkou 420 mg v ukončených studiích (např. RUTHEFORD, LAPLACE) významné snížení hladin sérových lipidů včetně jinak obtížně ovlivnitelného aterogenního lipoproteinu (a) (pokles o 20 – 30 %). Mechanizmus posledního popsaného efektu není zřejmý, ale jistě se podílí na výsledném příznivém ovlivnění rizika aterosklerotických komplikací. Jakkoli jsou výsledky ukončených projektů slibné, musíme vyčkat, až evolokumab získá důkazy ze studie FOURIER, která testováním více než 22 000 pacientů po dobu pěti let snad jednoznačně potvrdí místo této nové léčby v prevenci a léčbě aterotrombotických cévních příhod.
Bokocizumab je testován v hodnoceních programu SPIRE. Také v rámci této série klinických studií nás bude nejvíce zajímat výsledek projektů SPIRE 1 a 2 s více než 18 000 pacienty, v nichž primárním sledovaným cílem jsou KV mortalita a výskyt KV příhody. Výsledky těchto prací s bokucizumabem můžeme očekávat v roce 2017.
Nadějný obrázek účinku použití PCSK9 inhibitorů na výskyt aterotrombotických cévních příhod ukazují post hoc analýzy některých programů. Použití alirokumabu v 78 týdnů trvající studii ODYSSEY long term vedlo ke snížení rizika výskytu kombinovaného sledovaného cílového ukazatele (fatální a nefatální IM nebo CMP, nestabilní AP vyžadující hospitalizaci) o 48 %. Analogicky evolocumab snížil riziko KV příhody během ročního sledování kohorty nemocných zařazených do studií OSLER 1 a 2 o 53 % ve srovnání s placebem podávaným k maximální možné současné terapii.
Registr GLORIA-AF
Registr GLORIA ‑ AF, jehož výsledky byly prezentovány na sjezdu ESC v Barceloně 2014, je zaměřen na standardní neselektovanou populaci pacientů s nově vzniklou fibrilací síní s rizikem tromboembolických komplikací a jeho výsledkem má být posouzení vlivu různých schémat antitrombotické terapie na prevenci CMP.
Cílem tohoto observačního registru je kolekce dat nejméně 56 000 pacientů s nově diagnostikovanou fibrilací síní, a to postupně ve třech fázích v celkem více než 2 200 centrech, která se zabývají léčbou fibrilace síní. Jedná se o konsekutivní pacienty s nevalvulární fibrilací síní FS s CHA2DS2-VACc skóre ≥ 1 s jasnou indikací antikoagulační terapie dle aktuálních doporučení ESC. Design registru je uveden na obr 1.
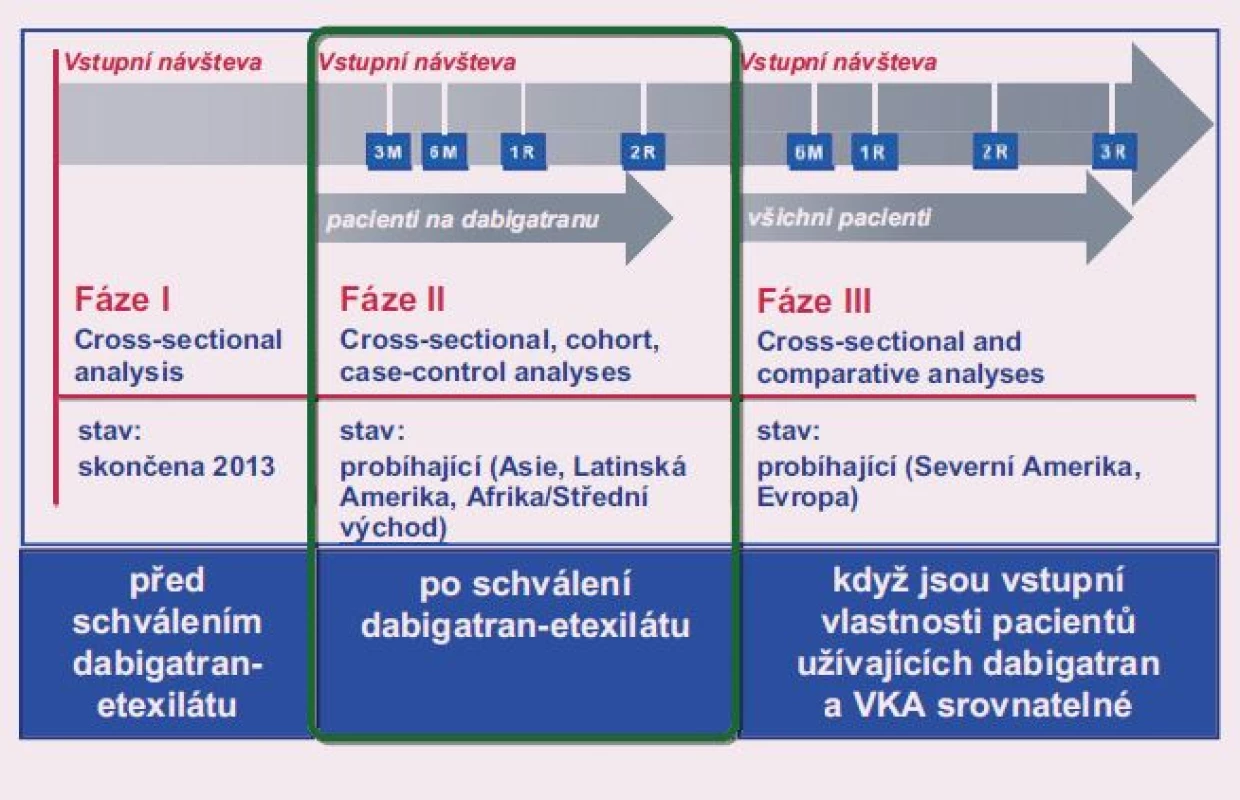
Fáze II, která probíhala od listopadu 2011 do ledna 2014, zahrnula 10 675 pacientů – nejvíce v Evropě a Severní Americe, dále v regionech Asie, Latinské Ameriky a Afriky.
Analýza antitrombotické terapie při vstupu do registru je uvedena v grafu 4 a vyjadřuje výraznou diferenci mezi regiony, samozřejmě s přihlédnutím k poměrně malým počtům zařazených pacientů v Africe a Latinské Americe.

Závěrem lze konstatovat, že antagonisté vitaminu K se nadále široce využívají v každodenní klinické praxi, a to i přes rostoucí používání nových perorálních antikoagulancií (NOAC).
V některých oblastech, např. Severní Americe a v zemích EU, roste výrazně používání NOAC a jejich preference před VKA (warfarin).
Nicméně v kontrastu k výše uvedeným datům zůstává vysoký podíl neléčených nebo špatně léčených pacientů (pouze ASA – aspirin) v Asii, ale také v některých regionech Severní Ameriky.
prof. MU Dr. Jindřich Špinar, CSc., FESC
www.fnbrno.cz
jspinar@fnbrno.cz
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2015 Číslo 3
-
Všechny články tohoto čísla
- Bezdrátová kardiostimulace – budoucnost nebo fikce?
- Novinka v intervenční terapii srdečního selhání se zachovalou ejekční frakcí levé komory
- Novinky v koronárních intervencích
- Mnohočetné postižení věnčitých tepen diagnostikované při pPCI pro STEMI: kompletní revaskularizace nebo konzervativní léčba. Studie Prague‑ 13.
- Erratum - Přímé versus nepřímé metody stanovení intenzity zatížení v kardiovaskulární rehabilitaci
- Farmakologická a nefarmakologická léčba fibrilace síní – současný pohled
- Léčebné postupy u námahové anginy pectoris
- Srdeční zástava a poresuscitační péče
- Komentovaná zkrácená verze evropských doporučení pro diagnostiku a management akutní plicní embolie z roku 2014
- Co přinesla nová evropská guidelines pro trvalou kardiostimulaci a srdeční resynchronizační léčbu (2013) v oblasti diagnostiky arytmií pomocí dlouhodobého monitorování EKG – současné technické aspekty a typy dlouhodobého monitorování EKG
- Fixní trojkombinace antihypertenziv a subklinické orgánové poškození – kazuistika
- Studie IMPROVE‑ IT u pacientů s diabetes mellitus
- Studie TECOS – efekt sitagliptinu na kardiovaskulární příhody u diabetes mellitus 2. typu
- Co zaznělo v HOT lines na ČKS 2015
- Co zaznělo na ESC 2015
- 500 transplantací srdce v Brně
- 25th European Meeting on Hypertension and Cardiovascular Protection, Milan 2015
- Zemřel prof. MUDr. Miloš Štejfa, DrSc., FESC28. 5. 1929– 20. 5. 2015
- Vzpomínka na prof. Miloše Štejfu
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Srdeční zástava a poresuscitační péče
- Léčebné postupy u námahové anginy pectoris
- Bezdrátová kardiostimulace – budoucnost nebo fikce?
- Novinka v intervenční terapii srdečního selhání se zachovalou ejekční frakcí levé komory
