Dapagliflozin a studie DECLARE – vstupní charakteristika
Dapagliflozin and the DECLARE study – input characteristic
Gliflozins – SGLT2 – mean a new approach to the treatment of type 2 diabetes mellitus. The mechanism of action is the excretion of excess sugar via the kidneys. In 2015, the first mortality study with SGLT2 empagliflozin – EMPA-REG OUTCOME was completed, in 2017 the CANVAS programme with canagliflozin were published and further studies are ongoing. An extensive programme has been launched with dapagliflozin, where meta-analyses of smaller studies have shown very positive results in reducing cardiovascular events. A large international clinical trial with dapagliflozin has been going on under the name DECLARE, scheduled to be completed in the summer of 2018. At the beginning of 2018, the initial characteristics of the patients enrolled in this study were published. The study included 17,160 patients with type 2 diabetes mellitus who were randomized to placebo or dapagliflozin at 10 mg/day. The mean age of the patients was 63.8 ± 6.8 years, mean duration of diabetes 11.8 ± 7.8 years, mean glycated haemoglobin 8.3% ± 1.2%. A total of 6,971 (40.6%) patients had confirmed cardiovascular disease and 10,189 (59.4%) had multiple risk factors.
Key words:
gliflozines – dapagliflozin – DECLARE – input characteristic
Autoři:
J. Špinar
Působiště autorů:
Interní kardiologická klinika LF MU a FN Brno
Vyšlo v časopise:
Kardiol Rev Int Med 2018, 20(1): 61-65
Souhrn
Glifloziny SGLT2 – znamenají nový přístup k léčbě diabetes mellitus 2. typu. Mechanizmem účinku je vylučování nadbytečného cukru ledvinami. V roce 2015 byla ukončena první mortalitní studie s SGLT2 empagliflozinem – EMPA-REG OUTCOME, v roce 2017 byl publikován program CANVAS s canagliflozinem a další studie probíhají. Rozsáhlý program má právě dapagliflozin, kdy metaanalýzy menších studií ukázaly velmi pozitivní výsledky na snížení kardiovaskulárních příhod. V současnosti probíhá velká mezinárodní klinická studie s dapagliflozinem pod názvem DECLARE, jejíž plánované ukončení je na léto 2018. Na začátku roku 2018 byla publikována vstupní charakteristika nemocných v této studii. Studie zařadila 17 160 nemocných s diabetes mellitus 2. typu, kteří byli randomizováni na léčbu placebem nebo dapagliflozinem v dávce 10 mg/ den. Průměrný věk nemocných byl 63,8 ± 6,8 let, průměrná doba trvání diabetu 11,8 ± 7,8 let, průměrný glykovaný hemoglobin 8,3 ± 1,2 %. Celkem 6 971 (40,6 %) nemocných mělo potvrzeno kardiovaskulární onemocnění a 10 189 (59,4 %) mělo vícečetné rizikové faktory.
Klíčová slova:
glifloziny – dapagliflozin – DECLARE – vstupní charakteristika
Úvod
Glifloziny (SGLT2 inhibitory) přinesly do léčby diabetes mellitus (DM) převratný mechanizmus účinku, dlouho se totiž vůbec nevěřilo, že by bylo možné snižovat hladinu cukru v krvi cestou vylučování cukru močí. SGLT2 inhibitory neboli glifloziny mají za sebou zajímavou historii. V roce 1835 Petersen izoloval florizin z kůry jabloně, který byl používán především jako antimalarikum. Co se týče diabetu, naopak převládalo mínění, že by mohly glifloziny DM způsobovat, protože se v moči nemocných nalézal cukr, což mělo být známkou hyperglykemie.
Glifloziny jsou molekuly, které umí zablokovat účinek klíčového SGLT2. Praktickým důsledkem je vyloučení až 70 g glukózy močí za den, což představuje množství energie získané přibližně jedním hlavním jídlem [1]. Při léčbě se pak kromě glykemie snižuje i hmotnost pacienta a mnohdy i krevní tlak (TK).
Nežádoucí účinky gliflozinů jsou předmětem diskuzí a velkých klinických studií. Jde především o riziko močových a urogenitálních infekcí. Z dalších pozorovaných vedlejších účinků je prozatím nejasný vztah k amputacím dolních končetin.
Studie EMPA-REG OUTCOME byla prezentována na podzim 2015 a okamžitě vyvolala nadšení, ale i řadu diskuzí [2,3]. Dlouhodobé multicentrické randomizované dvojitě zaslepené placebem kontrolované studie se zúčastnilo více než 7 000 pacientů s DM 2. typu (DM2) s vysokým kardiovaskulárním (KV) rizikem. Medián doby sledování činil 3,1 roku. Empagliflozin v kombinaci se standardní terapií snížil výskyt úmrtí v důsledku KV onemocnění a výskyt nefatálního infarktu myokardu (IM) nebo nefatální cévní mozkové příhody (CMP) o 14 %. Během terapie došlo ke snížení mortality na KV choroby o 38 %. Užívání empagliflozinu také vedlo ke snížení celkové mortality o 32 % a k redukci hospitalizací pro srdeční selhání (SS) o 35 %. Celkový bezpečnostní profil léku byl v souladu s předchozími studiemi.
V roce 2017 byly publikovány výsledky programu CANVAS s canagliflozinem, který zahrnul 10 142 nemocných s DM a vysokým KV rizikem [4]. Primární cíl (úmrtí z KV příčin, nefatální IM a nefatální CMP) byl na placebu 31,5 a na aktivní léčbě 26,9 na 1 000 pacientských let (p < 0,001 pro noninferioritu; p = 0,02 pro superioritu). Canagliflozin zvýšil riziko amputací dolních končetin 6,3 vs. 3,4 na 1 000 pacientských let.
Na začátku roku 2018 byla publikována vstupní charakteristika nemocných zařazených do studie DECLARE (Dapagliflozin effect on cardiovascular events – DECLARE-TIMI 58) s dapagliflozinem oproti placebu u nemocných s prokázaným KV onemocněním a/ nebo vysokým KV rizikem (obr. 1) [5].
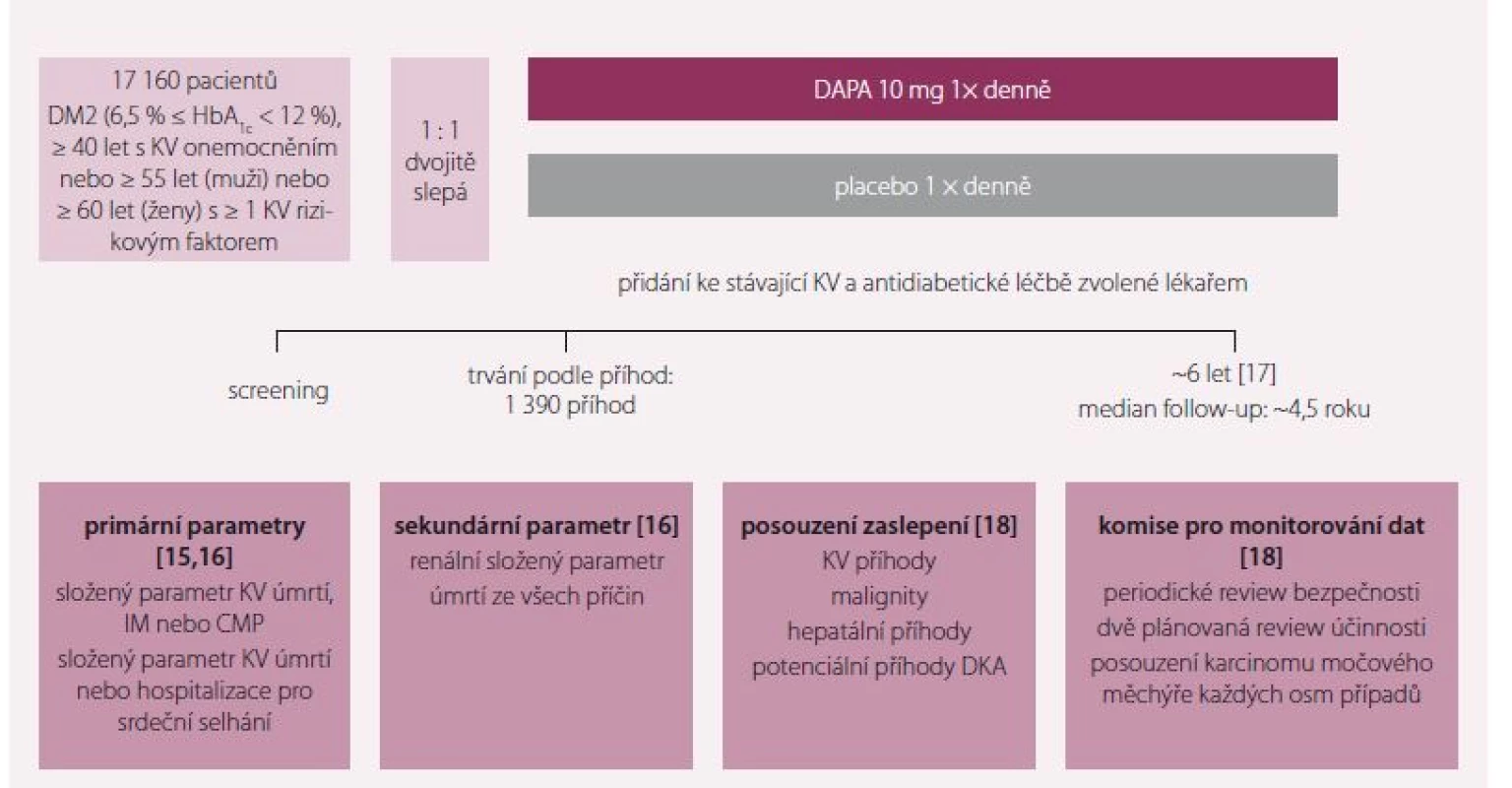
Základní charakteristika nemocných ve studii DECLARE
Studie zařadila 17 160 nemocných s DM2, kteří byli randomizováni na léčbu placebem nebo dapagliflozinem v dávce 10 mg/ den. Průměrný věk nemocných byl 63,8 ± 6,8 let, průměrná doba trvání diabetu 11,8 ± 7,8 let, průměrný glykovaný hemoglobin 8,3 ± 1,2 %. Celkem 6 971 (40,6 %) nemocných mělo potvrzené KV onemocnění (tzv. CVD skupina – cardiovascular disease group) a 10 189 (59,4 %) mělo vícečetné rizikové faktory (tzv. MRF skupina – multiple risc factor group) (tab. 1). Pacienti s KV onemocněním byli častěji muži (72,1 vs. 56,1 %) a měli podobnou délku trvání DM (12,0 vs. 11,7 let).
![DECLARE-TIMI 58 – základní charakteristiky. Upraveno dle [5,15,16].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/ac1f8670e9ba6a03a33749be025c196c.jpg)
Ve skupině s KV onemocněním byl častěji podáván metformin a sulfonylurea než ve skupině s rizikovými faktory, byl zde také častěji podáván inzulin (44,2 vs. 36,4 %) (obr. 2). Často byla podávána antihypertenziva, vysoké bylo především podávání betablokátorů v CVD skupině oproti MRF skupině (66,6 vs. 32,3 %). V CVD skupině bylo taktéž více antiagregační a antikoagulační terapie (aspirin 71,1 vs. 39,1 %, clopidogrel 24,7 vs. 1,5 %, warfarin 6,1 vs. 3,5 %).
![DECLARE-TIMI 58 – léčba při zařazení do studie. Upraveno dle [5,15,16].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/770bc2373aea19cd7299ec72b2489f5f.jpg)
Předchozí IM, angioplastika nebo bypass byl hlášen u 20,9; 21,3 a 9,8 % z celé populace a u skupiny CVD u 51,4; 52,4 a 24,1% (tab. 2). Překvapivě minimální rozdíly byly v TK a hodnotách lipidů mezi oběma skupinami (tab. 3). Creatinová clearance (CrCl < 60 ml/ min podle Cocrofta Goulta) byla vylučovacím kritériem, průměrná rychlost glomerulární filtrace (eGFR) podle MDRD kalkulace byla 86,1 + 21,8 ml/ min/ 1,73 m2.
![DECLARE-TIMI 58 – kardiovaskulární onemocnění. Upraveno dle [5,15,16].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/50bfb0c05f1f6b203e2da4ee9b9950fd.jpg)
![DECLARE-TIMI 58 – laboratorní hodnoty. Upraveno dle [5,15,16].](https://www.kardiologickarevue.cz/media/cache/resolve/media_object_image_small/media/image/7c30b9006abbc8fbd732691882580479.jpg)
Diskuze
Dapagliflozin je vysoce selektivní inhibitor SGLT2, který snižuje hyperglykemii potenciací glykosurie. Účinkuje tedy nezávisle na funkci β buněk a doplňuje mechanizmy účinku antidiabetik závislé na inzulinu s minimálním rizikem hypoglykemie. V klinických studiích, ve kterých byl dapagliflozin hodnocen jak v monoterapii, tak v kombinaci s metforminem, derivátem sulfonylurey, pioglitazonem či inzulinem, bylo prokázáno, že účinně snižuje nejen hodnotu glykovaného hemoglobinu, ale také tělesnou hmotnost a TK. Riziko hypoglykemií bylo ve většině studií podobné jako u placeba; mírně častěji byly zaznamenány močové infekce a infekce genitálu, popřípadě bolesti zad, polyurie či mírné zhoršení dyslipidemie. Dapagliflozin je nové, perspektivní antidiabetikum s komplexním působením a malým rizikem nežádoucích účinků, jež nepochybně významně zvýší kvalitu antidiabetické léčby.
Je všeobecně přijímáno, že dobrá kontrola glykemie je spojena se snížením mikrovaskulárních komplikací, mnohem méně je ale popisována korelace s makrovaskulárními komplikacemi [6]. Právě objev skupiny SGLT2 inhibitorů, případně GLP-1 receptorových agonistů, které snižují i makrovaskulární komplikace, vyvolává v léčbě DM velké naděje. Tyto naděje poprvé přinesly výsledky studie EMPA-REG OUTCOME [2], kde hlavní cíl KV úmrtí, IM a CMP byl snížen o 38 % relativního rizika. Studie CANVAS pak toto potvrdily 14% snížením rizika [4]. V obou studiích bylo riziko snížení hospitalizací pro SS, a to o 35 %, resp. 33 %. Studie DECLARE si stanovila kompozitní cíl, a to jak úmrtí, tak hospitalizace pro SS.
Studie DECLARE si stanovila taktéž bezpečnostní cíle, tak aby byly zodpovězeny některé otázky vyvolané výsledky studií EMPA-REG a CANVAS, především otázku na amputace dolních končetin [2,4].
Základní hypotéza studie DECLARE je, že zlepšení metabolických parametrů, a to jak snížení glykemie, tak snížení TK a hmotnosti, povede ke zlepšení (snížení) KV cílů, a to jak u populace s již známým KV onemocněním (CVD), tak u populace s „pouze“ rizikovými faktory (MRF) [7 – 10]. Proto bylo zařazeno 59,4 % pacientů bez prokázaného KV onemocnění, což odlišuje tuto studii od předchozích. Studie EMPA-REG zařadila pouze nemocné s prokázaným KV onemocněním a program CANVAS měl 3 486 (34,4 %) osob s pouze vícečetnými rizikovými faktory, ale bez prokázaného KV onemocnění.
Délka sledování ve studii EMPA-REG byla 3,1 let, v programu CANVAS 2,4 let. Ve studii DECLARE se očekává, že by to mohlo být kolem 4 let, což by mělo ještě více zdůraznit význam kontroly rizikových faktorů jako glykemie, TK a hmotnost na KV nemocnost i úmrtnost. Toto delší sledování umožní i lepší posouzení možnosti dalšího popisovaného nežádoucího účinku, a to výskytu karcinomu močových cest. Výhodou studie DECLARE je i velmi rychlý nábor pacientů umožněný velkým počtem center a zemí účastnících se studie, kdy dlouhý nábor jako třeba v programu CANVAS je pak ovlivněn i měnící se doprovodnou terapií [2,11].
Studie DECLARE má velké množství nemocných užívajících statiny, antiagregační či antikoagulační léčbu, ACE inhibitory či sartany a betablokátory, tedy vysoce kvalitní KV léčbu v primární či sekundární prevenci [12]. Je pochopitelné, že je rozdíl v užívání těchto léků mezi primární a sekundární prevencí i ve studii DECLARE. Dík velkému vzorku sledované populace bude ale možné udělat i subanalýzy. Rozdíly jsou samozřejmě i v preskripci dalších antidiabetik a inzulinu, které jsou pravděpodobně závislé i na délce trvání DM. Rozdíly se předpokládají i v hodnocení renálních funkcí, kdy studie DECLARE má menší postižení ledvin než předchozí dvě studie. Předpokládá se, že bude potvrzen renální efekt SGLT2 inhibitorů [13,14].
Závěr
Studie DECLARE-TIMI 58 je velkou klinickou studií zahrnující velké počty nemocných jak s potvrzeným KV onemocněním, tak s rizikovými faktory. Tato rozsáhlost studie umožní subanalýzy s významnými klinickými důsledky, včetně důležité informace u nemocných s rizikovými faktory, ale zatím bez prokazatelného KV onemocnění. Studie popíše nejen KV výstupy, ale i renální bezpečnost. Studie by měla mít zásadní význam pro budoucí doporučení léčby nemocných s DM2.
Hlavní výhody studie DECLARE jsou:
- DECLARE-TIMI 58 je velká multicentrická, randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie s robustním designem,
- má nejvíce zařazených pacientů s SGLT2 inhibitory z KV studií - 17 160 pacientů,
- široká populace pacientů zahrnuje pacienty s rizikovými faktory (60 %) nebo s KV onemocněním v anamnéze (40 %),
- rozmanitost zařazené populace posílí externí validitu a aplikovatelnost výsledků studie,
- očekávaný medián sledování je dlouhý, odhaduje se 4,5 roku.
Za mírnou nevýhodu studie se považuje delší dokončení studie kvůli designu a počtu zařazených pacientů, které vyžadují větší počet nahromaděných příhod.
Doručeno do redakce: 2. 2. 2018
Přijato po recenzi: 13. 2. 2018
prof. MU Dr. Jindřich Špinar, CSc., FESC
Zdroje
1. Prázný M, Šoupal J. Postavení nových antidiabetik v klinické praxi: SGLT2 vs DPP4 inhibitory. Vnitř Lék 2015; 61(4): 291 – 294.
2. Zinman B, Wanner CH, Lachin JM et al. The EMPA-REG OUTCOME Investigators. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015; 373(22): 2117 – 2128. doi: 10.1056/ NEJMoa1504720.
3. Kvapil M. EMPA REG OUTCOME. Důkaz, že populace pacientů s diabetem se mění. Remedia 2016; 26 : 67 – 72.
4. Neal B, Perkovic P, Mahaffey KW et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. NEJM 2017; 377(7): 644 – 657. doi: 10.1056/ NEJMoa1611925.
5. Raz I, Mosenzon O, Bonaca MP et al. DECLARE-TIMI 58: participants baseline charcteristics. Diabetes Obes Metab 2018. doi: 10.1111/ dom.13217.
6. Bergenstal RM, Bailey CJ, Kendall DM. Type 2 diabetes: assessing the relative risks and benefits of glucose-lowering medications. Am J Med 2010; 123(4): 374.e 9 – 18. doi: 10.1016/ j.amjmed.2009.07.017.
7. Ferrannini E, Mark M, Mayoux E. CV Protection in the EMPA-REG outcome trial: a "thrifty substrate" hypothesis. Diabetes Care 2016; 39(7): 1108 – 1114. doi: 10.2337/ dc16-0330.
8. Mudaliar S, Alloju S, Henry RR. Can a shift in fuel energetics explain the beneficial cardiorenal outcomes in the EMPA-REG OUTCOME study? A unifying hypothesis. Diabetes Care 2016; 39(7): 1115 – 1122. doi: 10.2337/ dc16-0542.
9. Vallon V, Thomson SC. Targeting renal glucose reabsorption to treat hyperglycaemia: the pleiotropic effects of SGLT2 inhibition. Diabetologia 2017; 60(2): 215 – 225. doi: 10.1007/ s00125-016-4157-3.
10. Heerspink HJ, Perkins BA, Fitchett DH et al. Sodium glucose cotransporter 2 inhibitors in the treatment of diabetes mellitus: cardiovascular and kidney effects, potential mechanisms, and clinical applications. Circulation 2016; 134(10): 752 – 772. doi: 10.1161/ CIRCULATIONAHA.116.021887.
11. Fletcher B, Gheorghe A, Moore D et al. Improving the recruitment activity of clinicians in randomised controlled trials: a systematic review. BMJ Open 2012; 2(1): e000496. doi: 10.1136/ bmjopen-2011-000496.
12. Piepoli MF, Hoes AW, Agewall S et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J 2016; 37(29): 2315 – 2381. doi: 10.1093/ eurheartj/ ehw106.
13. Wu JH, Foote C, Blomster J et al. Effects of sodium-glucose cotransporter-2 inhibitors on cardiovascular events, death, and major safety outcomes in adults with type 2 diabetes: a systematic review and meta-analysis. Lancet Diabetes Endocrinol 2016; 4(5): 411 – 419. doi: 10.1016/ S2213-8587(16)00052-8.
14. Wanner C, Inzucchi SE, Lachin JM et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016; 375(4): 323 – 334. doi: 10.1056/ NEJMoa1515920.
15. Raz I et al. Poster 1245-P. 77th Scientific Sessions of the American Diabetes Association. San Diego, CA, 2017.
16. Raz I et al. Poster 1129. 53rd Annual Meeting of the European Association for the Study of Diabetes. Lisabon, Portugal, 2017.
17. Study NCT01730534. ClinicalTrials.gov website. Accessed December 2017.
18. In House Data, AstraZeneca Pharmaceuticals LP. CSP D1693C00001; H1 2017 results. Published 2017.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2018 Číslo 1
-
Všechny články tohoto čísla
- Srdeční selhání ve stáří
- Léčba arteriální hypertenze u starších osob
- Polyfarmakoterapie ve stáří – lékové interakce nejčastěji předepisovaných lékových skupin v kardiologii
- Chronické srdeční selhání a paliativní péče
- Tyreopatie ve stáří a kardiovaskulární postižení
- Přínosy a rizika profylaxe tromboembolické nemoci u geriatrického pacienta
- Imunosenescence a infekční komplikace vyššího věku
- Závratě a pády jako častá symptomatologie kardiovaskulárního postižení ve vyšším věku
- Duální inhibice AT1 receptoru pro angiotenzin II a neprilysinu nebo inhibice angiotenzin konvertujícího enzymu?
-
Stručný komentář k novým doporučením pro léčbu hypertenze v USA
2017 ACC/ AHA High Blood Pressure Guideline - Specifika diagnostiky a léčby ve stáří
- Dapagliflozin a studie DECLARE – vstupní charakteristika
- Přehled echokardiografických parametrů v diagnostice srdečního selhání se zachovalou ejekční frakcí levé komory
- Zvýšená hladina NP u stabilních pacientů 3 měsíce po STEMI je jednoduchý nástroj k predikci dlouhodobé nepříznivé prognózy
- Klinická kardiologie (3. vyd.)
- Zpráva z akce – ACC 2018 v Orlandu
- Zemřel prof. MUDr. Roman Čerbák, CSc., FESC *19. 10. 1933 – †4. 3. 2018
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Přehled echokardiografických parametrů v diagnostice srdečního selhání se zachovalou ejekční frakcí levé komory
- Specifika diagnostiky a léčby ve stáří
- Srdeční selhání ve stáří
- Tyreopatie ve stáří a kardiovaskulární postižení
