Lékové interakce – aktuálně a prakticky
Drug interactions – current and practical
Drug interaction can be defined as the change of an effect of a drug owing to synchronous giving of this drug with the another one or with more other drugs, with certain food, drink or an other chemical substance. Undesirable drug interactions belong to adverse drug effects. An occurance of drug interactions increases with a number of using drugs. A contemporary pharmacotherapy and deficiencies in a health care system bring a risk of drug interactions, false drug interactions and duplicities. Series drug interactions can cause also „over the counter“ drugs which patient uses mostly without an advisement of a treating medical doctor. A basic source of information about known drug interactions of a concrete patient is the Summary of Product Characteristics. Authors divide drug interactions to interactions leading to an amplifying of an effect, to a reducing of an effect, to a potentiation of an adverse effect or to a rise of a new one and to a very serious up to a fatal adverse effect. The article is completed with a table of examples of drug interactions leading to a very serious up to a fatal adverse effect.
Keywords:
Drug interactions – adverse effect – CYP3A4 – CYP2D6 – P-glycoprotein – QT interval – serotonine syndrome
Autoři:
Holý J.; Pešková M.
Působiště autorů:
Interní oddělení Nemocnice České Budějovice, a. s. Zdravotně sociální fakulta Jihočeské Univerzity, České Budějovice
Vyšlo v časopise:
Kardiol Rev Int Med 2020, 22(3): 103-107
Souhrn
Lékovou interakci lze definovat jako změnu účinku léku následkem současného podávání tohoto léku s lékem jiným či s více jinými léky, s určitou potravou, nápojem či jinou chemickou látkou. Nežádoucí lékové interakce patří mezi nežádoucí účinky léčiv. Výskyt lékových interakcí stoupá s počtem užívaných léků. Současná farmakoterapie i nedostatky systému zdravotnické péče přinášejí riziko lékových interakcí, nepravých lékových interakcí a duplicit. Závažné lékové interakce mohou způsobit i volně prodejná léčiva, které nemocný užívá většinou bez vědomí ošetřujícího lékaře. Základním zdrojem informací o známých lékových interakcích konkrétního léku je souhrn údajů o přípravku. Autoři dělí lékové interakce na interakce vedoucí k zesílení účinku, k zeslabení účinku, k potenciaci či ke vzniku nového nežádoucího účinku a k velmi závažnému až fatálnímu nežádoucímu účinku. Článek je doplněn tabulkou příkladů konkrétních lékových interakcí vedoucí k velmi závažnému až fatálnímu nežádoucímu účinku.
Klíčová slova:
lékové interakce – nežádoucí účinek – CYP3A4 – CYP2D6 – P-glykoprotein – QT interval – serotoninový syndrom
Úvod – význam lékových interakcí
Lékovou interakci (LI) lze definovat jako změnu účinku léku následkem současného podávání tohoto léku s lékem jiným či s více jinými léky. Faktorem, který účinek léku změní, může však být i potrava, nápoje či jiné chemické látky, které se do organizmu dostanou z okolního prostředí [1]. Známy jsou též takové LI, ke kterým dojde po následném podání dvou léčiv (tedy ne současném) nebo po vysazování jednoho ze dvou současně podávaných léčiv [2]. Jednou změnou účinku léku následkem LI je zvýšení jeho účinku, pak mluvíme o synergizmu, další změnou může být naopak zeslabení tohoto účinku, kdy mluvíme o antagonizmu. Jindy je účinek zcela rozdílný od účinku, který by nastal, pokud by byl lék podán ve stejné dávce jednotlivě. V takovém případě se nejčastěji jedná o účinek toxický [3]. Takový účinek lze jistě zařadit k účinkům nežádoucím. Nežádoucí účinek (NÚ) léčiva lze definovat jako škodlivou a nepředpokládanou reakci, která se objevuje u člověka při běžně používaných dávkách [2]. Všechny LI však rozhodně nepatří k nežádoucím účinkům léčiv. Existují i žádoucí, prospěšné LI, které lze naopak terapeuticky využít. Synergizmus účinku je využíván při kombinaci imunosupresivní farmakoterapie po orgánové transplantaci, při kombinované chemoterapii onkologických onemocnění, při kombinované antimikrobiální léčbě, léčbě hypertenze i bronchiálního astmatu. Účinek antagonistický využíváme například při podání naloxonu kvůli předávkování opioidů, extrapyramidový syndrom jako NÚ dlouhodobého užívání neuroleptik lze zmírnit antiparkinsonikem s anticholinergním účinkem [3]. Téma žádoucích LI však přesahuje téma tohoto článku, kterým jsou zejména LI nežádoucí. Význam znalosti LI stoupá, neboť stále více nemocných užívá pravidelně více léčivých přípravků [2].
Tento fakt se týká zejména občanů České republiky, neboť ti patří ve spotřebě léků v rámci Evropské unie k nejvíce exponované populaci, vyšší spotřebu mají jen občané Maďarska a Francie [4]. Je prokázáno, že výskyt LI stoupá s počtem současně podávaných léků, a to prakticky exponenciálně [5]. Užívá-li nemocný 10 léků současně, je pravděpodobnost vzniku klinicky závažné LI asi 15 %, užívá-li současně 20 léků, je pravděpodobnost klinicky závažné LI stoupá asi na 60 % [4]. Ještě větším rizikem farmakoterapie, než jsou LI, bývají duplicity, k jejichž výskytu přispívá i fakt, že řada různých léků obsahuje tutéž léčivou látku, aniž by název takového léku připomínal, o jakou látku se jedná [6]. Riziko duplicit, popř. dokonce multiplicit stoupá také díky užívání fixních kombinací. Obdobné riziko představují též tzv. nepravé LI, kdy jsou nemocnému podávány dva různé přípravky obsahující tutéž léčivou látku či látku s podobným účinkem [7]. K riziku LI, nepravých LI a duplicit přispívá též současný systém zdravotní péče, kdy o jednoho nemocného pečuje několik specialistů, kteří nemusí být přesně obeznámeni s aktuální medikací nemocného. V takovém případě je potřeba, aby konečné lékové schéma vytvářel jeden lékař, který bude znát vyjádření všech specialistů, bude dlouhodobě znát i nemocného, vč. jeho soběstačnosti a kognitivních funkcí. Role takového koordinátora však zejména ve větších městech s dobrou dostupností specializovaných ambulancí citelně chybí [8].
Výskyt lékových interakcí
Ohledně výskytu nežádoucích LI nemáme přesná data. Objektivní hodnocení prevalence LI je obtížné jak pro nedostatky v jejich evidenci, tak proto, že všechny LI nejsou rozpoznány. Diagnostika LI vyžaduje totiž důkladnou diferenciálně diagnostickou rozvahu, pro kterou musí být odborník vybaven klinickými i teoretickými znalostmi. Studie, které se výskytu LI věnovaly, měly různý metodologický přístup a většina byla provedena u nemocných hospitalizovaných. Výrazně vyšší výskyt LI byl zjištěn v geriatrických a psychiatrických zařízeních [1]. Podle starších studií se klinicky významné LI projevily odhadem u 4–5 % hospitalizovaných nemocných, podle další starší studie byla LI bezprostřední příčinou hospitalizace u méně než 1 % nemocných [3]. LI jsou spolu s dalšími nežádoucími účinky léků a s chybami v užívání léků příčinou hospitalizace seniorů až ve 28 % [8]. V ambulantní sféře se LI vyskytují zřejmě častěji než v nemocnicích, dle starší analýzy údajů o 400 000 nemocných v primární a sekundární péči se u 11,1 % z nich objevily příznaky, které byly pravděpodobně důsledkem LI [3]. Incidence prokazatelných následků LI je uváděna v enormně širokém rozpětí, a to 4–88 % [5,9]. Při analýze databáze zdravotní pojišťovny Škoda Mladá Boleslav bylo zjištěno, že se u klientů této pojišťovny v roce 2006 vyskytly kontraindikované lékové interakce u předepisovaných léčiv ve 711 případech, což by prostou matematickou aproximací na celou populaci ČR znamenalo výskyt přesahující 60 000 případů [4]. Na výskytu LI se může podílet i „samoléčitelství“ nemocnými, o kterém se ošetřující lékaři většinou nedozví. V lékárnách i v jiných prodejnách lze získat tzv. volně prodejná léčiva („over the counter“, „OTC“ drugs), která představují z pohledu LI stejná rizika jako léky vázané na preskripci [10]. Riziko LI představují i fytofarmaka, potravinové doplňky a různé složky potravy, které jsou v tomto směru podceňovány ještě více než léčiva volně prodejná [10]. Počet publikovaných LI v současné době již značně přesáhl počet 20 000, z toho je přibližně 4 500 LI klinicky velmi významných [4]. Dle jiného zdroje je počet kontraindikovaných lékových kombinací (komedikací) několik tisíc [11].
Klasifikace (dělení) lékových interakcí
Jak již bylo uvedeno výše, lze z hlediska léčebného prospěchu či jeho opaku LI dělit na prospěšné, tj. žádoucí, a na škodlivé, tj. nežádoucí [2]. Podle mechanizmu vzniku lze LI rozdělit na farmaceutické, farmakodynamické a farmakokinetické [1,5,9]. Při farmaceutických LI dochází ke vzájemnému fyzikálně chemickému či chemickému ovlivnění buď ještě mimo organizmus či na úrovni vstupní cesty do organizmu [5]. Jedná se vlastně o lékové inkompatibility [1]. Při LI farmakodynamických je účinek jednoho léků změněn přítomnosti dalšího v místě jeho účinku, a to buď přímo na receptorech, nebo nepřímo interferencí s fyziologickým mechanizmem [1]. Farmakodynamické LI jsou častější než farmakokinetické, ovšem při znalosti farmakologie jsou obvykle lépe predikovatelné [5]. Při LI farmakokinetických dochází k ovlivnění léčiv v organizmu při cestě k cíli jejich účinku, k orgánům eliminace či při jejich eliminaci z těla. Lze tedy rozlišit LI na úrovni absorpce, biodistribuce a eliminace, skládající se z biotransformace (metabolizmu) a exkrece [3,5]. K LI však může docházet na více úrovních, jeden lék může vyvolat LI jak farmakokinetickou, tak farmakodynamickou [3]. Z hlediska výsledného efektu lze LI rozdělit na LI vedoucí k zesílení účinku, k zeslabení účinku, vedoucí k potenciaci či vzniku nového NÚ a nakonec vedoucí ke vzniku velmi závažného až fatálního NÚ. Toto dělení bude vzhledem k jeho praktičnosti použito i v tomto článku.
Zdroje informací o lékových interakcích
Základním zdrojem informací o známých LI konkrétního léčivého přípravku (dále LP) je souhrn údajů o přípravku (summary of product characteristics – SPC). Jde o část dokumentace, kterou předkládá výrobce LP ke schválení registračním orgánům. SPC jako základní zdroj informací o konkrétním LP je určen odborným pracovníkům, tedy lékařům a farmaceutům. Základním zdrojem informací pro pacienty je pak příbalová informace či leták (PIL), který musí být plně v souladu se schváleným SPC [2]. Tyto informace jsou dostupné na internetových stránkách registračních orgánů, ale též např. v pravidelně aktualizované databázi automatizovaného informačního systému léčivých přípravků, známého pod zkratkou AISLP (www.aislp.cz). Je však třeba upozornit na to, že výzkum na poli LI probíhá i po registraci léčivého přípravku a ročně vycházejí řádově desítky až stovky publikací o LI nových. Důležité nové informace o konkrétním LP by se měly do SPC LP doplnit, ovšem aktualizace SPC je zdlouhavým administrativním procesem. SPC konkrétního LP tedy v daném čase nemusí vždy odrážet aktuální situaci. Zdrojem významných aktuálních informaci na poli LI budou jistě registrační orgány, které jsou za dozor nad LP, tedy za farmakovigilanci, zodpovědné. Tuzemský registrační orgán Státní ústav pro kontrolu léčiv například vydává informační zpravodaj „Nežádoucí účinky léčiv“ a měsíčník Farmakoterapeutické informace [11,12]. Držitelé rozhodnutí o registraci (tedy výrobci LP) předávají zdravotníkům nové, důležité informace týkající se bezpečnosti LP pomocí tzv. Informačních dopisů. K výzkumným účelům je v publikacích nejčastěji užit „software“ Micromedex® Drug-Reax, který někteří autoři považují za nejspolehlivější kvůli vysoké senzitivitě [13]. Internetové stránky Drugs.com přinášejí aktualizované informace o více než 24 000 léčivech na předpis, o volně prodejných léčivech i o přírodních produktech. Tyto stránky klasifikují LI do 4 skupin – jako méně důležité (minor), mírné (moderate), větší (major) a neznámé (unknown) (drugs.com). Tématem LI se dlouhodobě zabývá tuzemská společnost DrugAgency, a. s., která vytváří, nabízí a pravidelně aktualizuje CD Kompendium lékových interakcí DrugAgency, a. s. Program stratifikuje riziko LI při současném podávání dvou léků ve škále 0–6. Hodnocení 0 znamená, že k LI prokazatelně nedochází, hodnocení 1–6 znamená riziko LI, které roste s výší číslice. Hodnocení 5 znamená velmi závažnou LI, kdy je většinou vhodné oba léky současně nepodávat, při hodnocení 6 je současné podávání obou léků kontraindikováno [14]. Program využívající americkou databázi léčivých přípravků se nazývá Lexicomp. Tento program hodnotí LI písmeny A až D, písmeno X znamená kontraindikaci testované komedikace [15]. Jednou z významných a obsáhlých monografií je Stockley’s Drug Interactions (přes 1 000 stránek). Nelze též nezmínit příspěvek Farmakologické interakce v knize Pokroky ve farmacii 1. z roku 1978 od tuzemských průkopníků problematiky LI [16].
Lékové interakce vedoucí k zesílení účinku – příklady
Klinicky závažné LI v komedikaci s jinými léčivy vyvolává nejčastěji warfarin, obávané jsou zejména LI vedoucí ke zvýšení jeho antikoagulačního účinku, a tudíž k riziku krvácení, a to i život ohrožujícímu. Žádné jiné perorální antikoagulans nemá tolik popsaných LI a žadné jiné nemá tak významné rozdíly v dávkování jako právě warfarin [17]. Antikoagulační účinek warfarinu je zvyšován amiodaronem, příčinou této LI je inhibice metabolizmu S i R izoformy warfarinu na úrovni cytochromu P450, konkrétně enzymu CYP3A4. Cytochrom P450 je lokalizován především v játrech a ve střevě a jde o rodinu asi 100 izoenzymů, přičemž nejvíce léků metabolizuje právě izoenzym CYP3A4 [11]. K této inhibici dochází 4–6 dní od začátku terapie amiodaronem a může přetrvávat 6–16 týdnů po ukončení této terapie [18]. Dalším antiarytmikem zvyšujícím účinek warfarinu je např. propafenon, který je metabolizován enzymy CYP2D6, CYP3A4 a CYP1A2, z nichž poslední dva metabolizují i R-izoformu warfarinu [18]. Udává se, že při této komedikaci se plazmatická hladina warfarinu zvyšuje až o 50 % [18]. Dalším lékem zvyšujícím antikoagulační účinek warfarinu s rizikem krvácení je klaritromycin, který inhibuje enzym CYP3A4 [19]. Poměrně nedávno se zjistilo, že také paracetamol podávaný pravidelně a ve vyšších dávkách může zvýšit účinnost warfarinu, toto zvýšení však může být malé či jen středně velké a neznamená, že by tuto komedikaci nebylo možno podávat vůbec [6]. Obecně lze doporučit monitoraci protrombinového času – „international normalized ratio“ (INR) po nasazení a po případném vysazení léčiva, které potenciální LI s warfarinem vyvolává, dále je doporučováno aktivně pátrat po krvácivých projevech. Ovšem ani tzv. nová perorální antikoagulancia nejsou bez rizika LI, a jelikož všechna perorální antikoagulancia mají úzké terapeutické okno, jakákoli odchylka v jejich hladině může vést ke krvácivým či naopak k trombotickým NÚ [17]. Vzhledem k riziku zvýšení účinku dabigatranu jsou spolu s ním kontraindikovány silné inhibitory tzv. P-glykoproteinu (PgP), kterými jsou ketokonazol, itrakonazol, cyklosporin a dronedaron [17]. PgP je transmembránovým přenašečem či efluxní pumpou kódovanou genem MDR1 (multidrug resistance), tato pumpa přenáší substráty ven z buňky. PgP je přítomen v ledvinách, játrech, tenkém i tlustém střevě, mozku, varlatech, nadledvinách, těhotné děloze, ale i v nádorových buňkách [2]. PgP omezuje absorpci svých substrátů ze střevního lumen, omezuje jejich distribuci do mozku a podporuje jejich vylučování do žluči a do moči [11]. Při komedikaci dabigatranu s amiodaronem a verapamilem je doporučena redukce dávky dabigatranu [20]. Při léčbě rivaroxabanem či apixabanem je třeba se kvůli riziku předávkování vyhnout inhibitorům PgP a současně i enzymu cytochromu P 450 3A4, ke kterým patří azolová antimykotika (ketokonazol, itrakonazol, vorikonazol) a inhibitory proteáz HIV, např. ritonavir [20]. Jiným příkladem zvýšení účinku vlivem LI je komedikace teofylinu s ciprofloxacinem i s jinými chinolony. Výrobce doporučuje při takové komedikaci snížit dávku theofyllinu na maximálně 60 % dávky doporučené a během léčby theofyllinem spolu s chinolony je důrazně doporučováno stanovení hladin theofyllinu v séru [21]. Nelze nezmínit též grapefruitový džus, který díky inhibici izoenzymu 3A4 ve střevě zvyšuje plazmatické hladiny a AUC řady léků, tento efekt byl poprvé prokázán v r. 1991 u dvou dihydropyridinových blokátorů kalciových kanálů – u felodipinu a nifedipinu [22].
Lékové interakce vedoucí k zeslabení účinku – příklady
Pravděpodobně nejrozšířenější LI bude nejspíše snížení antihypertenzního účinku hypotenziv při komedikaci s nesteroidními antiflogistiky (NSA). K této LI dochází zřejmě kvůli inhibici syntézy prostaglandinů a projevuje se zejména u betablokátorů, diuretik a inhibitorů angiotenzin-konvertujícího enzymu [5]. Krevní tlak je při takovéto komedikaci zvýšen většinou o několik mm Hg a je vhodné o tom nemocné poučit a krevní tlak kontrolovat [23]. Účinek warfarinu je snižován fenytoinem, karbamazepinem, azathioprimem a samozřejmě vitamínem K [11]. Významným enzymovým induktorem je rostlina třezalka tečkovaná (Hypericum perforatum), ze které se využívá sušená nať, a to zejména jako součást čajových směsí či ve formě granulí. S touto rostlinou interaguje mnoho léků včetně warfarinu [24]. Třezalka tečkovaná a další silné inhibitory enzymu CYP3A4, jako jsou karbamazepin, fenytoin a fenobarbital mohou vést při současném podávání rivaroxabanem ke snížení plazmatických hladin rivaroxabanu [25]. Další silný inhibitor izoenzymu 3A4 rifampicin vede při komedikaci s rivaroxabanem přibližně k 50% poklesu střední hodnoty AUC rivaroxabanu. Výrobce proto doporučuje se současnému podávání výše uvedených induktorů enzymu CYPC3A spolu s rivaroxabanem vyhnout, pokud není nemocný pozorně sledován kvůli známkám a příznakům trombózy [25]. Tato podmínka je spíše iluzorní, nebo prvním příznakem trombózy může být i život ohrožující plicní embolie. Antagonisté H2 receptorů (např. ranitidin) i inhibotory protonové pumpy (IPP) snižují plazmatické koncentrace azolových antimykotik, neboť ke vstřebávání těchto antimykotik je zapotřebí kyselého pH v žaludku, čemuž antagonisté H2 receptorů či IPP zabraňují [23]. Tímto mechanizmem IPP snižují absorpci ketokonazolu a itrakonazolu, ne však flukonazolu [26]. Pantoprazol snižuje hladinu imunosupresiva mykofenolátu-mofetilu až o 30 % [26]. Účinek všech antidiabetik se snižuje podáváním glukokortikoidů [22], dále též thiazidů i perorálními kontraceptivy [3,5]. Při podávání fenytoinu či karbamazepinu nemocnému užívajícímu simvastatin dojde vlivem indukce těmito antiepileptiky k snížení plazmatických hladin simvastatinu k subterapeutické úrovní [11].
Lékové interakce vedoucí k potenciaci či vzniku nového nežádoucího účinku
Ke zvýšení rizika gastrotoxicity dochází při současném podávání nejen nesteroidních antiflogistik (NSA) spolu s glukokortikoidy, ale též NSA s antidepresivy – inhibitory zpětného vstřebávání serotoninu (SSRI), což platí nejvíce pro neselektivní NSA. Potenciaci gastrotoxicity při komedikaci NSA s SSRI dokládá epidemiologická studie Helin-Salmivaara. Toto riziko lze snížit podáváním COX-2 selektivního NSA či současnou gastroprotekcí nejlépe IPP [23]. Kombinujeme-li amiodaron s betablokátory, verpamilem nebo diltiazemem, je třeba se obávat zhoršení již existujícího srdečního selhání, závažné hypotenze, bradyarytmie až asystolie. I když může kombinace amiodaronu s některými betablokátorty zlepšit prognózu nemocných po infarktu myokardu, je nezbytné tyto nemocné pečlivě sledovat. Amiodaron díky inhibici izoenzymu 2D6 zvyšuje plazmatické hladiny betablokátorů metabolizovaných enzymem CYP2D6, kterými jsou metoprolol, betaxolol, bisoprolol, nebivolol a karvedilol. Kombinace amiodaronu a betablokátoru sotalol je kvůli své nebezpečnosti dokonce kontraindikovaná [23]. Pokud podáváme antidiarhoikum loperamid, který se váže na opioidní receptory, spolu ketokonazolem či itrakonazolem, pak se objeví centrální opioidní příznaky, zejména útlum dechového centra. Důvodem je jednak inhibice enzymu CYP3A4, která jednak vede ke zvýšení plazmatických hladin loperamidu, jednak inhibice i PgP, která umožní přestup hematoencefalickou bariérou a tak průnik do centrálního nervového systému [23]. Významnou roli v LI hraje grapefruitová šťáva, která díky inhibici enzymu CYP3A4 zvyšuje hladiny řady léků [24], např. většiny blokátorů kalciových kanálů [22]. V r. 1991 Bailey et al publikovali práci o možnosti zvýšení biologické dostupnosti, a tím i účinku dvou dihydropyridinových blokátorů kalciovýchh kanálů – felodipinu anifedipinu [22]. LI grapefruitového džusu s felodipinem se stala modelovou a nejčastěji studovanou. Jednorázové podání 250 ml grepového džusu zvýšilo AUC felodipinu o 167 % a maximální plazmatickou hladinu o 245 %. Pětidenní podávání grepového džusu vede ke zvýšení AUC felodopinu o 300 % a maximální plazmatickou koncentraci o 500 % [22]. Vysvětlením je redukce enzymu CYP 3A4 v enterocytech tenkého střeva o 62 % [22]. Výrobce felodipinu proto užívání léku spolu s grapefruitovou šťávou zakazuje [27]. Při současném podávání grapefruitového džusu spolu verapamilem došlo ke zvýšení AUC verapamilu od 43 %, současně se však objevil i AV blok 1. stupně [22]. Byla popsána kazuistika nemocné léčené simvastatinem, která požívala několik dnů současně plody grapefruitu, což vedlo k rabdomyolýze s akutním selháním ledvin s nutností hospitalizace a přechodné léčbě hemodialýzou [4]. Je potřebné též uvést, že kombinace inhibitorů ACE či antagonistů angiotenzinu II (sartanů) spolu s furosemidem a NSA zvyšuje četnost nefropatií. Těmito LI jsou zvláště ohroženi senioři a diabetici, a to i ti diabetici, u kterých se známky nefropatie dosud neobjevily [23]. Při kombinaci inhibitorů ACE či sartanů se spironolaktanem či jiným kalium šetřícím diuretikem hrozí závažná hyperkalemie, která může skončit fatálně [23]. Výše uvedená kombinace ve studii RALES sice prokázala příznivý vliv na přežívání nemocných se srdečním selháním se systolickou dysfunkcí levé komory srdeční, ale nemocný s hyperkalemií byli ze studie vyřazeni a u ostatních byla kalemie pečlivě monitorována [23]. Hyperkalemie dále hrozí při komedikaci kalium šetřícího diuretika spolu s Kalium chloratum [1].
Lékové interakce vedoucí ke vzniku velmi závažného až fatálního nežádoucího účinku
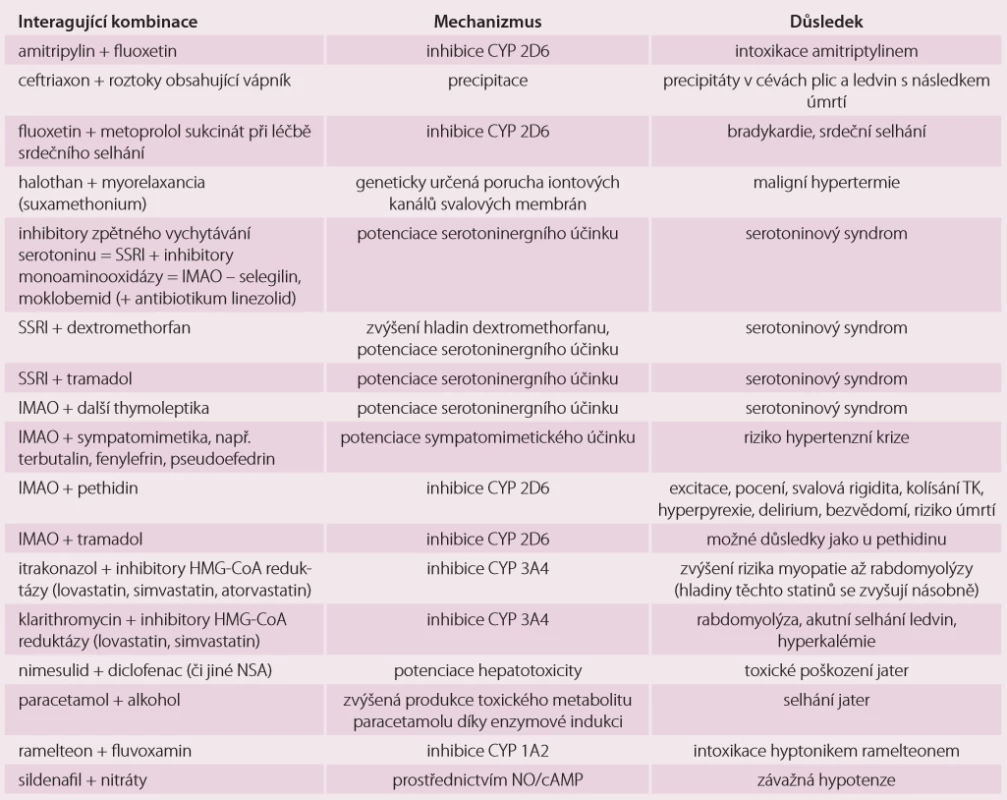
Nejvýznamnější příklady potenciálních velmi závažných až fatálních LI shrnuje tab. 1. Při podávání dvou a více jakýchkoli léků prodlužující QT interval na EKG, hrozí komorová tachykardie typu Torsades de Pointes (TdP), která špatně reaguje na antiarytmickou medikaci a je potenciálně fatální. Nebezpečí této maligní arytmie dále zvyšuje vrozené prodloužení intervalu QT, vyšší věk, kardiovaskulární onemocnění a hypokalemie [23]. Tato arytmie také hrozí při současném podání grapefruitového džusu s terfenadinerm, astemizolem a cisapridem [22]. Toto riziko maligní arytmie vedlo ke stažení terfenadinu, astemizolu, cisapridu i thioridazinu z trhu v ČR [23]. Erytromycin toho času v ČR též dostupný není, proto riziková kombinace terfenadinu s erytromycinem s rizikem komorových arytmií TdP v tab. 1 uvedena není. Mnoho léků z více lékových skupin působí serotoninergně, tedy zvyšují dostupnost neurotransmiteru serotoninu. Vzájemná kombinace těchto léků zvyšuje riziko tzv. serotoninového syndromu. Tento syndrom se projevuje příznaky jednak centrálními, ke kterým patří zmatenost, mánie, dysartrie, třes, hyperreflexie, svalové záškuby a motorická inkoordinace, jednak příznaky periferními, ke kterým patří abdominální křeče, meteorizmus, průjem, hypertenze, tachykardie, pocení a kardiovaskulární kolaps [2]. Jiní autoři do tohoto syndromu zařazují i horečku, respektive zimnici [23]. Jde o syndrom vzácný, ale potenciálně fatální. V případě, že nemocný užívá jeden ze serotoninergních léků, lze při diagnostice serotoninového syndromu použít tzv. Sternbachova kritéria. Není bez zajímavosti, že jedním z léků, které mohou serotoninový syndrom v kombinaci s jiným serotoninergním lékem vyvolat, je i třezalka tečkovaná [28].
Závěr
Problematika nežádoucích LI v současnosti nabírá na významu. Je to dáno jednak zvyšující se spotřebou léků, která se projeví také v polypragmazii jednotlivých nemocných, a tak zvýšením rizika LI, jednak zvýšením délky života, kdy seniorský věk představuje jeden z rizikových faktorů vzniku LI. Navíc mohou závažné LI způsobit i volně prodejná léčiva, o jejichž užívání nemocným se ošetřující lékaři většinou nedozví, též fytofarmaka, potravinové doplňky i různé složky potravy, které jsou podceňovány ještě více. Z této skupiny byl v tomto článku podtrhnut význam extraktů z třezalky tečkované jako enzymového induktoru a grapefruitového džusu jako naopak enzymového inhibitoru.
Doručeno do redakce: 10. 8. 2020
Přijato po recenzi: 24. 8. 2020
MU Dr. Jiří Holý Holý, Ph.D.
www.nemcb.cz
holy@nemcb.cz
Zdroje
1. Grundmann M. Lékové interakce I. Interní medicína pro praxi 2000; 1 : 40–41.
2. Lincová D, Farghali H et al. Základní a aplikovaná farmakologie. 1. vyd. Praha: Galén 2002.
3. Perlík F, Martínková J. Lékové interakce. Postgraduální medicína 2002; 4 (3): 311–317.
4. Suchopár J, Prokeš M. Lékové interakce – problém nebo teoretické riziko? Praktické lékárenství 2007; 3 (5): 199.
5. Holý J, Pešková M. Lékové interakce a současná klinická praxe. Kardiol Rev Int Med 2015; 17 (1): 70–75.
6. Prokeš M, Suchopár J. Kombinovaná analgetika-antipyretika a jejich rizika. Medicína pro praxi 2015; 12 (5): 247–251.
7. Prokeš M. Lékové interakce – skrytá hrozba. Dostupné na: http: //www.edukafarm.cz/c456-lekove-interakce-skryta-hrozba.
8. Matějovská Kubešová H, Bielaková K, Výška O et al. Polyfarmakoterapie ve stáří: problém lékových interakcí nejčastěji předepisovaných lékových skupin v kardiologii. Kardiol Rev Int Med 2018; 20 (1): 22–28.
9. Květina J, Grundmann M. Farmakologické interakce. Klin Farmakol Farm 2003; 1 : 17–21.
10. Doležal T. Lékové interakce volně prodejných léčiv. Dostupné na: https: //docplayer.cz/38328841-Úvod-lékové-interakce-volně-prodejných-léčiv-lékové-interakce-volně-prodejných-léčiv.html.
11. Farmakoterapeutické informace č. 11/2011. Dostupné na: http: //www.sukl.cz/sukl/listopad2011.
12. Informační zpravodaj Nežádoucí účinky léčiv. Dostupné na: http: //www.sukl.cz/sukl/informacni-zpravodaj-nezadouci-ucinky-leciv.
13. Roblek T, Vaupotic T, Mrhar A et al. Drug-drug interaction software in clinical practice: a systematic review. Eur J Clin Pharmacol 2015; 71 (2): 131–142. doi: 10.1007/s00228-014-1786-7.
14. Princip programu Kontrolní modul lékových interakcí Vademecum DrugAgency, a. s. Dostupné na: drugagency.cz.
15. Urbánek K. Lékové interakce a jejich praktický význam. Dostupné na: https: //www.healthcomm.cz/online/files/2.pdf.
16. Květina J, Fendrych Z. Farmakologické interakce. In: Pokroky ve farmacii 1. Praha: Avicenum 1978.
17. Suchopár J, Bultas J. Perorální antikoagulancia, jejich lékové interakce a dávkování u pacientů s fibrilací síní. Remedia 2015; 25 (2): 118–126.
18. Suchý D, Poklopová Z. Lékové interakce warfarinu s kardiovaskulárními léky. Klin Farmakol Farm 2005; 19 : 40–42.
19. Souhrn údajů o přípravku Warfarin Orion. Dostupné na: http: //www.sukl.cz/modules/medication.
20. Kessler P. Porovnání warfarinu a nových antitrombotik z hlediska lékových interakcí. Klin Farmakol Farm 2012; 26 (2): 74–78.
21. Souhrn údajů o přípravku Euphyllin CR N 100–400 mg. Dostupné na: http: //www.sukl.cz/modules/medication.
22. Grundmann M. Lékové interakce II. Int Med Prax 2000; 2 : 39–40.
23. Farmakoterapeutické informace č. 12/2011. Dostupné na: http: //www.sukl.cz/sukl/prosinec2011
24. Adamcová M. Přetahovaná mezi léky. Vesmír 2019; 98 : 586–587.
25. Souhrn údajů o přípravku Xarelto 2,5 mg potahované tablety. Dostupné na: http: //www.sukl.cz/modules/medication.
26. Špičák J. Léčba inhibitory protonové pumpy. Kardiol Rev Int Med 2014; 16 (3): 214–218.
27. Souhrn údajů o přípravku Plendil ER 5 + 10 mg tablety s prodlouženým uvolňováním. Dostupné na: http: //www.sukl.cz/modules/medication.
28. Prokeš M, Suchopár K. Serotoninový syndrom: co bychom o něm měli vědět. Med praxi 2014; 11 (5): 226-230.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2020 Číslo 3
-
Všechny články tohoto čísla
- Lékové interakce – aktuálně a prakticky
- Vybrané lékové interakce v kardiologii
- EMPEROR reduced – srdeční a renální cíle s empagliflozinem u nemocných se srdečním selháním se sníženou ejekční frakcí
- Kvalita života u nemocných po akutním infarktu myokardu
- Interakce léčiv se zaměřením na vybrané lékové skupiny v kardiologii
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Lékové interakce – aktuálně a prakticky
- Vybrané lékové interakce v kardiologii
- Interakce léčiv se zaměřením na vybrané lékové skupiny v kardiologii
- Kvalita života u nemocných po akutním infarktu myokardu
