Akutní selhání ledvin
Acute renal failure
Acute and chronic renal failure are rather historical terms, which have been replaced by the precisely defined terms "acute kidney injury" and "chronic kidney disease". Acute kidney injury is generally defined as a sudden deterioration in renal function due to a decrease in glomerular filtration and is diagnosed based on accumulation of nitrogen metabolism end products, decreased urine output, or both. Chronic kidney disease lasts at least 3 months, with damage being defined either by the presence of structural changes, a pathological urinary finding or a significant reduction in glomerular filtration. If the last criterion is used, no further signs of kidney damage are required for diagnosis. In some cases, it is unclear whether acute kidney injury or chronic kidney disease are present. In such cases, medical history, searching for stigmata of organ damage and the development over time are important for a correct diagnosis. The aim of this paper is to give a brief overview of acute kidney damage, diagnostic options and therapeutic modalities.
Key words:
acute renal injury – chronic kidney disease – glomerular filtration
Autoři:
J. Vachek; V. Tesař
Působiště autorů:
Klinika nefrologie 1. LF UK a VFN v Praze
Vyšlo v časopise:
Kardiol Rev Int Med 2017, 19(4): 285-287
Souhrn
Akutní a chronické selhání ledvin jsou již spíše historické pojmy, které byly nahrazeny exaktně definovanými termíny „akutní poškození ledvin“ a „chronické onemocnění ledvin“. Akutní poškození ledvin je obecně definováno jako náhlé zhoršení funkce ledvin podmíněné poklesem glomerulární filtrace a je diagnostikováno hromaděním konečných produktů metabolizmu dusíku, sníženým výdejem moči nebo obojím. Chronické onemocnění ledvin je definováno jako poškození ledvin trvající minimálně tři měsíce, přičemž poškození je definováno buď přítomností strukturních změn, patologického močového nálezu, nebo významným snížením glomerulární filtrace. Je-li užito toto kritérium, nejsou již nutné pro diagnózu další známky poškození ledvin. V některých případech není jasné, zda jde o akutní poškození ledvin či jejich chronické onemocnění, pak jsou pro diagnózu rozhodující anamnestické údaje, pátrání po stigmatech orgánových poškození a vývoj v čase. Cílem tohoto sdělení je podat stručný přehled o akutním poškození ledvin, diagnostických možnostech a terapeutických modalitách.
Klíčová slova:
akutní poškození ledvin – chronické onemocnění ledvin – glomerulární filtrace
Úvod
Selhání ledvin je popisný pojem užívaný v situaci, kdy neznáme dynamiku renálního poškození a nevíme, zda jde o akutně vzniklý stav nebo déle trvající proces, který je často asymptomatický. V současnosti se rozlišují dvě základní klinické jednotky: akutní poškození ledvin (acute kidney injury – AKI) a chronické onemocnění ledvin (chronic kidney disease – CKD), které mají své přesné definice na základě klinických i laboratorních nálezů. Ne vždy je však zřejmé, zda jde o AKI nebo o nepoznané CKD, v takovém případě je nutné pátrat po anamnestických údajích (déletrvající hypertenze, diabetes mellitus, dědičná onemocnění ledvin v rodině), zjistit starší laboratorní nálezy a pátrat po tzv. orgánových stigmatech CKD (např. svráštění ledvin, známky sekundárního hyperparatyreoidizmu, anémie). Jsou-li tyto známky přítomny, podporují diagnózu CKD. Léčebný postup pak spočívá v přípravě nemocného k náhradě funkce ledvin (hemodialýza, peritoneální dialýza nebo transplantace ledviny), případně v konzervativní léčbě CKD (v případě méně pokročilého nálezu nebo nesouhlasu nemocného s náhradou funkce ledvin). Naopak nejsou-li známky CKD, je nutné přepokládat AKI, což je principiálně reverzibilní stav.
POZOR
Základní nefrologické vyšetření zahrnuje:
- anamnézu,
- klinické vyšetření,
- základní biochemické a hematologické vyšetření,
- vyšetření moči a sedimentu,
- zobrazovací vyšetření (nejčastěji ultrazvukem, event. CT či MR).
Podle potřeby může být nutné doplnit některá další vyšetření (imunologie, sérologie, atp.).
Akutní poškození ledvin je dle iniciativy KDIGO (Kidney disease: improving global outcomes) definováno splněním jedné z následujících podmínek [1 – 4]:
- absolutní vzestup sérového kreatininu o více než 26,5 µmol/l,
- ≥ 1,5násobný vzestup kreatininu oproti výchozí hodnotě, která je známá nebo předpokládaná za předchozích 7 dní,
- diuréza < 0,5 ml/kg/h po dobu 6 hod.
Jde o akutně vzniklé zhoršení renálních funkcí, které trvá zpravidla v řádu dní, může se rozvinout až v selhání ledvin a v principu je reverzibilní. Hlavním symptomem je pokles diurézy (oligurie – výdej moči pod 500 ml/den, resp. anurie – pod 100 ml/den). Nicméně až ve 30 % případů probíhá AKI pod obrazem normourie nebo až polyurie, jediným laboratorním nálezem je pak vzestup dusíkatých katabolitů (urea, kreatinin).
Uvádění dalších definic AKI jako AKIN nebo RIFLE by přesáhlo záměr tohoto textu, v případě zájmu je lze snadno dohledat.
Epidemiologie
AKI postihuje cca 5 % všech hospitalizovaných pacientů. U pacientů léčených na jednotkách intenzívní péče je prevalence AKI vyšší (cca 33 %). Jde o jeden z nejčastějších důvodů konzultace nefrologa nebo internisty v nemocnici [2–4].
Didakticky se rozdělují příčiny AKI na prerenální, intrarenální a postrenální. Hranice mezi nimi však nejsou zcela ostré a ne vždy lze příčinu jednoznačně identifikovat, např. při déletrvajícím prerenálním inzultu může dojít k akutní tubulární nekróze (intrarenální charakter poškození) [1–4].
Prerenální příčiny AKI jsou nejčastější (cca 60 %). Nejčastějšími vyvolávajícími momenty nebo rizikovými faktory jsou dehydratace a/ nebo pokles cirkulujícího objemu, snížení minutového srdečního vývoje, systémová vazodilatace (např. septický šok), vazokonstrikce renálních tepen – buď zprostředkovaná cytokiny, nebo při hepatorenálním syndromu.
Při prerenálním poškození ledvin jsou zpočátku tubulární a glomerulární struktury intaktní, příčinou snížení nebo ztráty renální funkce je snížená efektivní perfuze ledvin. Snížení efektivního cirkulujícího objemu vede k aktivaci systému renin-angiotenzin-aldosteron a vyplavení katecholaminů a syntetický analog ADH. Tyto hormonální kontraregulační mechanizmy působí pokles natriurézy a vzestup močové osmolality. Častým klinickým problémem je, že někteří rizikoví nemocní s prerenálním poškozením ledvin (např. s chronickým srdečním selháním, jaterní cirhózou nebo nefrotickým syndromem) jeví známky celkové hyperhydratace, ale ve skutečnosti u nich je intravaskulární volum snížen. Pokud jsou v takové situaci podána diuretika, dochází k dalšímu prohloubení intravaskulární volumové deplece a hrozí přechod v intrarenální poškození ledvin (tubulární nekróza). Při včasném zvrácení vyvolávající příčiny je prerenální poškození ledvin reverzibilní [2 – 4].
Intrarenální AKI je méně časté (cca 35 % případů AKI). Příčiny intrarenálního AKI lze rozdělit do čtyř základních kategorií:
- tubulotoxické poškození ledvin, např. ischemické etiologie, postmedikamentózní, kontrastová nefropatie po aplikaci RTG kontrastní látky, pigmentová nefropatie (hemolýza, rhabdmyolýza), tubulární okluze, např. při mnohočetném myelomu nebo urátové nefropatii atd.,
- makrovaskulární poškození při vaskulitidě, ateroembolické chorobě ledvin, tromboembolické nemoci,
- mikrovaskulární poškození, např. vlivem akutní nebo rychle progredující glomerulonefritidy,
- akutní tubulointersticiální nefritida, tj. imunitní (alergická) reakce na léky či jiné inzulty.
Morfologickým korelátem AKI jsou obstrukce tubulů epitelovými buňkami odloučenými z bazální membrány. Příčinou tubulární nekrózy je hypoxie vyvolaná hypoperfuzí ledvin a poruchou cévních regulačních mechanizmů.
Postrenální příčiny AKI jsou nejméně časté. Vyvolávajícími mechanizmy mohou být vrozené vady v oblasti uropoetického traktu, získané obstrukce, maligní tumory, gynekologická onemocnění a operační komplikace, malpozice močového katetru nebo např. anticholinergních farmak, především při preexistující hyperplazii prostaty.
POZOR
Při akutním zhoršení renálních funkcí je na prvním místě nutné vyloučit ultrazvukovým vyšetření subrenální obstrukci!
Klinický obraz
Klinický obraz AKI je poměrně nespecifický. Zpravidla – především v iniciální fázi – dominují symptomy onemocnění, jež vedlo k AKI. Jak již bylo uvedeno, nemusí být oligurie i anurie vždy vyjádřena, proto je nutné v rizikových situacích (změna medikace, akcentace diuretické léčby, vyšetření s kontrastní látkou) monitorovat renální funkce (sérový kreatinin, vyšetření moči, sledování příjmu a výdeje tekutin). Ve fázi manifestního poškození ledvin (ať už s oligoanurickým či non-oligurickým průběhem) dochází k poklesu glomerulární filtrace a vzestupu dusíkatých katabolitů v séru. Je riziko hyperhydratace, levostranného srdečního selhání s plicním edémem, edémem mozku, hyperkalemie, metabolické acidózy a uremie. V diuretické (polyurické) fázi dochází k reparaci renálních struktur, přičemž však existuje riziko dehydratace a minerálové dysbalance (především hypokalmie, hyponatrmie) [1–4].
AKI může vést k vzniku celé řady orgánových komplikací:
- plíce – plicní edém, pleurální výpotek, šoková plíce při multiorgánovém selhání,
- kardiovaskulární – perikarditida, poruchy srdečního rytmu při minerálové dysbalanci, hypertenze,
- gastrointestinální – vředová choroba, krvácení do zažívacího traktu,
- centrální nervová soustava – encefalopatie, křeče, poruchy vědomí,
- anémie, krvácivost,
- infekce.
Diferenciálně diagnosticky je nutné zvažovat především funkční oligurii a nerozpoznané CKD. V tab. 1 jsou uvedeny některé anamnestické údaje a klinické a paraklinické nálezy, jež mohou podpořit zvažovanou diagnózu.
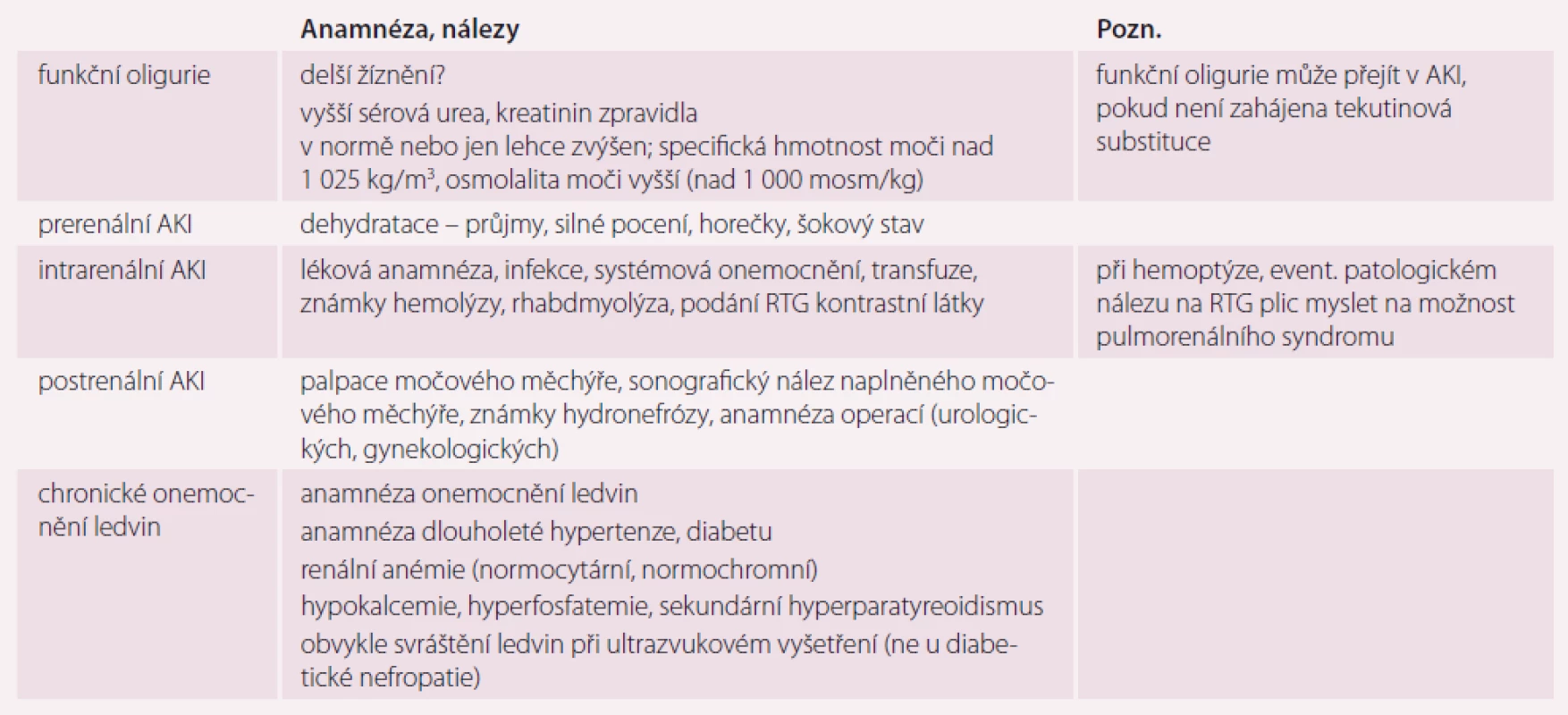
Laboratorní a pomocná vyšetření
Předpokladem je pečlivý odběr anamnézy, klinické vyšetření a údaj o příjmu a výdeji tekutin:
- základní biochemická vyšetření, kompletní mineralogram vč. vápníku a fosforu, močovina, kreatinin, kyselina močová, laktátdehydrogenáza (LDH; vzestup mj. při trombotické mikroangiopatii), kreatinkináza (CK), myoglobin, elektroforéza bílkovin,
- krevní obraz vč. schistocytů (při podezření na trombotickou mikroangiopatii),
- moč včetně sedimentu (M+S),
- event. frakční exkrece z nativní moči – umožňuje diferencovat mezi prerenálním a intrarenálním poškozením, při prerenáním AKI je FE(Na) pod 1 %, při intrarenálním nad 1 %,
- sonografie ledvin a močového měchýře, event. včetně duplexního sona renálních tepen,
- event. renální biopsie při podezření na rychle progredující glomerulonefritidu nebo při jiných neobjasněných patologických stavech s aktivním močovým nálezem.
Terapie
Terapie spočívá v léčbě základního onemocnění, které vedlo k AKI, v symptomatické léčbě a případně v náhradě funkce ledvin [5,6].
V první řadě jde například o léčbu šoku, substituci krevními deriváty při akutní posthemoragické anémii, vysazení nefrotoxických léčiv, zajištění derivace moči apod. Pokud je nevyhnutelné podávat nefrotoxická léčiva (např. aminoglykosidová antibiotika), monitorujeme jejich hladiny.
Ve většině případů se podaří AKI zvládnout adekvátní náhradou tekutin, upřednostňujeme krystaloidy. Místo fyziologického roztoku, který obsahuje vysoké množství chloridů s toxickým vlivem na funkci ledvin, užíváme raději tzv. balancované roztoky (např. Ringer laktát nebo Plasmalyte). Hydroxyetylškroby (HAES) se již podle doporučení výboru Evropské agentury pro léčivé přípravky (EMA) nemají používat kvůli zjištění, že pacienti s těžkou sepsí léčení HAES byli vystaveni většímu riziku poškození ledvin vyžadujícího dialýzu. Tekutiny doplňujeme za monitorace diurézy, extrarenálních ztrát a centrálního žilního tlaku, dále sledujeme v pravidelných intervalech (1–2× denně) mineralogram [5–7]. Energetický příjem pacienta by se měl pohybovat mezi 20 a 30 kcal/kg/den, doporučené cílové hodnoty glykemie se pohybují v rozmezí 6,1–8,3 mmol/l [6–9]. Vzhledem k bezproblémové dostupnosti dialýzy v našich podmínkách neomezujeme příjem bílkovin pacienta, abychom tím hypoteticky oddálili potřebu dialýzy. Pro pacienta je výhodnější enterální výživa, parenterální výživu indikujeme při nemožnosti enterální nutrice. Dříve paušálně podávaný furosemid indikujeme jen v případě přítomnosti hypervolemie a pozitivní tekutinové bilance, spíše však v těchto případech zvažujeme dialýzu. Podávání tzv. renálních dávek dopaminu s představou zlepšení perfuze ledvin je nepodložené. Dialýza je indikována při anurii, hyperkalemii > 6,5 mmol/l, těžké, jinak nezvládnutelné metabolické acidóze, hyperhydratatci s plicním edémem, symptomech uremie (perikarditida, neurologická či gastrointestinální symptomatologie). V principu lze užít dvě základní modality – intermitentní hemodialýzu (IHD) a kontinuální náhradu funkce ledvin (CRRT). HD volíme u hemodynamicky stabilizovaných pacientů a u těch, kde je zapotřebí rychle korigovat minerálovou poruchu (hyperkalemii, hyperkalcemii). I CRRT užíváme u hemodynamicky nestabilních pacientů, např. v šokovém stavu, při srdečním selhání, u kterých by mohl být výhodný i předpokládaný imunomodulační efekt procedury (odstranění mediátorů zánětu) [6 – 9].
Prognóza akutního selhání ledvin
Prognóza AKI závisí na zvládnutí základní příčiny onemocnění, z výše uvedeného přehledu je však zřejmé, že se vždy jedná o závažnou a potenciálně i život ohrožující komplikaci. I přes značné pokroky ve znalostech patogeneze AKI jsou naše současné terapeutické možnosti poněkud omezené. Pacienti, kteří prodělali AKI, by měli být sledováni nefrologem mimo jiné proto, že jsou tito pacienti ohroženi rozvojem CKD, resp. až desetinásobně vyšším rizikem rozvoje terminální fáze CKD – renálního selhání [9].
Doručeno do redakce: 4. 12. 2017
Přijato po recenzi: 11. 12. 2017
MUDr. Jan Vachek
www.vfn.cz
jan.vachek@gmail.com
Zdroje
1. Mehta RL, Kellum JA, Shah SV et al. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit Care 2007; 11(2): R31. doi: 10.1186/ cc5713.
2. Bellomo R, Ronco C, Kellum JA et al. Acute renal failure – definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care 2004; 8(4): R204 – R212. doi: 10.1186/ cc2872.
3. Hsu CY, McCulloch CE, Fan D et al. Community-based incidence of acute renal failure. Kidney Int 2007; 72(2): 208 – 212. doi: 10.1038/ sj.ki.5002297.
4. Levey AS, Eckardt KU, Tsukamoto Y et al. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2005; 67(6): 2089 – 2100. doi: 10.1111/ j.1523-1755.2005.00365.x.
5. Prescott AM, Lewington A, O'Donoghue D. Acute kidney injury: top ten tips. Clin Med 2012; 12(4): 328 – 332.
6. Druml W. Acute renal failure is not a "cute" renal failure! Intensive Care Med 2004; 30(10): 1886 – 1890. doi: 10.1007/ s00134-004-2344-z.
7. Palevsky PM, Zhang JH, O'Connor TZ et al. Intensity of renal support in critically ill patients with acute kidney injury. N Engl J Med 2008; 359(1): 7 – 20. doi: 10.1056/ NEJMoa0802639.
8. Bellomo R, Cass A, Cole L et al. Intensity of continuous renal-replacement therapy in critically ill patients. N Engl J Med 2009; 361(17): 1627 – 1638. doi: 10.1056/ NEJMoa0902413.
9. Thakar CV, Christianson A, Himmelfarb J et al. Acute kidney injury episodes and chronic kidney disease risk in diabetes mellitus. Clin J Am Soc Nephrol 2011; 6(11): 2567 – 2572. doi: 10.2215/ CJN.01120211.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2017 Číslo 4
-
Všechny články tohoto čísla
- Antiarytmická léčba u fibrilace síní
- Upstream terapie u fibrilace síní, co nového?
- Úloha intrakardiální echokardiografie při katetrizační ablaci poruch srdečního rytmu
- Moderní pohled na elektrickou kardioverzi fibrilace síní
- Náhlá srdeční smrt a její diagnostika
- Ischemie a infarkt myokardu při poruchách nitrokomorového vedení na elektrokardiogramu
- Význam nových parametrů kontraktility a tepové práce pro hodnocení srdeční funkce a prognózy
- Kvalita života pacientů s dlouhodobou mechanickou srdeční podporou
- Moderní farmakologická léčba diabetes mellitus 2. typu
- Revmatoidní artritida pro kardiologa
- Akutní selhání ledvin
- Súčasné fixné antihypertenzné liekové dvojkombinácie v Slovenskej republike
- MUDr. Pavel Jerie se dožívá 90 let
- Srdíčkáři na Pálavě aneb V. setkání osob žijících s transplantovaným srdcem
- První Kurz srdečního selhání v Brně
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Ischemie a infarkt myokardu při poruchách nitrokomorového vedení na elektrokardiogramu
- Súčasné fixné antihypertenzné liekové dvojkombinácie v Slovenskej republike
- Moderní farmakologická léčba diabetes mellitus 2. typu
- Akutní selhání ledvin
