Home monitoring nemocných s fibrilacemi síní
Home monitoring of patients with atrial fibrillation
Home Monitoring is an advanced telemonitoring system used in clinical cardiology practice in the Czech Republic during ambulatory monitoring of patients with implantable devices. The percentage of patients with atrial fibrillation, which can be both basic and complicating disease, is increasing in this population. The presence of some kinds of implantable devices offers the possibility of a remote monitoring use in more efficient management of patients with atrial fibrillation. Through Home Monitoring system health care can be individualized, asymptomatic clinical events can be detected earlier and thus prevent their negative impacts.
Keywords:
home monitoring – telemonitoring – atrial fibrillation – heart failure
Autoři:
O. Ošmera; A. Bulava
Působiště autorů:
Kardiocentrum Nemocnice České Budějovice, a. s.
1; Zdravotně sociální fakulta, Jihočeská univerzita v Českých Budějovicích
2
Vyšlo v časopise:
Kardiol Rev Int Med 2011, 13(3): 167-173
Souhrn
Home Monitoring je pokročilým telemonitoringovým systémem užívaným v klinické kardiologické praxi v ČR při ambulantním sledování pacientů s implantabilními přístroji. V této populaci je narůstající podíl pacientů s fibrilací síní, která může být jak základním, tak i komplikujícím onemocněním. Přítomnost některých implantabilních přístrojů skýtá možnost využití dálkového monitorování v efektivnějším managementu pacientů s fibrilací síní. Prostřednictvím systému Home Monitoring lze individualizovat péči, časněji zaznamenávat i asymptomatické klinické události a předcházet jejich negativním dopadům.
Klíčová slova:
home monitoring – telemonitoring – fibrilace síní – srdeční selhání
Úvod
Telemonitoring je telemedicínská služba, jejímž cílem je sledování zdravotního stavu pacientů na dálku [1]. Údaje lze shromažďovat buď automaticky pomocí osobních zařízení pro sledování zdraví, nebo za aktivní spolupráce pacienta a lze je po jejich zpracování a sdělení příslušným zdravotníkům použít k optimalizaci sledovacích a léčebných protokolů pacienta.
Systémy pro telemonitoring v kardiologii jsou v současné době již široce používány v klinické praxi při sledování pacientů s implantovanými kardiostimulátory (peacemakery – PM), implantabilními kardiovertery-defibrilátory (ICD) a systémy pro srdeční resynchronizační léčbu (CRT, event. v kombinaci s funkcí ICD–CRT/D). Implantabilní přístroje mají čtyři funkce: detekce arytmií, léčba některých arytmií (antitachykardický pacing – stimulace (ATP), šok, overdrive), kardiostimulace a schopnost uchovávat data (holterovské funkce, záznamy epizod včetně intrakardiálního EKG) [2]. Ve všech případech se jedná o údaje hodnotné pro sledování a léčbu pacientů.
Home Monitoring BIOTRONIK
Home Monitoring (HM) BIOTRONIK se v současnosti jeví jako nejpokročilejší systém pro telemonitoring pacientů s implantovanými přístroji v kardiologii, zároveň je jediným z uvedených systémů, který je používán v současné klinické praxi v České republice. Jedná se o plně automatický systém, který zasílá kódované zprávy přes GSM mobilní síť do HM Service Center v Berlíně, kde jsou zprávy dekódovány a přes zabezpečené webové rozhraní dostupné během minut ošetřujícímu lékaři, kterému je rovněž umožněno nastavení parametrů pro hlášení událostí prostřednictvím SMS, faxu nebo e-mailu [3,4].
Podle konsenzu odborníků Heart Rhythm Society/European Heart Rhythm Association (HRS/EHRA) je pro pacienty s kardiovaskulárními implantabilními elektronickými přístroji (CIED) doporučována osobní kontrola alespoň jednou ročně. Vzdálený monitoring může potom nahradit další kontroly, pokud je zdravotní stav pacienta stabilní, nepředpokládá se programování přístroje, neblíží se termín elektivní výměny přístroje pro depleci zdroje nebo není předpokládán přínos z časné detekce změny zdravotního stavu či nedošlo k malfunkci přístroje. To dovoluje optimalizaci léčebných postupů a využití prostředků zdravotní péče [5,6].
Fibrilace síní
Fibrilace síní (FS) je nejčastější supraventrikulární arytmií charakterizovanou rychlou nekoordinovanou akcí srdečních síní. Bývá uváděna celková incidence 1–6 %, s prevalencí 0,1 % u osob mladších než 55 let, 3,8 % u osob 60letých a starších a 10 % u osob 80letých a starších. Předpokládá se nárůst počtu osob s FS až na dvojnásobek do roku 2050 [7]. Frekventovanější je výskyt této arytmie u mužů všech věkových skupin. V 10–15 % případů není FS spjata s dalším onemocněním („lone FS“), častěji je ale asociována s organickým postižením srdce (ischemická choroba srdeční (ICHS), srdeční selhání, chlopenní vady, kardiomyopatie) nebo jinými komorbiditami (hypertenze, diabetes mellitus) [8]. U pacientů se srdečním selháním je výskyt FS závislý na jeho stupni: kolísá přibližně od 5 % při NYHA I až téměř k 50 % při NYHA IV.
U pacientů s FS je udávána přibližně dvojnásobná mortalita při srovnání s pacienty se sinusovým rytmem. Hlavní příčinou zvýšené morbidity i mortality při FS je vyšší výskyt tromboembolických příhod. Výskyt ischemických iktů je u pacientů s FS bez koincidence chlopenních vad průměrně 5 % za rok, což je 2–7krát vyšší počet než u pacientů se sinusovým rytmem, u pacientů s FS a chlopenní vadou může narůst riziko iktu až 17krát [9]. Liší se podle přítomnosti dalších rizikových faktorů a narůstá exponenciálně s věkem. 20 % všech ischemických mozkových příhod má příčinu ve FS a u 40 % pacientů s FS lze prokázat klinicky němé mozkové infarkty. U pacientů s FS byl zjištěn dvojnásobný výskyt kognitivní dysfunkce nebo demence oproti populaci bez FS [10]. Mortalita závisí také na přítomnosti kardiálního onemocnění. Zvýšená je však i mortalita u idiopatické arytmie [11,12].
Tato zjištění vypovídají o klinické, prognostické a socioekonomické závažnosti této frekventní arytmie v populaci. Nepochybně se jedná o velký klinický problém v důsledku měnící se epidemiologie FS, ale také pro samotný negativní dopad na mortalitu a morbiditu pacientů s FS.
FS lze klasifikovat po jejím rozpoznání a prvotní diagnostice dle délky trvání arytmie (a to bez ohledu na symptomy) na:
- paroxyzmální FS: rekurentní epizody arytmie spontánně terminující do sedmi dnů,
- perzistující FS: udržuje se více než sedm dnů nebo trvá kratší dobu, ale vyžaduje kardioverzi (elektrickou či farmakologickou),
- dlouhodobá perzistující FS: trvá déle než jeden rok,
- permanentní FS: kardioverze arytmie proběhla bez úspěchu či o ni vůbec nebyl učiněn pokus.
Klasifikace má význam pro přístup k terapii pacientů s FS, vypovídá částečně o době trvání arytmie, event. o předchozích intervencích ve vztahu k arytmii. Terapie a léčba u pacientů s FS je pak primárně cílená na úlevu od symptomů, zachování nebo vylepšení funkce levé komory srdeční, resp. srdečního výdeje u pacientů se srdečním selháním. Sekundárně je pak zaměřená na redukci mortality a morbidity (zejména iktu) v souvislosti s FS.
FS u pacientů s pacemakery
Incidence výskytu arytmií, zejména pak fibrilace síní, je v populaci nositelů pacemakerů (PM) velmi vysoká. Udávána je četnost přes 50 % v průběhu uplynutí šesti let životnosti přístroje v případě pacientů s poškozením sinusového uzlu. U pacientů trpících AV blokádami je pak incidence přes 20 % [13]. Přítomnost supraventrikulárních tachyarytmií v diagnostice PM (tedy v čítačích a statistikách přístroje) je nezávislým prediktorem celkové mortality, mozkové příhody nebo přítomnosti chronické formy fibrilace síní u pacientů s poškozením funkce sinusového uzlu [14].
Riziko kardioembolizace upravené o známé rizikové faktory pacientů bylo vyčísleno jako 3,1násobné u pacientů s epizodami FS delšími než 24 hod detekovanými implantovaným přístrojem zjištěnými při ambulantních kontrolách [15]. V prospektivní studii TRENDS byl kalkulován nezvýšený poměr rizika iktu v případě paroxyzmů FS kratších než 5,5 hod, ale 2,2násobný v případě paroxyzmů delších při srovnání se skupinou bez FS [16].
V retrospektivně hodnoceném souboru 276 pacientů Varma et al popsali záchyt alespoň jednoho „dne s fibrilací síní“ (mode-switch po více než 20 % dne) u 10,5 %. 79 % z nich mělo pak při arytmii průměrnou komorovou frekvenci vyšší než 80/min [17]. Ve studii Ricciho et al byl hodnocen význam HM při detekci a léčbě fibrilace síní v souboru 166 pacientů, kteří byli sledováni v průměru 16 měsíců. U 42 z nich (26 % souboru) byly detekovány systémem HM epizody fibrilace síní, 78 % z nich bylo vyzváno k časnější kontrole a u 60 % bylo na základě toho intervenováno (změna medikace, kardioverze) [18].
Otázkou tedy je, zda setrvalé monitorování srdečního rytmu může řídit management antikoagulační terapie ve vztahu ke klinickému riziku iktu. A dále pak jaký je zlomový bod pro rozhodnutí o soustavné antikoagulaci ve vztahu k CHADS2 skóre.
FS u pacientů s implantovanými kardiovertery-defibrilátory a systémy pro srdeční resynchronizační terapii
Incidence výskytu FS je udávána 3–4 % za rok u pacientů se srdečním selháním. Montero dokonce udává u pacientů v době implantace kardioverteru-defibrilátoru (ICD) koexistenci jiné arytmie (než pro které byl ICD implantován) u 20–30 % pacientů. Až 45 % těchto pacientů má pak jiné arytmie diagnostikovány do uplynutí 17 měsíců od implantace [19].
Výsledky ze studie ALTITUDE s rozsáhlou kohortou téměř 24 tisíc pacientů se srdeční resynchronizační léčbou (CRT) ukázaly významný nárůst mortality u skupin pacientů s dokumentovanou fibrilací síní. Při srovnání 56 % pacientů bez FS byl v případě pacientů s paroxyzmální formou arytmie v trvání kratší než jeden den (20 % pacientů) poměr rizika 1,25 (1,15–1,35). Při paroxyzmech FS v trvání 1–7 dní (4 % pacientů) bylo pak mortalitní riziko zvýšeno na 1,49 (1,29–1,72), tedy dokonce více než u skupiny 20 % pacientů s perzistentní formou FS, kde dosahovalo „jen“ 1,46 (1,35–1,57) při srovnání se skupinou bez výskytu FS [20].
Neadekvátní terapie ICD je udávána v širokém rozpětí 8−41 %, v průměru 16 % [21], a může mít příčiny jak klinické (nejčastěji nesprávnou diskriminaci supraventrikulární tachykardie při epizodách fibrilace síní s rychlou komorovou odpovědí nebo např. T-wave oversensingu), tak technické (poruchu integrity, dislokaci elektrody nebo elektromagnetickou interferenci). V současném trendu narůstá také počet profylaktických indikací pro implantace ICD, což je ovšem spojeno s nižší mírou adekvátní šokové terapie [22]. Rovněž HM může být účinným nástrojem k detekci udělených i přerušených neadekvátních terapií, a může tak přispět k jejich eliminaci [23,24].
Nedostatečnou kontrolu komorové frekvence při epizodách FS měla jedna třetina pacientů s biventrikulárním ICD. Jejich průměrná komorová odpověď při běžící arytmii byla vyšší než 80/min a maximální překračovala 110/min ve 34 % případů z 443 pacientů [25].
Přínos systému Home Monitoring u pacientů s FS
Standardní forma ambulantních kontrol u pacientů s FS je limitující v možnosti omezeného počtu plánovaných návštěv pacienta ve specializovaných ambulancích. Při těchto vyšetřeních jsou zpětně analyzovány statistiky v paměti implantovaných přístrojů včetně čítačů arytmií a eventuálních záznamů intrakardiálního EKG ke zhodnocení typu arytmie, správnosti detekce, délky trvání nebo komorové odpovědi při běžící arytmii.
Nově diagnostikovaná FS
U asymptomatických nebo nízce symptomatických pacientů bez dosud dokumentované FS je diagnostika arytmie prostřednictvím HM možná v jednodutinových přístrojích nepřímo (komorová odpověď, tachykardické epizody, nepravidelnost RR intervalů, event. záznam intrakardiálního EKG). Spolehlivá je pak diagnostika v dvoudutinovém přístroji díky kombinaci ukazatelů (síňové vs komorové frekvence, mode-switch přístroje, atrioventrikulární synchronie, záznam intrakardiálního EKG aj.). FS pak u těchto pacientů může signifikantně zvyšovat riziko iktu, pokud nemají zavedenou antikoagulační léčbu z jiné indikace (obr. 1).
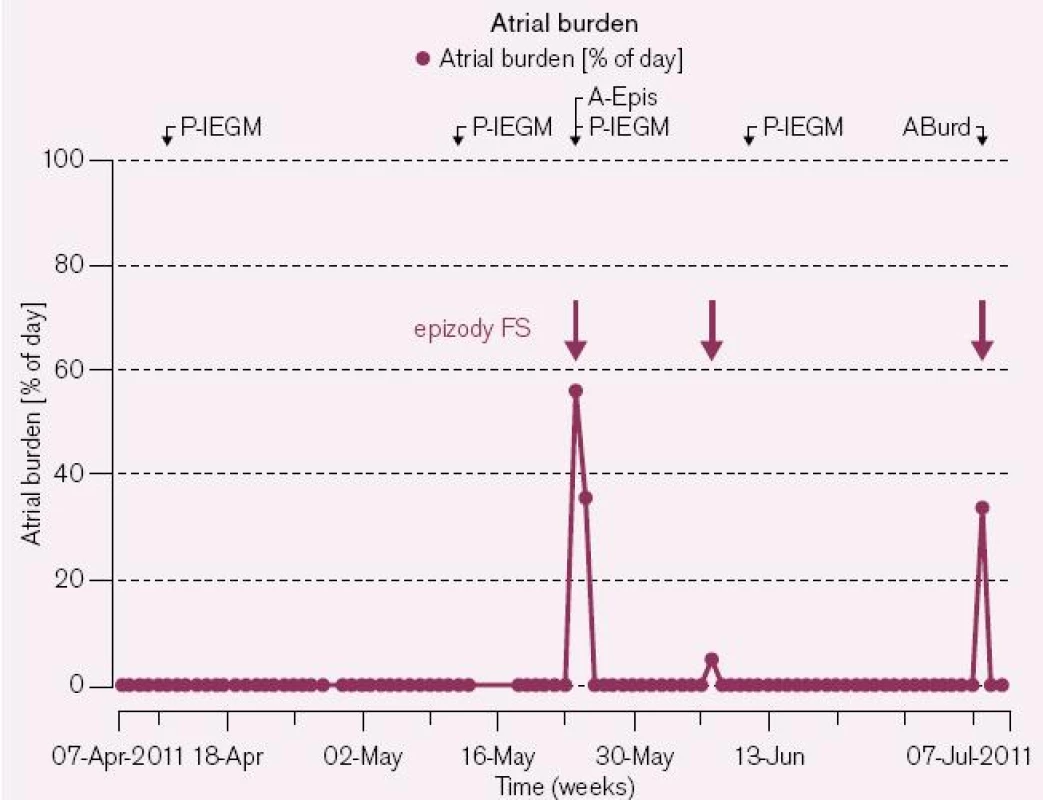
Detekce asymptomatických epizod FS
Pozdní detekce asymptomatických epizod FS při plánovaných kontrolách pacienta neumožňuje promptní a cílený terapeutický zásah. Efektivní farmakoterapie nebo časná elektrická kardioverze ke kontrole rytmu, ale i účinná bradykardizující medikace při kontrole srdeční frekvence mohou zabránit vzniku nežádoucích klinických událostí včetně vzniku perzistentních a permanentních forem arytmie.
Kontrola rytmu a kontrola frekvence
Systém HM umožňuje zhodnotit den ode dne efekt nově indikované nebo změněné antiarytmické terapie u pacientů s paroxyzmální formou FS. Lze posoudit negativní, nulový nebo částečný efekt léčby či úplnou eliminaci arytmie. V případě provedení elektrické kardioverze je recidiva FS odhalena časně v horizontu 24 hod. U permanentní FS je možné kontinuální monitorování srdeční frekvence s vyhodnocením průměrných hodnot celodenních, nočních klidových, ale i maximální komorové odpovědi včetně počtu epizod, kdy byly hodnoty (dle nastavení holterovských funkcí PM) komorové odpovědi překročeny. Některé z těchto hodnot jsou při standardní formě plánovaných kontrol zavzaty do celkových součtů statistik a tímto přestávají být některá data při zpětné analýze použitelná pro klinické účely a korekci farmakoterapie. Ať tedy zvolíme léčebnou strategii ve smyslu kontroly srdečního rytmu či kontroly frekvence, monitorovat lze pomocí telemetrického systému HM obojí (obr. 2a, b, c).



Monitorace pacientů po radiofrekvenční katetrové ablaci pro fibrilaci síní
Objektivní míra úspěšnosti nefarmakologické léčby fibrilace síní metodou radiofrekvenční katetrové ablace je nepřímo dána způsobem následné monitorace pacientů po samotném výkonu. Tedy dokonalejší způsoby následného monitorování relativně snižují podíl pacientů bez zjištěné recidivy arytmie. Kontinuálním monitorováním systémem HM lze u pacientů s implantovanými přístroji nejen prokazatelně vyhodnocovat období bez arytmie, ale v případě recidivy včasně korigovat antiarytmickou léčbu a vést bezpečnou strategii antikoagulační terapie.
Přínos systému Home Monitoring u pacientů s FS a srdečním selháním
Negativní dopady FS na klinický stav pacientů s chronickým srdečním selháním mají několik příčin. Dochází k hemodynamickému propadu při ztrátě atrioventrikulární synchronie a ztrátě síňového příspěvku k plnění dysfunkční komory. Nepravidelná a často nefyziologicky rychlá komorová odpověď dále snižuje srdeční výdej a může způsobovat významný pokles resynchronizace u CRT přístrojů. V neposlední řadě je zde opět riziko trombembolizmu. Důsledkem je dekompenzace a progrese kardiálního selhávání s nutností opakovaných hospitalizací a zvýšenou mortalitou [26].
Detekce ztráty resynchronizace CRT systémů
Nepravidelná komorová odpověď bez koordinace s aktivitou síňovou při FS s nežádoucím uplatněním vlastního převodu na komory je spolu s komorovou extrasystolií nejčastější příčinou ztráty resynchronizace u biventrikulárních kardiostimulátorů. Ztráta může být úplná v případě rychlejší komorové odpovědi, kdy je vlastní aktivita snímána (senzována) jak v pravé, tak v levé komoře, nebo je částečná v případě poněkud pomalejší komorové odpovědi, kdy se intermitentně biventrikulární stimulace uplatňuje a střídá se s vlastním rytmem nebo kardiostimulační systém k senzovaným vlastním stahům pravé komory „synchronně stimuluje“ komoru levou.
Úplnou i částečnou ztrátu biventrikulární stimulace lze systémem HM dobře detekovat a vyhodnotit – podobně jako z čítačů a statistik samotného přístroje při interogaci v ambulanci, včetně procentuálního podílu z celkové aktivity přístroje. V případě korekce medikace však lze prostřednictvím HM posoudit jak trend narůstající biventrikulární stimulace při zpomalení komorové odpovědi nebo její plné obnovení při nastolení sinusového rytmu, tak neúspěch této léčby, event. další progrese nepříznivého stavu (obr. 3).
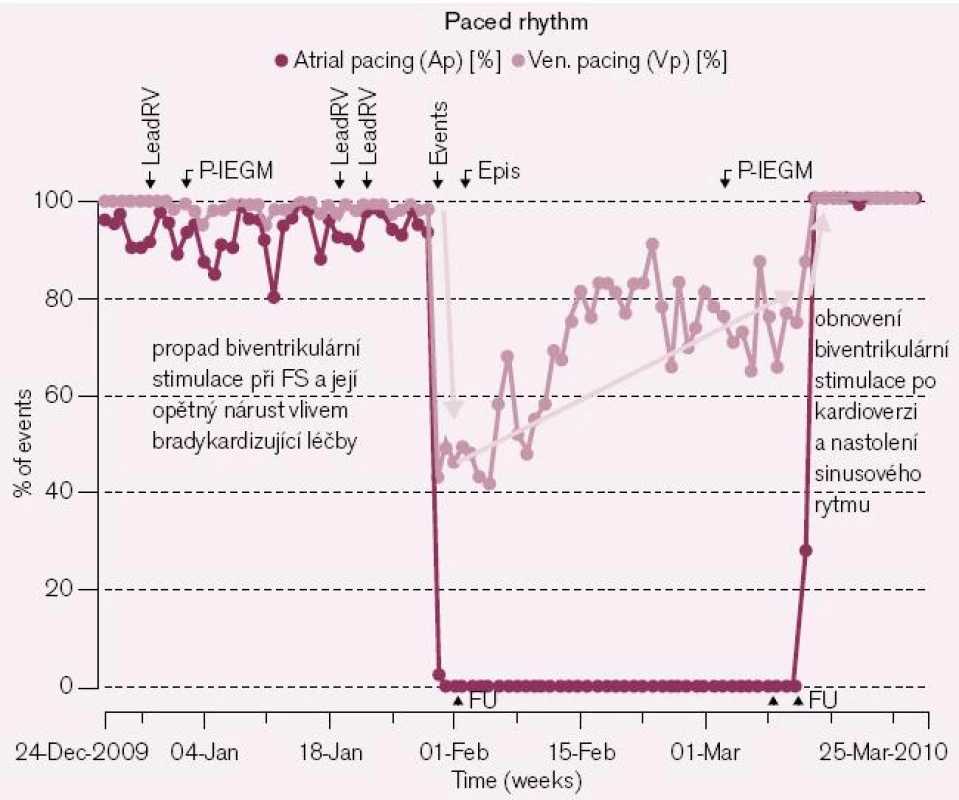
Neadekvátní terapie ICD
Již výše byly zmíněny četnost neadekvátní terapie ICD v průměru 16 % [21] a její příčiny – nejčastěji nesprávná diskriminace supraventrikulární tachykardie při epizodách fibrilace síní s rychlou komorovou odpovědí. Systém HM může být účinným nástrojem k detekci udělených i přerušených neadekvátních terapií, a může tak přispět k jejich eliminaci. V případě ICD terapií je vždy získávána zpráva z čítačů arytmií, počtu udělených ATP a šokových terapií, event. počtu přerušených terapií. Současně skýtá systém možnost přenosu části intrakardiálního EKG (tedy elektrické aktivity snímané přímo implantovanou elektrodou přístroje) z jedné nebo i více epizod se záchytem rytmu před epizodou, její detekcí a rytmem po přístrojem vyhodnoceném skončení arytmie. To umožňuje zhodnocení adekvátnosti udělené terapie jednodutinových ICD. V případě dvoudutinových a biventrikulárních systémů je pak se znalostí síňového rytmu diagnostika ještě snazší (obr. 4).
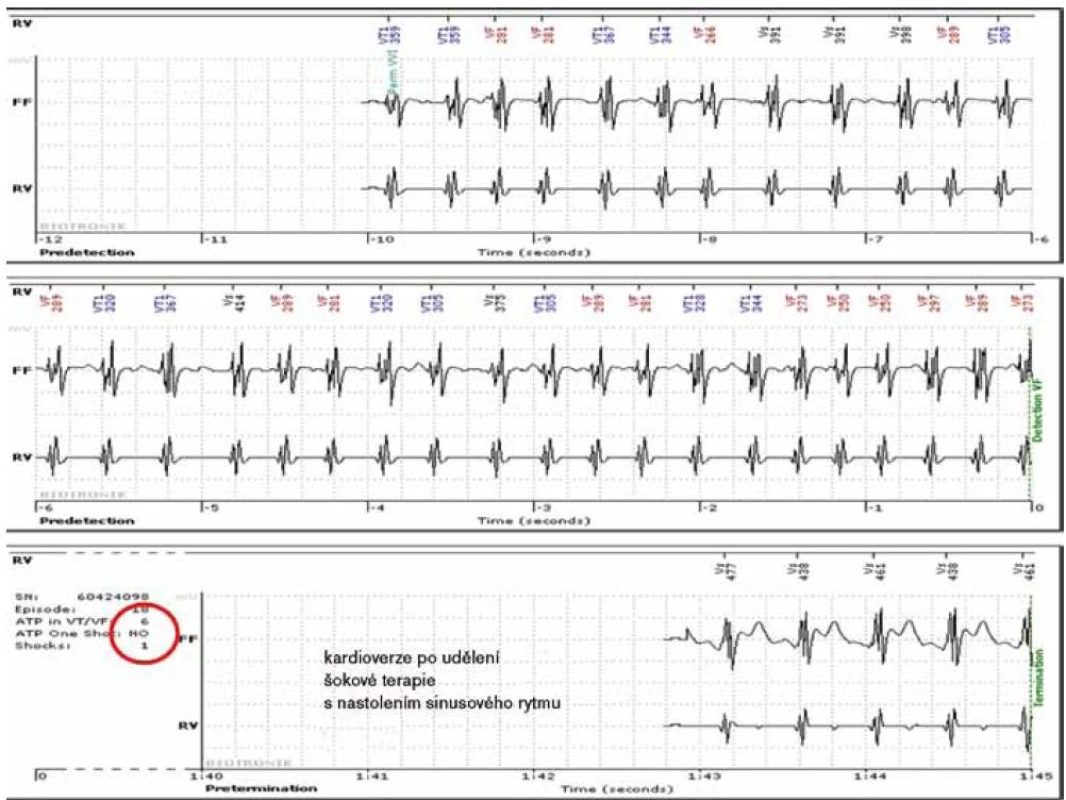
Podstatným přínosem jsou opět kontinuální monitorace pacienta po přeprogramování ICD systému v parametrech detekce a udělování terapií nebo případné korekce medikace. HM systémem lze zachytit také některé komorové arytmie pomalu akcelerující do pásma pro detekci tachykardií diskriminovaných ICD přístrojem někdy falešně jako supraventrikulární pro nesplnění náhlého začátku, a proto bez udělení ICD terapie.
Pacienti s neadekvátními šokovými terapiemi při fibrilaci síní s rychlou komorovou odpovědí často nepřistoupí z vlastní iniciativy k časnější kontrole v kardiocentru nebo u ambulantního kardiologa pro jinak subjektivně tolerovanou arytmii a uspokojivý zdravotní stav. Data z telemonitoringového systému jsou v tomto případě nepostradatelným prostředníkem v časném kontaktu pacienta lékařem a provedení mimořádné kontroly s patřičnou intervencí. Opakované šokové terapie jsou totiž nejen traumatizující, ale také zkracují životnost baterie přístroje a neadekvátní terapie ICD mohou být i samotným spouštěčem maligní arytmie.
Progrese srdečního selhání a častější hospitalizace při FS
Existují zatím pouze nespecifické markery srdečního selhání a bez klinického, event. zobrazovacích vyšetření je zatím spolehlivá predikce blížící se dekompenzace nemožná. Kombinace těchto markerů nicméně může svědčit pro kardiální dekompenzaci a v případě koincidence se setrvalým paroxyzmem, event. nově vzniklou FS je klinická kontrola pacienta indikovaná.
Ačkoli systém HM neobsahuje spolehlivý prediktor srdečního selhávání, umožňuje detekci nárůstu průměrné komorové frekvence, nárůstu průměrné noční klidové komorové frekvence, pokles aktivity pacienta v trendu a současně záchyt FS jako příčiny horšení klinického stavu s případnou ztrátou srdeční resynchronizace. Vyhodnocením kombinací těchto markerů lze v relevantních případech kontaktem pacienta a mimořádnou klinickou kontrolou předejít významnějšímu zhoršení s případnou nutností hospitalizace.
Diskuze
V budoucnu lze vzhledem k současné epidemiologii FS a soudobému negativnímu dopadu na mortalitu a morbiditu pacientů s FS předpokládat:
- nárůst počtu pacientů s FS absolutně i v populacích s implantabilními přístroji (PM, ICD, CRT/D),
- další snahu o vývoj nových antiarytmik a další rozvoj nefarmakologických strategií v léčbě FS,
- snahu o pokroky v antikoagulační terapii vývojem nových farmak s bezpečnějším terapeutickým profilem,
- diskuzi o strategiích kontroly rytmu vs kontroly frekvence,
- možné snížení relativní morbidity a mortality v populaci s FS zlepšením managementu pacientů s FS.
V populaci pacientů s implantabilními přístroji v kardiologii trpících FS mohou být využity technologie telemonitoringu, ověřené v klinické kardiologické praxi. Dokáží podle dostupných studií nejen snížit pracovní zátěž a zefektivnit využití prostředků zdravotní péče, ale také jejich redistribuci ve prospěch účelného zaměření na vážné a relevantní klinické události.
Využití telemonitoringového systému může částečně řešit výše zmíněné nepříznivé trendy v epidemiologii pacientů s FS, ale také zprostředkovat dosažení vytyčených cílů k jejich zvládnutí. Se systémem Home Monitoring BIOTRONIK u pacientů s fibrilací síní je možné:
dosáhnout změny přístupu k léčbě FS ve smyslu snahy o kontrolu rytmu v indikovaných případech (a to jak nefarmakologickými způsoby léčby, tak užitím nových antiarytmik) a s tím související nutnost následné monitorace pacientů,
cílení léčby do časných stadií arytmie k prevenci remodelace a vzniku perzistentních a permanentních forem FS, a tedy potřeba časného záchytu asymptomatických a nízce symptomatických forem,
posun od managementu implantabilních přístrojů k managementu onemocnění (FS, srdečního selhání a jejich kombinace),
individualizace následné ambulantní péče, predikce a prevence nepříznivých klinických událostí v souvislosti s FS při optimalizaci pracovních postupů, plánovaných a mimořádných kontrol a zefektivnění ambulantní péče.
Závěr
Telemonitoring a kontroly na dálku se jeví v budoucnu jako pravděpodobný standard péče o pacienty s implantovanými kardiostimulátory, ICD a systémy pro srdeční resynchronizační léčbu, ale nepochybně i pro další chronicky nemocné, protože mohou nabídnout efektivnější využití zdrojů, zajistit větší bezpečnost a kvalitu života pro pacienty při současném snížení nákladů na péči.
Dosavadní studie ukázaly dostatečnou spolehlivost současných monitorovacích systémů a analýzy kalkulovaných nákladů předpokládají prospěch z jejich použití, s jistými rozdíly v závislosti na systému poskytování zdravotní péče, nákladech a úhradách za péči a jistě geografických charakteristikách. V případě péče o pacienty s fibrilací síní narůstají možnosti využití systému HM k prospěchu jak pacientů, tak systému poskytování zdravotní péče.
Očekávané jsou výsledky dalších probíhajících studií s cílem zlepšit kvalitu života chronicky nemocných, zajistit jejich vyšší bezpečnost, ovlivnit jejich prognózu, ale také dále vyjednávat o úhradách za telemedicínské služby s plátci zdravotní péče.
Doručeno do redakce 8. 7. 2011
Přijato po recenzi 2. 8. 2011
MUDr. Ondřej Ošmera1
doc. MUDr. Mgr. Alan Bulava, Ph.D.1,2
1Kardiocentrum Nemocnice České Budějovice, a. s.
2Zdravotně sociální fakulta, Jihočeská univerzita v Českých Budějovicích
ondrej.osmera@seznam.cz
Zdroje
1. Paré G, Jaana M, Sicotte C. Systematic review of home telemonitoring for chronic diseases: the evidence base. J Am Med Inform Assoc 2007; 14 : 269–277.
2. Masella C, Zanaboni P, Di Stasi F et al. Assessment of a remote monitoring system for implantable cardioverter defibrillators. J Telemed Telecare 2008; 14 : 290−294.
3. Ošmera O, Bulava A. Telemedicína – objev třetího tisíciletí? Cor Vasa 2010; 52 : 55−61.
4. J. Lipoldová, M. Novák. Dálkové monitorování implantabilních kardiostimulátorů a kardioverterů-defibrilátorů. Kardiol Rev 2006; 8 : 129–139.
5. Ricci RP, Morichelli L, Santini M. Home monitoring remote control of pacemaker and implantable cardioverter defibrillator patients in clinical practice: impact on medical management and health-care resource utilization. Europace 2008; 10 : 164−170.
6. Wilkoff B, Auricchio A, Brugada J et al. Heart Rhythm Society (HRS); European Heart Rhythm Association (EHRA); American College of Cardiology (ACC); American Heart Association (AHA); European Society of Cardiology (ESC); Heart Failure Association of ESC (HFA); Heart Failure Society of America (HFSA). HRS/EHRA Expert Consensus on the Monitoring of Cardiovascular Implantable Electronic Devices (CIEDs): description of techniques, indications, personnel, frequency and ethical considerations: developed in partnership with the Heart Rhythm Society (HRS) and the European Heart Rhythm Association (EHRA); and in collaboration with the American College of Cardiology (ACC), the American Heart Association (AHA), the European Society of Cardiology (ESC), the Heart Failure Association of ESC (HFA), and the Heart Failure Society of America (HFSA). Endorsed by the Heart Rhythm Society, the European Heart Rhythm Association (a registered branch of the ESC), the American College of Cardiology, the American Heart Association. Europace 2008; 10 : 707−725.
7. Bytešník J, Čihák R. Arytmie v medicínské praxi. 1. vyd. Praha: Triton 1999 : 60–61.
8. Lévy S, Camm AJ, Saksena S et al. Working Group on Arrhythmias, Working Group on Cardiac Pacing of the European Society of Cardiology, North American Society of Pacing and Electrophysiology. International consensus on nomenclature and classification of atrial fibrillation; a collaborative project of the Working Group on Arrhythmias and the Working Group on Cardiac Pacing of the European Society of Cardiology and the North American Society of Pacing and Electrophysiology. Europace 2003; 5 : 119–122.
9. Risk factors for stroke and efficacy of antithrombotic therapy in atrial fibrillation. Analysis of pooled data from five randomized controlled trials [published erratum appears in Arch Intern Med 1994; 154 : 2254]. Arch Intern Med 1994; 154 : 1449–1457.
10. Miyasaka Y, Barnes ME, Petersen RC et al. Risk of dementia in stroke-free patients diagnosed with atrial fibrillation: data from a community-based cohort. Eur Heart J 2007; 28 : 1962–1967.
11. Dries DL, Exner DV, Gers JB et al. Atrial fibrillation is associated with an increased risk form mortality and heart failure progression in patients with asymptomatic and symptomatic left ventricular systolic dysfunction: a retrospective analysis of the SOLVD trials. J Am Coll Cardiol 1998; 32 : 695–703.
12. Hamer ME, Blumenthal JA, McCarthy EA et al. Quality-of-life assessment in patients with paroxysmal atrial fibrillation or paroxysmal supraventricular tachycardia. Am J Cardiol 1994; 74 : 826–829.
13. Lurie KG, Iskos D, Fetter J et al. Prehospital discharge defibrillation testing in ICD recipients: a prospective study based on cost analysis. Pacing Clin Electrophysiol 1999; 22 (1 Pt 2): 192–196.
14. Glotzer TV, Hellkamp AS, Zimmerman J et al. MOST Investigators. Atrial high rate episodes detected by pacemaker diagnostics predict death and stroke: report of the atrial diagnostics ancillary study of the MOde Selection Trial (MOST). Circulation 2003; 107 : 1614–1619.
15. Capucci A, Santini M, Padeletti L et al. Italian AT500 Registry Investigators. Monitored Atrial Fibrillation Duration Predicts Arterial Embolic Events in Patients Suffering From Bradycardia and Atrial Fibrillation Implanted With Antitachycardia Pacemakers. J Am Coll Cardiol 2005; 46 : 1913–1920.
16. Glotzer T, Daoud EG, Wyse DG et al. The Relationship Between Daily Atrial Tachyarrhythmia Burden From Implantable Device Diagnostics and Stroke Risk: the TRENDS study. Circ Arrhythm Electrophysiol 2009; 2 : 474–480.
17. Varma N, Stambler B, Chun S. Detection of atrial fibrillation by implanted devices with wireless data transmission capability. Pacing Clin Electrophysiol 2005; 28 Suppl 1: S133–S136.
18. Ricci RP, Morichelli L, Santini M. Remote control of implanted devices trough Home Monitoring technology improves detection and clinical management of atrial fibrilation. Europace 2009; 11 : 54−61.
19. Schmitt C, Montero M, Melichercik J. Significance of supraventricular tachyarrhythmias in patients with implanted pacing cardioverter defibrillators. Pacing Clin Electrophysiol 1994; 17 (3 Pt 1): 295–302.
20. Cesario DA et al. Atrial fibrillation and outcomes in a large cohort of CRT recipients: results from the ALTITUDE study. J Am Coll Cardiol 2011; 57 : 153.
21. Theuns DA, Klootwijk AP, Simoons ML et al. Clinical variables predicting inappropriate use of implantable cardioverter-defibrillator in patients with coronary heart disease or nonischemic dilated cardiomyopathy. Am J Cardiol 2005; 95 : 271–274.
22. Moss AJ, Zareba W, Hall WJ et al. Multicenter Automatic Defibrillator Implantation Trial II Investigators. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346 : 877–883.
23. Fauchier L, Sadoul N, Kouakam C et al. Potential cost savings by telemedicine-assisted long-term care of implantable cardioverter defibrillator recipients. Pacing Clin Electrophysiol 2005; 28 (Suppl 1): S255−S259.
24. Res JC, Theuns DA, Jordaens L. The role of remote monitoring in the reduction of inappropriate implantable cardioverter defibrillator therapies. Clin Res Cardiol 2006; 95 (Suppl 3): III17−21.
25. Boriani G, Gasparini M, Landolina M et al. Clinical Service cardiac centres. Incidence and clinical relevance of uncontrolled ventricular rate during atrial fibrillation in heart failure patients treated with cardiac resynchronization therapy. Eur J Heart Fail 2011; 10. [Epub ahead of print]
26. Zareba W, Steinberg JS, McNitt S et al. MADIT II Investigators. Implantable cardioverter-defibrillator therapy and risk of congestive heart failure or death in MADIT II patients with atrial fibrillation. Heart Rhythm 2006; 3 : 631–637.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2011 Číslo 3
-
Všechny články tohoto čísla
- Fibrilace síní z pohledu nových doporučení a dálková monitorace v kardiologii
- Antiarytmická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní
- Nefarmakologická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní
- Antitrombotická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní
- Upstream terapie u fibrilace síní
- Home monitoring nemocných s fibrilacemi síní
- Home monitoring a implantáty
- Telemonitoring krevního tlaku u nemocných s arteriální hypertenzí
- Twin cities
- Chronické srdeční selhání u ženy středního věku při nonkompaktní kardiomyopatii
- Galerie autorů
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Antiarytmická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní
- Chronické srdeční selhání u ženy středního věku při nonkompaktní kardiomyopatii
- Antitrombotická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní
- Home monitoring a implantáty
