Je protidestičková léčba indikována v primární prevenci?
Is anti-platelet treatment indicated in primary prevention?
Thrombosis complications of atherosclerosis are the cause of a pandemic of different cardiovascular diseases in the industrialised world. Since the end of the 1980’s there has been a series of studies monitoring the effect of anti-platelet treatment using acetylsalicylic acid (ASA) as part of primary prevention. Almost one hundred thousand probands have been included in these controlled studies. A composite analysis of the results shows that the treatment is effective in the prevention of acute myocardial infarction, finding a clinically and statistically significant reduction in incidence of around one-third. Undesirable effects accompanying the administration of ASA were bleeding, in particular significant bleeding into the digestive tract. This was recorded in 1–2% of those treated. Treatment with lower dosages of ASA should therefore be indicated in primary prevention only for those probands with a higher risk of coronary incident, i.e.
particularly for older men with an accumulation of at least 2 significant risk factors for atherogenesis.
Keywords:
atherothrombosis – primary prevention – acetylsalicylic acid – myocardial infarction
Autoři:
J. Bultas; D. Karetová
Vyšlo v časopise:
Kardiol Rev Int Med 2007, 9(4): 242-246
Kategorie:
Redakční článek
Souhrn
Trombotické komplikace aterosklerózy jsou příčinou pandemie řady kardiovaskulárních chorob v industriální společnosti. Od konce 80. let 20. století máme k dispozici řadu studií sledujících efekt protidestičkové léčby acetylsalicylovou kyselinou (ASA) v rámci primární prevence. Do těchto kontrolovaných studií bylo zařazeno téměř 100 000 probandů. Ze souhrnné analýzy výsledků vyplývá, že léčba je v prevenci akutního myokardiálního infarktu účinná, dokumentován je klinicky i statisticky významný pokles příhod asi o třetinu. Nežádoucím účinkem provázejícím podávání ASA bylo krvácení, zejména významné krvácení do zažívacího traktu. To se objevovalo u 1–2 % léčených. Proto bychom měli indikovat léčbu nižšími dávkami ASA v primární prevenci pouze u probandů s vyšším rizikem koronární příhody, tj. zejména u starších mužů s kumulací alespoň 2 významných rizikových faktorů aterogeneze.
Klíčová slova:
aterotrombóza – primární prevence – kyselina acetylsalicylová – infarkt myokardu
Úvod
Podíváme-li se, jak staré jsou snahy užít protidestičkovou léčbu v profylaxi kardiovaskulárních příhod, zjistíme, že již před 60 lety navrhl Paul Gibson podávání acetylsalicylové kyseliny (ASA) v prevenci koronární trombózy[1]. Rutinní zavedení antitrombotik v profylaxitrombotických příhod však trvalo více než 30 let. Dnes je protidestičková léčba jedním z významných faktorů zlepšujících prognózu nemocných s ischemickou chorobou srdeční, mozkovou či periferních tepen. Zda je tato profylaxe vhodná i u osob bez manifestní aterosklerózy, analyzuje tento souhrn.
Trombotické cévní komplikace jsou hlavní příčinou nemocnosti a úmrtnosti v industriální společnosti. Aterotrombóza je podkladem nemocí jako je infarkt myokardu, mozková mrtvice či kritická končetinová ischemie. Bohužel se tyto choroby často objevují u osob asymptomatických – více než polovina myokardiálních infarktů či iktů vzniká jako první projev choroby. Budeme-li proto s léčbou čekat až po překonání kardiovaskulární příhody – tj. až na prevenci sekundární – může být pro řadu nemocných pozdě. Podívejme se proto, zda máme dostatek dokladů pro iniciaci antitrombotické léčby u osob ještě asymptomatických, tj. v rámci prevence primární.
Význam endotelu, primární a sekundární hemostázy
Vlastní hemostáza má několik funkčních rovin: antitrombotickou roli intaktního endotelu, destičkovou hemostázu, koagulační kaskádu ústící v polymerizaci fibrinogenu a fibrinolýzu. V genezi aterotrombotických příhod hraje rozhodující roli poškození endotelu a primární, tzn.destičková, hemostáza. Intaktní endotel inhibuje aktivaci trombocytů (např. uvolněním NO a prostacyklinu), koagulační kaskádu (např. sekrecí trombomodulinu, heparan sulfátu či inhibitoru tkáňového faktoru – TFPI) a stimuluje také fibrinolýzu, tvorbou aktivátoru tkáňového plazminogenu – t-PA (schéma).

Destičková zátka vzniká všude tam, kde dojde k odhalení subendoteliálních struktur a k navázání trombocytů na kolagenní vlákna. Vlastní vazba vede k aktivaci trombocytů a k sekreci řady protrombotických substancí (tromboxanu A2 – TXA2, adenosin difosfátu – ADP, serotoninu aj.) a k uvolnění povrchových glykoproteinových receptorů IIb/IIIa. Vznik destičkového trombu je dán vzájemnou vazbou trombocytů pomocí receptorů IIb/IIIa a adhezivních proteinů, zejména fibrinogenu. Vzniklý destičkový trombus dále akceleruje koagulační kaskádu, neboť na povrchu aktivovaných destiček dojde k odhalení fosfolipidů katalyzujících koagulaci. Sekundární hemostáza, čili vytvoření fibrinové sítě pak trombotický proces stabilizuje [2,3]. V etiopatogenezi trombotické okluze však má rozhodující význam hemostáza destičková. Proto též v tomto přehledu klademe důraz na léčbu protidestičkovou, která je považována za zlatý standard.
Protidestičková léčba
Protidestičkové léky mohou působit na různých etážích, tzn. inhibují adhezi, aktivaci či agregaci (tab.1). Proto se upustilo od staršího názvu antiagregancia. Ovlivnění aktivace a sekrece dosáhneme např. acetylsalicylovou kyselinou (ASA), která ireverzibilně inhibuje cyklooxygenázu a utlumí tak syntézu důležitého aktivátoru destiček – TXA2. Podobně klopidogrel a tiklopidin nevratně zamezí aktivaci destičkových receptorů ADP a tlumí tak aktivaci trombocytů. Dipyridamol naopak reverzibilně inhibuje destičkovou fosfodiesterázu, která degraduje cyklický adenozin monofosfáz (cAMP) a cyklický guanozin monofosfát (cGMP), 2 důležité „druhé posly“stabilizující trombocyt. Inhibitory destičkových receptorů GP IIb/IIIa tlumí primární hemostázu ve fázi agregace. Vzhledem k vysoké ceně a k riziku krvácivých komplikací nebyla tato skupina k primární prevenci testována.

Kdo je nejvíce ohrožen?
V rámci primární prevence můžeme léčit pacienty se značně odlišným rizikovým skóre. Obecně lze říci, že u rizikové populace bude absolutní přínos léčby větší. Jak vytypovat správnou cílovou populaci? Riziko trombózy dramaticky stoupá s věkem. Příčin tohoto vzestupu je více: často je přítomná dysfunkce endotelu, stoupá prevalence aterosklerotického postižení tepenného řečiště, při inaktivitě či při fibrilaci síní se objevuje stáza krve, negativně se uplatňují též hormonální změny, interkurentní zánětlivé afekce, imobilizace či nádorová onemocnění vedou k aktivaci hemostázy a k hyperkoagulačnímu stavu. Více jsou ohroženi muži, u žen stoupá riziko až od 6. dekády či při hormonální substituční léčbě nebo hormonální antikoncepci. V obou skupinách pak přítomnost rizikových faktorů jakými jsou diabetes, dyslipidemie, hypertenze či kouření výskyt trombotických příhod násobí. Z těchto důvodů bychom se měli zejména zaměřit na tuto část populace.
Jaké jsou výsledky intervenčních studií?
K prevenci trombotických, resp. aterotrombotických, komplikací u populace bez zjevného kardiovaskulárního postižení se na prvém místě nabízí kyselina acetylsalicylová. Její výhodou je prověřený účinek v řadě jiných klinických situací. K těmto situacím patří zejména akutní a chronické formy ICHS, stavy po cévních mozkových příhodách či různé formy aterosklerózy periferního tepenného řečiště. Výhodou ASA je též nízká cena a dobrá snášenlivost.
Jaký je efekt ASA v rámci prevence primární? Máme k dispozici řadu studií, výsledky jsou souhrnně prezentovány na grafu 1 a v tab. 2. První 2 studie, které sledovaly dopad ASA na kardiovaskulární příhody, měly mnoho společného: Užívaly střední dávky ASA (325 mg, resp. 500 mg denně), byly prováděny v 80. letech a do studie byly zařazeni pouze zdraví lékaři – muži [4,5]. Ve studii britské, která po dobu 6 let sledovala více než 5 000 mužů, byl pozorován zajímavý efekt: 1/3 probandů randomizovaných k aktivní léčbě přestala ASA užívat, naopak část lékařů v placebo větvi ASA užívala.Výsledkem bylo výrazné oslabení výpovědní hodnoty studie: Byl patrný pouze nevýznamný trend k poklesu fatálních i nefatálních infarktů myokardu, k poklesu celkové i kardiovaskulární mortality a mírný trend k vzestupu mozkovýchpříhod. Obdobná, dvojitě slepá a na svou dobu nebývale rozsáhlá studie (22 000 mužů) byla provedena v USA. Po 5 letech byla studie předčasně ukončena pro vysoce významný pokles výskytu infarktu myokardu, který činil plných 47 % při léčbě ASA. Kardiovaskulární ani celková mortalita však ovlivněna nebyla. I v této studii byl pozorován trend k vzestupu četnosti mozkových příhod (tab. 2). Vzhledem k výrazné podobnosti obou studií byla provedena souhrnná analýza: Výskyt infarktu myokardu klesl významně o 1/3 (tj. o 32 %), celková úmrtnost klesla nevýznamně o 10 %. Při analýze cirkadiálního výskytu infarktu myokardu byl pozorován zajímavý efekt – podávání ASA zabránilo vzestupu výskytu příhod v ranních hodinách v době aktivace destiček při sympatikotonii.

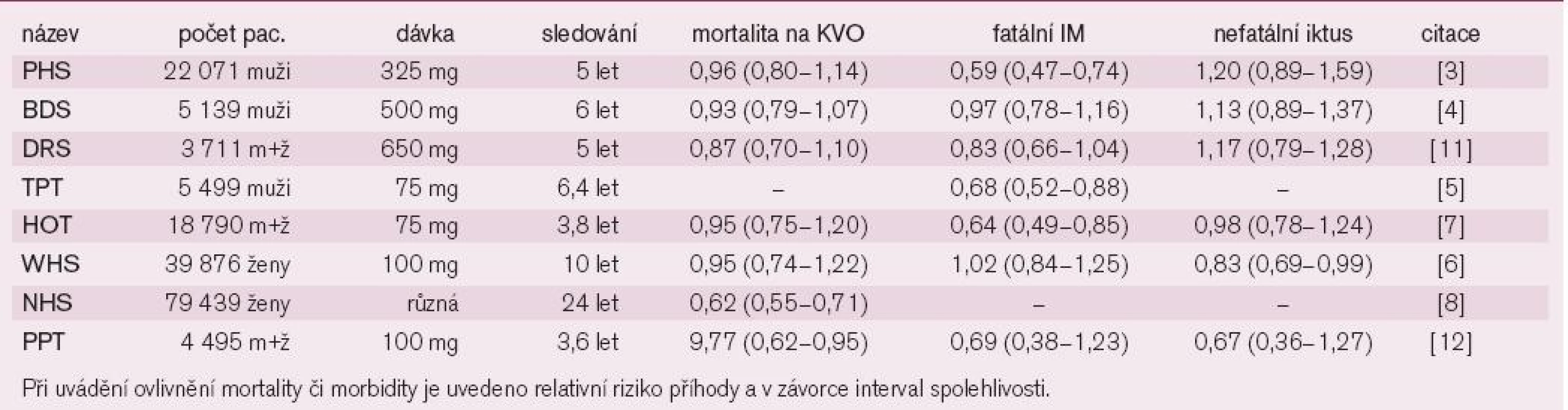
Třetí studií, která sledovala efekt ASA pouze u mužské asymptomatické populace, byla studieThrombosis Prevention Trial [6]. Během více než 6 let sledování 5 500 tisíce mužů byl pozorován v aktivní větvi léčené 75 mg ASA významný pokles nefatálního myokardiálního infarktu o 32%,ostatní ukazatele efektu nejsou k dispozici.
Nejvýznamnějším, na jaře 2007 ukončeným projektem, který sledoval efekt ASA v primární prevenci u žen byl Nurses’ Health Study [8]. Projekt je ojedinělý jednak počtem sledovaných žen – téměř 80 000 – i délkou sledování – od r. 1976 do r. 2004. Pravidelně užívalo ASA asi 35 000 žen. V této kohortě byl o 38 % nižší výskyt úmrtí z KV - příčin (RR, 0,62; 95% CI0,55–0,71), celková úmrtnost klesla o 25 % (RR 0,75; 95% CI 0,71–0,81). Na poklesu celkové mortality se podílelo menší měrou i snížení výskytu zhoubných nádorů o 12 % (RR 0,88;95% CI 0,81–0,96). Efekt ASA se projevil jiždo 5 let, naopak dopad na onkologická onemocnění byl pozorován až po 10 letech. Pokles kardiovaskulární mortality byl výrazně větší u žen starších a u žen s kumulací rizikových faktorů aterogeneze.
Byl-li pozorován u mužů pokles výskytu infarktu myokardu o 32 %, jak vypadá efekt u žen? Výhradně ženskou populaci sledovala Women Health Study [7]. Tento rozsáhlý recentní projektu 40 000 žen sledovaných po dobu 10 let neukázal žádný efekt profylakticky podávané ASA v obecné populaci na výskyt kardiovaskulární mortality, nefatálního infarktu myokardu či iktu (tab. 2). Pouze v podskupině žen nad 65 let snížila ASA výskyt těchto ukazatelů významně. Také metaanalýza studií s ženskou populací ukázala v podskupině žen nad 65 let významný pokles myokardiálního infarktu o 24 %, mortalita či výskyt mozkových příhod ovlivněny nebyly [7].
Dvě studie se zabývaly rizikovou smíšenou, tj. ženskou i mužskou, populací. U hypertoniků byl ve studii HOT dokumentován příznivý účinek doplnění antihypertenzní léčby o 75 mg ASA [9]. Opět byl pozorován významný pokles nefatálních infarktů myokardu o více než 1/3, zato kardiovaskulární úmrtnost či mozkové příhody ovlivněny nebyly (tab. 2). Podobná studie (Primary Prevention Trial) se smíšenou populací dospěla k podobným závěrům – významný pokles infarktu myokardu o 29 % a kardiovaskulární úmrtnosti o 23 %, výskyt mozkových příhod významně snížen nebyl.
Budeme-li chtít výsledky s ASA v primární prevenci shrnout, pak je možno říci, že u mužů jsou doklady o efektu ASA v primární prevenci na pokles výskytu nefatálního infarktu myokardu již ve věku středním, přínos je klinicky významný při kumulaci rizikových faktorů aterogeneze. Souhrnná data z 5 primárně preventivních studií (Physicians Health Study, British Doctors Trial, Thrombosis Prevention Trial, HOT Study a Primary Prevention Project) dokumentují pokles rizika infarktu o 32 % (RR 0,68, 95% CI0,54–0,86, p = 0,001) s nesignifikantním vzestupem mozkových příhod o 13 % (RR 1,13,95% CI 0,96–1,33, p = 0,15). V ženské populaci jsou obdobné, stejně významné doklady o efektu až od věku nad 60 let. Nicméně u starších žen jsou doklady o snížení úmrtnosti i výskytu cévních příhod nejméně stejně silné jako u mužů.
Ve studii CHARISMA byl prověřován účinek klopidogrelu přidaného k ASA u asyptomatických osob s kumulací rizikových faktorů a u osob symtomatických. V podskupině asymptomatických osob byl patrný trend k vzestupu souhrnného ukazatele (IM, iktus a KV úmrtnost) o 20 %, podobně stoupla též celková mortalita [10]. Je tedy možno formulovat závěr, že duální protidestičková léčba v primární prevenci není výhodná. V monoterapii nebyly ani klopidogrel ani tiklopidin testovány.
Dipyridamol je poslední z protidestičkových léků, o němž se uvažovalo v rámci primární prevence.Výsledky několika malých studií uzavřela analýza Cochrainova institutu konstatováním, že v rámci primární prevence nejsou doklady o efektu dipyridamolu ani v monoterapii ani v kombinaci [11].
Jaká jsou rizika protidestičkové léčby?
Podávání kyseliny acetylsalicylové či jiných protidestičkových léků je spojeno s rizikem krvácení, zejména krvácení do zažívacího traktu. Podkladem krvácení do zažívacího traktu je vlastní protidestičkový efekt a inhibice prostaglandinu E2, který má významný cytoprotektivní efekt na žaludeční sliznici. Riziko středně závažného krvácení se pohybuje kolem 1–2 % ročně, riziko velmi závažného pak kolem 0,1 až 0,2 % ročně. Dokument vydaný experty Evropské kardiologické společnosti ukázal, že riziko krvácení je srovnatelné u všech protidestičkových léků [12]. Není proto účelné zaměňovat při krvácení jeden lék za jiný. Podobně není indikováno rutinní podávání inhibitorů protonové pumpy v rámci prevence krvácení. Pouze při nutnosti pokračovat v protidestičkové léčbě u nemocného s anamnézou recentního krvácení do zažívacího traktu je výhodná dlouhodobá léčba inhibitory protonové pumpy, např. omeprazolem. Vlastní riziko krvácení lze snížit aplikací ASA v jedné dávce s podáním rychle a krátce působícího přípravku, užitím nižších dávek, tj. optimálně 75 až 100 mg ASA denně či obden, a vyvarováním se souběžného užívání nesteroidních antirevmatik. Analgetika typu paracetamolu naopak nevadí.
Kdy užít protidestičkovou léčbu,co doporučuje návrh expertů?
Experti Evropské kardiologické společnosti doporučují preventivní podávání malých dávek, tj.75–300 mg ASA denně či obden v primární prevenci při absolutním riziku příhody nad 1,5 % ročně. V takovém riziku jsou starší nemocní (od 7. decenia) s kumulací alespoň 2 rizikových faktorů, tj. kuřáci, diabetici, hypertonici či nemocní s dyslipidemií. Od léčby lze očekávat pokles výskytu infarktu myokardu asi o 1/3.
Jak postupovat v praxi – kdy acetylsalicylovou kyselinuv primární prevenci indikovat?
Stojíme před rozhodnutím: Na jedné straně můžeme snížit riziko infarktu myokardu, na straně druhé ohrozíme nemocného krvácením. Budeme-li porovnávat obě strany, musí v souladu s doporučenými postupy riziko koronární příhody významně převážit riziko krvácení. Vzhledem k tomu, že riziko středně významného až závažného krvácení se pohybuje kolem 1–2 % ročně, měli bychom indikovat ASA až při absolutním riziku akutní formy ICHS, zejména infarktu myokardu od 2 %. Tak převáží přínos léčby nad případným rizikem. Z grafu závislosti přínosu léčby na absolutním riziku kardiovaskulární příhody je patrné, že přínos léčby můžeme očekávat zejména u nemocných starších s kumulací alespoň 2 rizikových faktorů (graf 2).

Vedle poměru přínos versus riziko bychom měli zvážit též pohled farmakoekomomický. Budeme-li uvažovat roční riziko příhody 2 %, efekt léčby, tj. snížení rizika příhody 20–30 % a přímých ročních nákladů na léčbu kolem 300 Kč, musíme vynaložit pouhých 60 000 Kč k profylaxi 1 infarktu myokardu. Z farmakoekonomického pohledu jsou přímé náklady jistě příznivé. Nepřímé náklady, tj. výdaje spojené s případným krvácením, budou jistě výrazně nižší než výdaje spojené s léčbou akutní koronární příhody.
Racionálním postupem je tedy indikovatléčbu nižšími dávkami ASA (75–100 mg) v primární prevenci pouze u probandů s vyšším rizikem koronární příhody, tj. zejména u starších mužů a žen s kumulací alespoň 2 významných rizikových faktorů aterogeneze.
prof. MUDr. Jan Bultas, CSc.1
doc. MUDr. Debora Karetová, CSc.2
1Ústav farmakologie 3. LF UK, Praha
2II. interní klinika 1. LF UK a VFN, Praha
jbult@lf1.cuni.cz
Zdroje
1. Gibson P. Salicylic acid for coronary thrombosis? Lancet 1948; 1 : 965.
2. Colman RW, Hirsh J, Marder VJ et al. Hemostasis and thrombosis. Philadelphia: Lippincott Williams & Wilkins 2001.
3. Gawaz M. Blood platelets. Stutgart: Georg Thieme Verlag 2001.
4. The Steering Committee of the Physicians’ Health Study Research Group. Findings from the aspirin component of the ongoing Physicians Health Study. N Engl J Med 1988 : 318 : 262–264.
5. Petro R et al. Randomised trial of prophylactic daily aspirin in British male doctors. BMJ 1988; 296 : 313–316.
6. Thrombosis Prevention Trial. Lancet 1988; 351 : 233–241.
7. Ridker PM et al. A randomised trial of low dose aspirine in the primary prevention of cardiovascular diseases in woman. N Engl J Med 2005; 352 : 1293–1304.
8. Chan AT et al. Long-term aspirin use and mortality in women. Arch Intern Med 2007; 167(6): 562-572.
9. Hansson L et al. Effects of intensive blood pressure lowering and low-dose aspirin in patients with hypertension. HOT Study Group. Lancet 1998; 351 : 1855–1862.
10. Bhatt DL at al. A global view of atherothrombosis: baseline characteristics in the Clopidogrel for High Atherothrombotic Risk and Ischemic Stabilization, Management,and Avoidance (CHARISMA) trial. Am Heart J 2005; 150(3): 401.
11. De Schryver EL et al. Cochrane review: dipyridamole for preventing major vascular events in patients with vascular disease. Stroke 2003; 34(8): 2072–2080.
12. Patrono C et al. Expert consensus document on the use of the antiplatelet agents. Eur Heart J 2004; 25(2): 166–181.
13. ETDRS Investigators. Aspirin effects on morbidity and mortality in patients with diabetes mellitus. Early Treatment Diabetic Retinopathy Study Report 14. JAMA 1992; 268 : 1292–1300.
14. De Gaetano G et al. Collaborative Group of the Primary Prevention Project. Lancet 2001; 257 : 89–95.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2007 Číslo 4
-
Všechny články tohoto čísla
- Nobelova cena za fyziologii a medicínu 2007
- Poruchy glukózového metabolizmu u infarktu myokardu
- Je dilatační kardiomyopatie geneticky podmíněné onemocnění?
- Atypicky se prezentující nebo zcela bezbolestně probíhající AIM
- Zvláštnosti léčby akutního infarktu myokardu a diagnostické problémy u nemocných s diabetes mellitus
- Studie BARI 2D – sekundární prevence a optimální léčebné strategie u diabetiků 2. typu s ischemickou chorobou srdeční
- Je protidestičková léčba indikována v primární prevenci?
- Antiagregační léčba a potahované stenty v roce 2007
- Klinický význam měření distenzibilty karotické tepny
- Mitrální stenóza
- Použití kryodestrukce v nefarmakologické terapii fibrilace síní
- Současné možnosti chirurgické léčby fibrilace síní
- Koarktace aorty
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Mitrální stenóza
- Koarktace aorty
- Atypicky se prezentující nebo zcela bezbolestně probíhající AIM
- Je dilatační kardiomyopatie geneticky podmíněné onemocnění?
