Automatické funkce kardiostimulátorů
Pacemaker automatic functions
Early pacemakers were single-chamber, non-programmable, fixed rate devices. First automatic function was ability to sense intrinsic electrical activity. Nowadays the concept of „smart pacemaker“ is being created. That means general diagnostics, automatic optimization of pacing and arrhythmia treatment. Huge number of automatic functions for solving different problems and possible misinterpretation of heart rhythm is known till now. Pacemaker is no longer simple pulse generator but „monitor“ of heart rhythm and haemodynamic status and detector of incoming heart decompensation in patients with heart failure etc.
Pacemaker automatic functions (providing antibradycardia pacing and cardiac resynchronization therapy) were divided systematically to: control of pacemaker proper function (appropriate pacing and sensing, control of system integrity), functions for optimizing of pacemaker parameters (change of pacing rate, change of atrioventricular delay according to preference of intrinsic conduction or pacing, prevention and management of atrial tachyarrhythmias, prevention and management of pacemaker tachycardia, management of wrong sensing and oversensing) and diagnostic functions including storing of information about pacemaker activity and heart rhythm. The list of functions and algorithms is not complete and was not meant as summary of all possible functions. The aim is to put the reader into picture of pacemaker complexity.
Keywords:
pacemaker automatic functions, automatic capture, automatic sensitivity, sensor, hysteresis, hysteresis search, repetitive hysteresis, preference of intrinsic conduction, atrioventricular hysteresis, overdrive mode, atrial tachyarrhythmia prevention, mode switch, pacemaker tachycardia, endless loop tachycardia, pacemaker diagnostics functions
Autoři:
J. Lipoldová; M. Novák
Působiště autorů:
I. interní kardioangiologická klinika LF MU a FN u sv. Anny, Brno
; as. MUDr. Miroslav Novák, CSc.
Vyšlo v časopise:
Kardiol Rev Int Med 2006, 8(4): 174-184
Kategorie:
Redakční článek
Souhrn
První kardiostimulátory byly jednodutinové, neprogramovatelné, pracující v asynchronním režimu. První automatickou funkcí bylo vnímat vlastní srdeční akci. V současné době je vytvářen koncept „chytrého kardiostimulátoru“ („smart pacemaker“), což zahrnuje všestrannou diagnostiku, automatickou optimalizaci stimulace a terapii arytmií. V současné době existuje nepřeberné množství algoritmů řešících různé problémy i možné nesprávné interpretace vlastní činnosti. Kardiostimulátor už není jen pouhým generátorem impulzů, ale zároveň „monitorem“ srdeční činnosti a hemodynamické situace, u pacientů se srdečním selháním je detektorem možné nastupující dekompenzace apod.
Automatické funkce kardiostimulátorů (zajišťujících bradykardickou stimulaci či resynchronizační terapii) jsme rozdělili tematicky na kontrolu správné činnosti kardiostimulátoru (účinnosti stimulace, správného vnímání, integrity systému), funkce k optimalizaci činnosti kardiostimulátoru (úpravu stimulační frekvence, úpravu síňokomorového zpoždění podle preference vlastního vedení či komorové stimulace, prevenci a řešení síňových tachyarytmií, prevenci a řešení pacemakerové tachykardie, řešení špatného či nadměrného vnímání) a funkce diagnostické vč. ukládání informací o činnosti přístroje a o srdečním rytmu. Výčet funkcí a algoritmů není kompletní a nemůže být chápán jako absolutní přehled všech dostupných funkcí. Cílem je čtenáře zasvětit do širokých možností a zároveň do komplexnosti problematiky.
Klíčová slova:
automatické funkce kardiostimulátoru, automatic capture, automatic sensitivity, senzor, hystereze, vyhledávání hystereze, repetitivní hystereze, preference vlastního atrioventrikulárního vedení, atrioventrikulární hystereze, režim přestimulování, prevence síňových tachyarytmií, mode switch, pacemakerová tachykardie, diagnostické funkce kardiostimulátoru
Úvod
První kardiostimulátory (pacemakery - PM) byly jednodutinové, neprogramovatelné, pracující v asynchronním režimu, v současné terminologii v režimu V00. Tehdy přístroj slepě vydával impulzy a neřešil, zdali je to činnost efektivní, či ne, ani to, jestli spontánní QRS-komplex přišel, či nepřišel.
Koncept „chytrého kardiostimulátoru“ („smart pacemaker“) [1] se začal rozvíjet s objevením první automatické funkce - schopnosti vnímat vlastní srdeční akci. V současné době „chytrý kardiostimulátor“ znamená všestrannou diagnostiku, optimalizaci stimulace a terapii arytmií. S rozvojem mikroelektroniky a růstem komplexnosti vznikaly nové situace, které bylo nutné kardiostimulátor naučit detekovat, analyzovat a řešit. V současné době existuje velké množství algoritmů řešících různé potenciální situace, včetně možné chybné interpretace vlastní činnosti. Kardiostimulátor už není jen pouhý generátor impulzů, ale zároveň je „monitorem“ srdeční činnosti a u pacientů se srdečním selháním je také detektorem možné nastupující dekompenzace.
V tomto pojednání budou shrnuty automatické funkce kardiostimulátorů (zajišťujících bradykardickou stimulaci či resynchronizační terapii). Otázka implantabilních kardioverterů-defibrilátorů je natolik rozsáhlá, že se jí dotkneme jen zcela okrajově.
Jednotlivé automatické funkce jsme rozdělili tematicky na kontrolu správné činnosti PM, funkce k optimalizaci činnosti PM a funkce diagnostické vč. ukládání informací o činnosti přístroje a o srdečním rytmu. Výčet funkcí a algoritmů není kompletní, ale jde o přehled většiny dostupných funkcí a algoritmů v naší praxi.
Budou uvedeny algoritmy následujících výrobců: Biotronik GmbH & Co. (Berlín, Německo) – dále jen Biotronik, Ela Medical - Sorin Group (Le Plessis-Robinson, France) – dále jen ELA, Guidant Corporation (St. Paul, MN, USA) – dále jen Guidant, Medtronic, Inc. (Minneapolis, MN, USA) – dále jen Medtronic, St. Jude Medical, Inc. (St. Paul, MN, USA) – dále jen SJM, Vitatron B.V. (Arnhem, Nizozemsko) – dále jen Vitatron.
Kontrola správné činnosti PM
Pod tento název jsme zahrnuli kontrolu účinnosti stimulace, kontrolu správného vnímání a kontrolu integrity systému.
Automatická kontrola účinnosti stimulace
Biotronik: Automatic Capture Control
ELA: Auto-Threshold V
Guidant: Automatic Capture
Medtronic: Ventricular Capture Management, Atrial Capture Management
SJM: Ventricular AutoCapture
Automatická kontrola a regulace stimulačního výdeje byla vyvinuta pro komorovou stimulaci už v roce 1973. Do praxe se dostala mnohem později. Funkci poprvé uvedla na trh firma St. Jude Medical ve svých modelech Microny a Regency a následně ji implementovala i do dalších modelů včetně 2dutinových PM (rodina Affinity, Entity, Identity a další).
Systém pracuje na principu zpětné vazby. Po vydání stimulačního impulzu systém potvrzuje, zda je přítomna odpověď myokardu. Tu hodnotí podle přítomnosti tzv. evokované odpovědi. Jedná se o potenciálovou změnu v okénku 15-62,5 ms po vydání stimulačního pulzu. V případě zjištění, že stimulace byla neúčinná, vydává PM záložní impulz o dostatečně vysokém energetickém výdeji (obr. 1). Prahovou hodnotu výdeje určuje systém automaticky vlastním testem, který provádí ve stanovenou denní hodinu, nebo ve stanovených časových intervalech. Součástí systému je i diagnostický záznam četnosti vydávání záložních impulzů a automatické přeprogramování na vyšší výdej stimulačního impulzu při detekci záchytu 2 a více následujících (konsekutivních) cyklů s neefektivní stimulací [2].
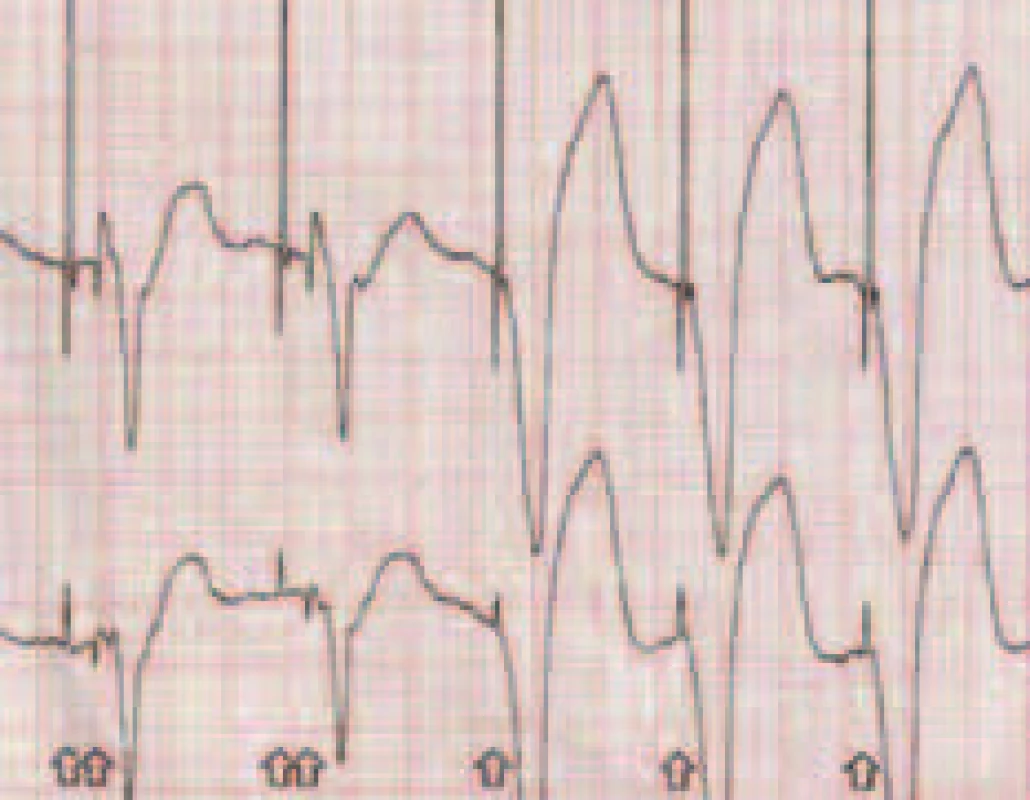
Nezbytností pro možné zapojení funkce je přítomnost bipolární elektrody a naprogramování unipolární stimulace a bipolárního vnímání.
Funkce SJM AutoCaptureTM je použitelná (resp. doporučovaná) u pacientů, kde evokovaná odpověď převýší „šum v pozadí“. Ten bývá tvořen hlavně polarizačním efektem rozložení stimulačních potenciálů kolem místa styku elektrody s myokardiální tkání. Velikost polarizačního signálu je závislá na povrchovém materiálu elektrody [3]. Nejmenší je u elektrod potažených nitridem titanu [4].
Velikost evokované odpovědi a polarizačního signálu nelze při implantaci běžným analyzačním zařízením měřit a nelze ji ani odhadnout pomocí měření velikosti vlny R [5,6]. Funkci je doporučováno zapojit až po vhojení elektrody (tj. asi měsíc po implantaci). Udává se, že cca u 5-7 % pacientů je evokovaná odpověď pro zapojení funkce nedostatečná [7]. V řadě studií bylo prokázáno, že zapojení funkce je bezpečné [8] a že v konečném důsledku vede k prodloužení praktické životnosti implantátu [9,10].
Analogické funkce vyvinuté firmami Biotronik, ELA, Guidant a Medtronic jsou kompatibilní s unipolárními i bipolárními elektrodami. Studie stran bezpečnosti jsou ale méně rozsáhlé.
Funkce není běžně užívána u ICD, ale na základě několika prospektivních studií [11] ji lze i v této indikaci využít. Procento pacientů s nedoporučením zapojení funkce je vyšší, cca 30 %. U ICD firmy SJM není funkce v základním softwarovém vybavení nabízena, neboť u ICD je vyžadována bipolární stimulace.
Bylo provedeno i úspěšné testování funkce u biventrikulární kardiostimulace [12], kdy ani při nastavení nenulového mezikomorového zpoždění nikdy nebyla stimulace kontralaterální komory chybně detekována jako evokovaná odpověď.
Automatická kontrola síňové stimulace vzhledem k malé evokované odpovědi přináší řadu technických problémů. První pokusy byly provedeny v roce 1991 [13] s užitím trifázického síňového pulzu k minimalizaci polarizačního efektu. Lepších výsledků v detekci evokované odpovědi bylo dosaženo výpočtem časového integrálu oproti maximální amplitudě signálu [14]. V současnosti je funkce dostupná u modelů firmy Medtronic a první studie svědčí o dobré efektivnosti a bezpečnosti [15].
Automatická kontrola správného vnímání vlastní srdeční činnosti
Biotronik: Automatic Sensitivity
ELA: AutoSensing (Atrial, Ventricular)
Medtronic: Sensing Assurance (Atrial, Ventricular)
SJM: Sense Ability
Automatické řízení citlivosti (senzitivity) je důležitou funkcí hlavně u ICD. Komorový filtr vstupního obvodu ICD je vyladěn na vnímání vln R v rozmezí mezi fyziologickým rytmem a komorovou fibrilací. Citlivost obvodu vstupu se automaticky přizpůsobuje amplitudě přicházejícího signálu. Jestliže se signál během komorové fibrilace zeslabuje, je citlivost zvýšena [16].
Některé modely (např. PM Medtronic EnRhythm DDD,R1) automaticky mění senzitivitu podle vnímaných signálů ze síní a komor. Funkce zároveň minimalizuje nadměrné vnímání (tj. oversensing) vlny T.
Přístroj automaticky upravuje prahy citlivosti po některých stimulovaných a vnímaných událostech, takže umožňuje snížení nadměrného snímání vln T a událostí v opačné dutině [17].
Automatická kontrola integrity systému
Biotronik: Automatic Lead Check
Medtronic: Automatic Impedance Measurement, Lead Monitor
Funkce automatické kontroly elektrody, resp. impedance, zajišťuje měření impedance elektrody při každém stimulu. Při detekci abnormální hodnoty je schopna přepnout mezi unipolární a bipolární stimulací [18].
Optimalizace činnosti PM
Pod tento název jsme zahrnuli přizpůsobení stimulační frekvence, automatickou optimalizaci síňokomorového zpoždění, optimalizaci činnosti PM při síňových tachyarytmiích a detekci vlastní možné chyby v interpretaci rytmu.
Schopnost zvýšení stimulační frekvence při zátěži či vegetativní synkopě
Senzor
Schopnost detekovat aktivitu pacienta a selektivně zvýšit podle její míry stimulační frekvenci byla do kardiostimulační techniky uvedena v 80. letech. V detekci aktivity bylo vyvinuto několik fyzikálních principů .
První modely využívaly piezoelektrických krystalů připevněných na pouzdro generátoru. Tlak prsních svalů na pouzdro se přenáší na krystaly, na kterých dochází k tvorbě elektrických potenciálů. Jejich amplituda odpovídá zátěži prsních svalů, tedy dobře koresponduje s fyzickou činností horní končetiny.
Následně byl vyvinut tzv. akcelerometr. Ten taktéž využívá piezoelektrického krystalu, který ale není v kontaktu s pouzdrem, ale jen malou plochou s obvody přístroje; při pohybu nebo vibraci dochází k deformaci krystalu a generování elektrického potenciálu [19].
Novější senzory využívají měření změny minutové ventilace [20]. PM vydává 8-20krát za sekundu podprahový stimulus mezi pouzdrem generátoru a prstencem komorové elektrody (u komorového PM) nebo síňovou elektrodou (u 2dutinového PM) a měří impedanci mezi generátorem a hrotem komorové elektrody. Změny transtorakální impedance dobře korelují s minutovou ventilací.
Jiné senzory aproximují aktivitu podle intervalu QT, u kterého je prokázána frekvenční závislost.
U všech typů PM s frekvenční adaptabilitou lze programovat řadu parametrů: míru zátěže, která spustí aktivaci senzoru (Biotronik a SJM: Sensor Threshold, Vitatron: Activity Threshold), maximální frekvenci vedenou senzorem (Maximum Sensor Rate), míru korelace mezi informacemi ze senzoru a skutečnou aktivitou (Biotronik: Sensor Gain, ELA, SJM a Vitatron: Slope, Guidant: Response Factor), parametry vzestupu frekvence (Biotronik: Rate Increase, SJM a Guidant: Reaction Time, Vitatron: Activity Acceleration) a poklesu senzorem vedené frekvence (Biotronik: Rate Decrease, SJM a Guidant: Recovery Time, Vitatron: Activity Deceleration). Některé parametry (např. Biotronik: Automatic Sensor Gain, ELA a SJM: Automatic Slope), popř. celé komplexní nastavení senzoru (např. Medtronic: Rate Profile Optimization, Vitatron: Fast Learn) lze naprogramovat na automatické nastavení. Systém podle dlouhodobých informací ze senzoru sám určí, jaká nejvyšší fyzická aktivita bývá pacientem dosahována a jak často bývá aktivita u pacienta přítomna, a podle toho upraví hodnoty příslušných parametrů.
Každý typ z výše uvedených principů senzoru má své výhody a nevýhody. Řada kardiostimulátorů je proto vybavena 2 senzory, které pracují na rozdílných principech [21] (akcelerometr + minutová ventilace nebo akcelerometr + interval QT).
Firma Biotronik vyvinula a v roce 2001 tzv. CLS-senzor (stimulace uzavřené smyčky, closed-loop stimulation). Jedná se o „fyziologický typ senzoru“. Využívá změny impedance pravokomorové elektrody, jejíž hodnota koreluje se změnou kontraktility pravé komory odrážející aktivaci autonomního nervového sytému. Je využíván mimo jiné v léčbě neurokardiogenní synkopy [22]. Při rapidním snížení preloadu (plnění pravé komory) v důsledku ortostatické reakce dojde k reaktivnímu zvýšení stimulační frekvence [23]. Systém CLS velmi dobře reaguje na evokovaný emoční stres [24]. Byl prokázán efekt na snížení zátěže síňovými tachyarytmiemi u pacientů s bradykardicko-tachykardickou formou sick sinus syndromu [25].
Schopnost snížení stimulační frekvence k přednostnímu uplatnění vlastního rytmu
Biotronik: Rate Hysteresis, Repetitive Rate Hysteresis, Scan Rate Hysteresis, Night Rate
ELA: Rest Rate
Guidant: Hysteresis Offset, Search Hysteresis
Medtronic: Rate Hysteresis, Sinus Preference, Sleep Function
SJM: Hysteresis Rate, Rate Hysteresis Search, Search Interval, Rest Rate
Vitatron: Atrial Refined Pacing, Night Rate Drop
Všichni výrobci implementují do svých výrobků funkci hystereze. Jako hystereze je označováno tolerování spontánního rytmu s nižší frekvencí, než je nastavená základní stimulační frekvence. Je označována buď absolutní hodnotou frekvence, nebo jako relativní (procentuální) snížení oproti základní stimulační frekvenci nebo vypočtené hodnotě stimulační frekvence (dané vlivem senzoru a dalšími algoritmy), tj. tzv. dynamická hystereze.
Vnímaná událost sníží stimulační frekvenci na frekvenci hystereze. V případě prodloužení intervalu R-R nad programovaný interval hystereze se uplatní stimulace a stimulační frekvence se opět zvýší na základní. Např. nastavení frekvence hystereze na 40 min-1 při základní stimulační frekvenci 60 min-1 znamená, že při snížení spontánní frekvence pod 40 min-1 se začne uplatňovat stimulace o frekvenci 60 min-1.
Rozšířením funkce hystereze je algoritmus zachovávající frekvenci hystereze po několik cyklů stimulovaného rytmu (opakování hystereze frekvence, Repetitive Hysteresis). Důsledkem je snížení zbytečné stimulace v důsledku např. jednorázové stimulace v postextrasystolické pauze.
Aktivnější přístup je přítomen ve funkci hledání hystereze (Scan Hysteresis, Hysteresis Search). Po programovatelném počtu konsekutivních stimulovaných stahů je na několik cyklů cíleně snížena stimulační frekvence na frekvenci hystereze. Pokud dojde k uplatnění vlastního rytmu, bude PM stimulovat až při poklesu spontánní frekvence pod frekvenci hystereze (v tom případě se stimulační frekvence zvýší na základní) [26].
Některé modely jsou vybaveny možností snížit základní programovanou frekvenci v době fyzického klidu (SJM a ELA: Rest Rate), detekované podle statistických informací senzoru. U jiných je možné programovat nižší tepovou frekvenci v nočních hodinách (Biotronik: Night Rate, Medtronic: Sleep Function, Vitatron: Night Rate Drop).
Schopnost změny síňokomorového (AV) zpoždění ve smyslu preference vlastního AV-vedení a spontánního šíření komorové aktivity
Biotronik: AV Hysteresis, Repetitive AV Hysteresis, AV Scan Hysteresis
ELA: AAIsafeR, DDD/AMC Mode
Guidant: AV delay hysteresis
Medtronic: Managed Ventricular Pacing, Search AV+
SJM: Autointrinsic Conduction Search
Vitatron: Ventricular Refined Pacing, AV delay hysteresis
Data z posledních let (studie MOST [27], studie DAVID [28] a další) ukazují, že vysoké procento pravokomorové stimulace je spojeno s vyšším rizikem rozvoje srdečního selhání, s vyšší celkovou mortalitou [29,30]. Všichni přední výrobci se proto soustředí na rozvíjení algoritmů zabraňujících nadměrné komorové stimulaci u 2dutinových modelů.
Prvním použitým algoritmem byla hystereze AV-intervalu (Biotronik: AV Hysteresis, Vitatron: AV delay hysteresis, Ventricular Refined Pacing, Guidant AV delay hysteresis [31] atd). Při detekci spontánní komorové události uvnitř programovaného AV-intervalu je AV-interval prodloužen o programovanou hodnotu. Naopak absence spontánní komorové události při prodlouženém AV-intervalu vede k jeho opětovnému zkrácení (obr. 2).
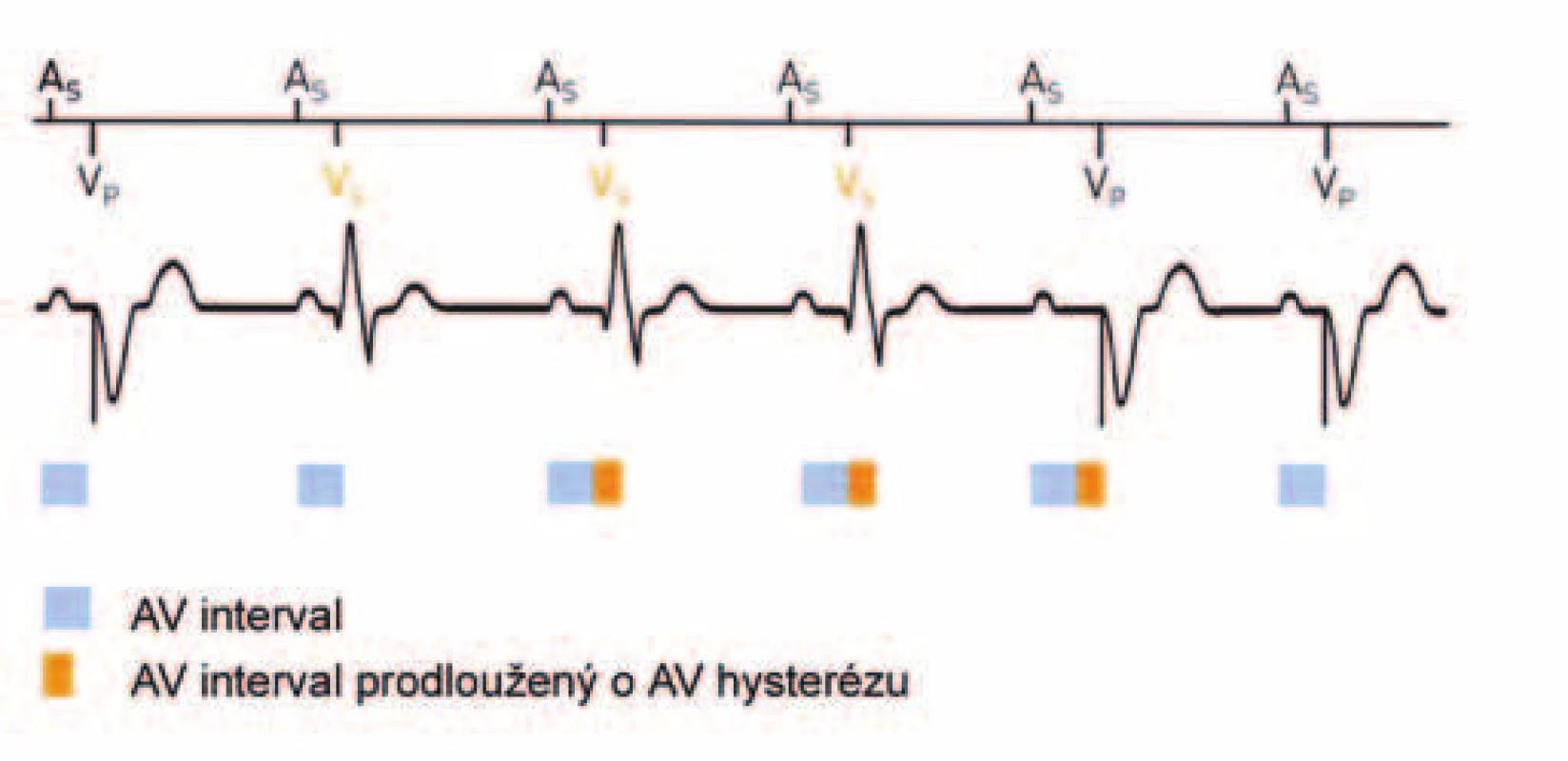
Druhým krokem snižujícím procento stimulovaných komorových událostí je zabránění zkrácení prodlouženého AV-intervalu už při první absenci spontánní komorové události. Tolerance více cyklů bez spontánního vedení je součástí funkce repetitivní AV-hystereze (Biotronik: Repetitive AV Hysteresis aj).
Ještě účinnější je aktivní vyhledávání vlastního AV-vedení funkcí skenování, resp. hledání AV-vedení (Biotronik: AV Scan Hysteresis, SJM: Autointrinsic Conduction Search, Medtronic: Search AV+ aj). Po programovatelném počtu konsekutivních stahů bez detekce spontánního AV-vedení je AV-interval prodloužen na několik cyklů a systém vyčkává detekce vlastního vedení. Pokud se objeví spontánní komorová událost, zůstane AV-interval prodloužený. V opačném případě dojde opět k jeho zkrácení na původní hodnotu.
Výše uvedené funkce dovolují prodloužení AV-intervalu na maximální hodnotu 300-350 ms. Tento zásah do časování PM může predisponovat ke vzniku pacemakerové tachykardie a též omezuje programování maximální sledovací frekvence (tj. maximální frekvence síní, která je PM převáděna na komory 1 : 1). Problém obcházejí nové funkce umožňující automatické střídání stimulace v režimu AAI a DDD. Algoritmus vyvinuly a rozvíjejí firma ELA (AAIsafeR, DDD/AMC Mode) a firma Medtronic (Managed Ventricular PacingTM). Pomocí těchto algoritmů se daří snížit procento pravokomorové stimulace i pod 0,4 % [32] při zachování bezpečnosti pro pacienta [33].
Schopnost změny síňokomorového (AV) zpoždění ve smyslu uplatnění komorové preexitace
Biotronik: Negative AV Hysteresis
Guidant: Tracking Preference
SJM: Negative AV/PV Hysteresis Search
V situacích, kdy je stimulace komor žádoucí (především u biventrikulární stimulace a stimulace pro hypertrofickou obstrukční kardiomyopatii), je výhodné užít negativní hysterezi AV-intervalu. Při detekci vlastní komorové události uvnitř AV-intervalu je AV-interval zkrácen (obr. 3).
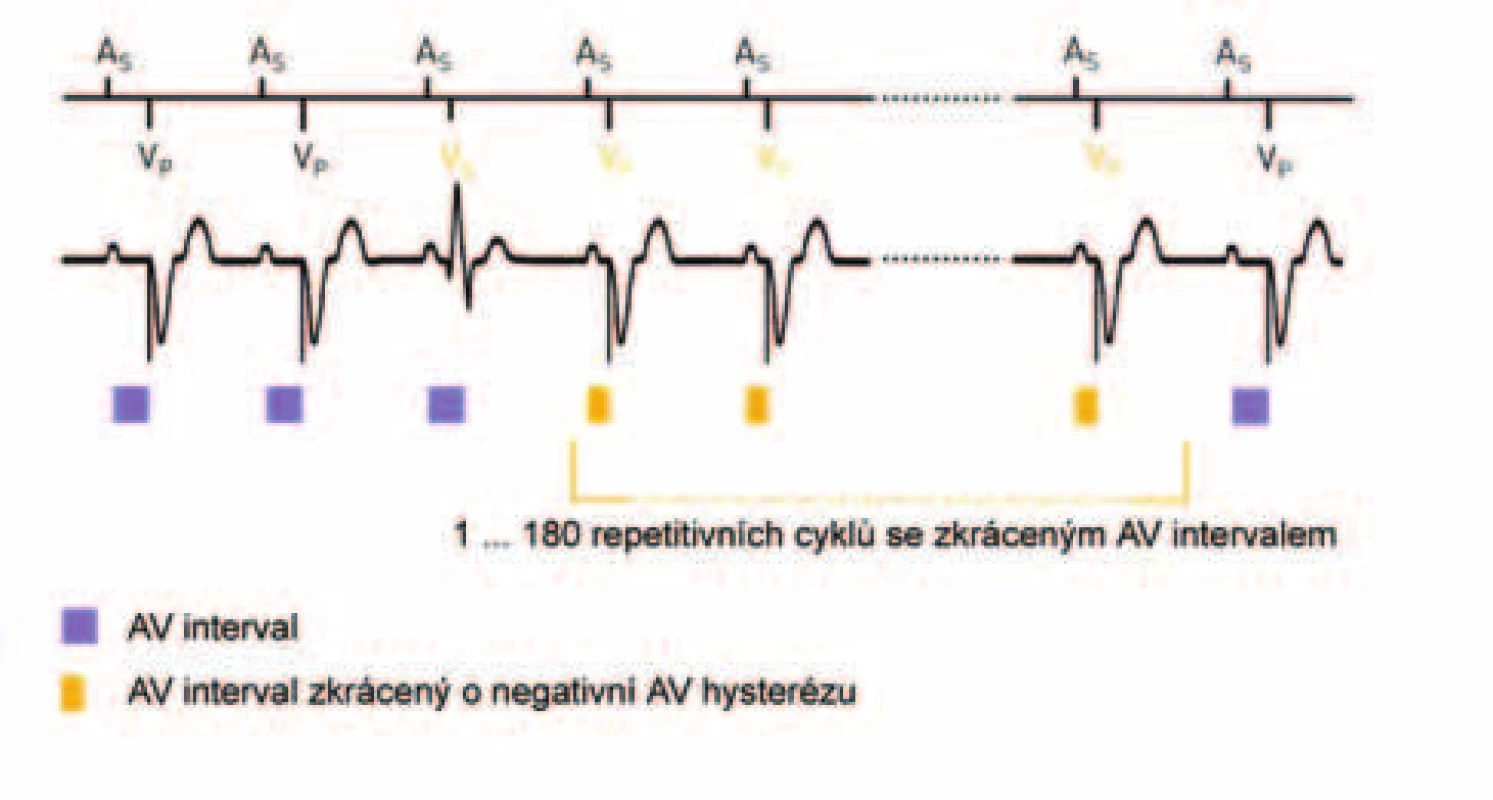
Možnost optimalizace činnosti při síňových tachyarytmiích ve smyslu prevence jejich vzniku
Biotronik: Overdrive režimy
ELA: Dynamic Sinus Rhythm Overdrive, Post Extrasystolic Pause Suppression, Rate Acceleration upon PACs
Medtronic: Atrial Preference Pacing, Post Mode Switch Overdrive Pacing (PMOP), Atrial Rate Stabilization
SJM: AF Suppression
Vitatron: Continuous Overdrive, Triggered Overdrive, Post-PAC Response, PAC Suppression, Post-AF Response, Post Exercise Response, Rate Soothing, Pace Conditioning
Algoritmy k prevenci rekurence fibrilace síní jsou zaměřeny na známé spouštěče [34] a můžeme je rozdělit na několik typů [35]:
- Trvalé přestimulování (overdrive) vlastního síňového rytmu: předpokládaným efektem tohoto algoritmu je snížení disperze atriální refraktorní periody [36,37] a redukce postextrasystolických pauz. Efekt byl sledován ve studii ADOPT-A [38], která prokázala snížení fibrilace síní (AF burden) o 25 %. Ve studii ATTEST [39] se prokázal i efekt přestimulování na verzi síňové tachykardie na sinusový rytmus. Většina výrobců proto vyvinula algoritmy přestimulování (Biotronik Overdrive režimy DDD(R)+, DDT/A(R)+, AAT(R)+, Medtronic: Atrial Preference Pacing, SJM: AF Suppression, Vitatron: Pace Conditioning, Rate Soothing) (graf 1).
- Reakce na síňové extrasystoly redukcí krátkých a dlouhých P-P-intervalů, např. algoritmy firmy ELA (Post Extrasystolic Pause Suppression, Rate Acceleration upon PACs) nebo Vitatron (PAC Suppression, Post-PAC Response).
- Reakce na skončení supraventrikulární arytmie s restitucí sinusového rytmu: přechodným zvýšením stimulační frekvence brání rychlému poklesu tepové frekvence (Vitatron: Post-AF Response).
- Pozátěžová reakce: brání rychlému poklesu tepové frekvence po ukončení zátěže (Vitatron: Post Exercise Response) (graf 2).


Preventivní algoritmy (bod 2-4) se prokázaly jako účinné hlavně v populaci pacientů s fibrilacemi síní a bez bradykardie (subanalýza studie AF Therapy Trial [40]).
Možnost optimalizace činnosti při síňových tachyarytmiích ve smyslu ochrany před převáděním rychlých síňových arytmií na komory
Biotronik: Mode Switch
ELA: Mode Switching
Guidant: Atrial Tachycardia Response
Medtronic: Automatic Mode Switching
SJM: Auto Mode Switch
Vitatron: Mode Switch
Aby se zabránilo převádění rychlých síňových rytmů na komory se všemi hemodynamickými důsledky [41], byl vyvinut princip přepínání režimů. Jedná se nejčastěji o změnu režimu DDD na režim DDI (resp. z režimu VDD na režim VDI), tedy z režimu využívajícího časování závislé na vlně P do režimu využívajícího časování závislé na vlně R. Mezi výrobci můžeme algoritmy přepínání režimu rozdělit na 3 hlavní užívané mechanizmy [42]:
- Tzv. „number of beats mode switch“ mechanizmus. Principem je detekce určitého (programovatelného) počtu intervalů P-P o frekvenci přesahující naprogramovanou hodnotu frekvence nebo trvání úseku se síňovou frekvencí převyšující danou hodnotu. Příkladem je funkce Biotronik Mode Switch (X/Z-out-of-8, překračující maximální sledovací frekvenci, Upper Tracking Rate), Guidant Atrial Tachycardia Response (programovatelný počet konsekutivních intervalů P-P přesahující ATR Trigger Rate), Medtronic Automatic Mode Switching [43] (překročení frekvence Detect Rate po dobu delší než Detect Duration) nebo SJM Auto Mode Switch (překročení hranice Atrial Tachycardia Detection Rate).
- Tzv. „single beat Mode Switch“ mechanizmus aktivující se při první vlně P vnímané uvnitř doby atriální refrakterní periody (např. Biotronik: Mode Conversion, ELA: Mode Switching). Výhodou je rychlé přepnutí režimu při tachykardii, nevýhodou četný výskyt falešně pozitivních detekcí [44] (zejm. u extrasystol).
- Tzv. „beat-to-beat Mode Switch“ (Vitatron Mode Switch) mechanizmus. Algoritmus srovnává interval P-P s povoleným rozsahem kolem spočtené fyziologické frekvence, tj. s tzv. fyziologickým pásmem (v případě nastavení na AUTO), resp. s maximální sledovací frekvencí (v případě nastavení na FIXED). Již první interval P-P překračující tuto hranici spustí přepnutí režimu.
Možnost optimalizace činnosti při síňových tachyarytmiích ve smyslu vyrovnávání nepravidelné komorové frekvence u fibrilace síní
Biotronik: Rate Fading (Rate Smoothing)
Guidant: Rate Smoothing, Ventricular Rate Regulation
Medtronic: Rate Drop Response, Conducted AF Response
SJM: Ventricular Rate Control
Vitatron: Flywheel, Ventricular Rate Stabilization, AF Deceleration
K vyrovnávání nepravidelností intervalů RR při fibrilaci síní se uplatní algoritmy, které tyto nepravidelnosti vyrovnávají stimulací do určité povolené frekvence. Algoritmy slouží ke zmírnění symptomů pacienta.
Detekce a řešení kardiostimulátorem zprostředkované tachykardie
Biotronik: PMT Protection
Guidant: PMT Termination
Medtronic: PMT Interventions
SJM: PMT Options
Vitatron: Automatic detection of Retrograde Conduction
Pacemakerová tachykardie (PMT) neboli tachykardie nekonečné smyčky (endless-loop tachycardia, ELT) je pacemakerem zprostředkovaná reentry tachykardie. Stimulace komor je retrográdně převedena na síně, aktivace síní vnímaná mimo refrakterní periodu vyvolává přes PM stimulaci komor. Pro její vznik je nutná přítomnost retrográdního vedení přes AV-uzel, nevhodné nastavení programu PM podporující udržení PMT a vyvolávající faktor (extrasystola, intermitentně neefektivní síňová stimulace, undersensing vlny P, oversensing v síňovém kanále atd.) [45-47].
Pacemakery jsou vybaveny preventivními algoritmy bránícími vzniku pacemakerové tachykardie a každý výrobce poskytuje doporučení k optimalizaci jejich programování. Žádný z algoritmů však nemůže vyloučit vznik PMT na 100 %.
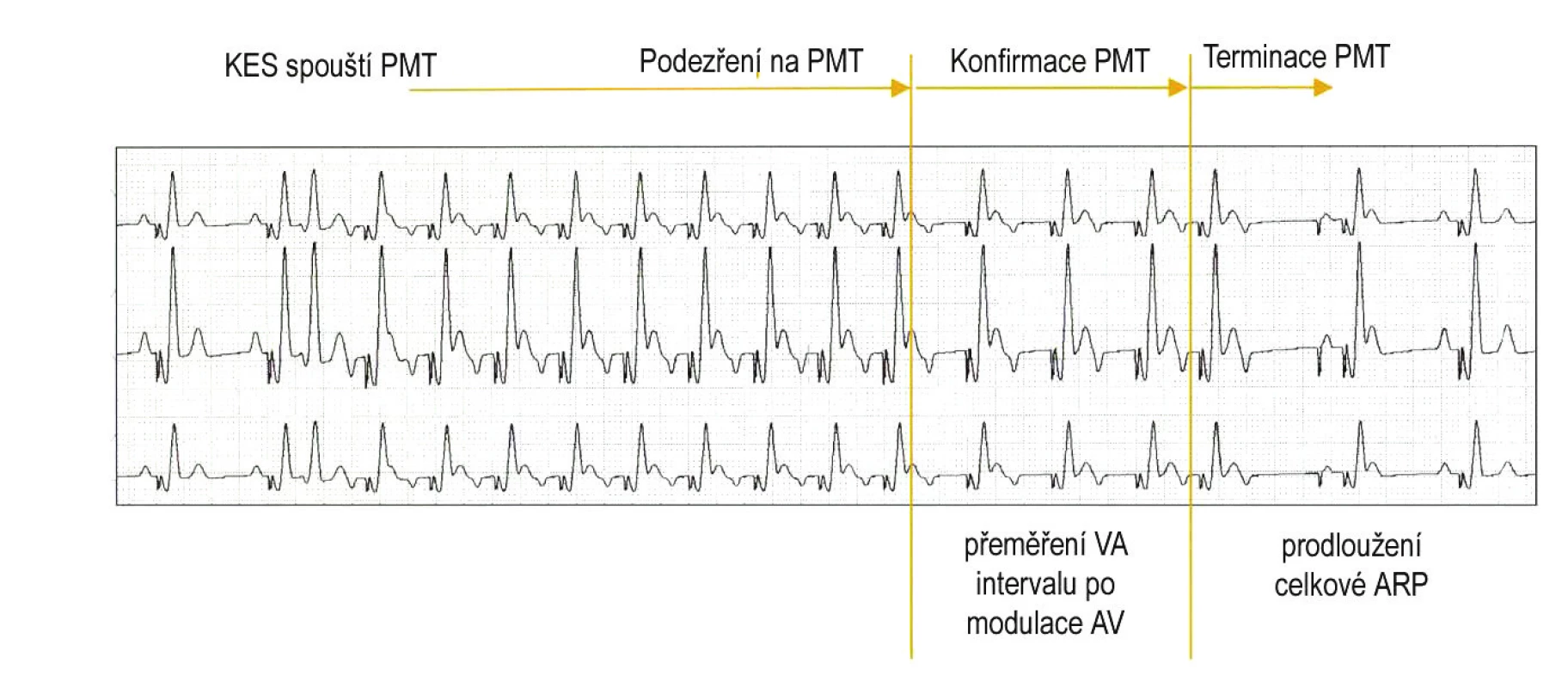
Prvním krokem v managementu je detekce běžící PMT. K hodnocení je užito většinou 8-16 konsekutivních stahů. Pokud jejich frekvence dosáhne určité hodnoty (např. Maximum Tracking Rate u modelů Guidant, přesáhne frekvenci ADLR – Activity Daily Living Rate při nízké aktivitě senzoru u modelů Medtronic, přesáhne PMT Detection Rate u modelů SJM), je počítán průměrný VA-interval. U některých výrobců je podmínkou detekce VA-interval kratší než programovaná hodnota (Biotronik, Medtronic, Vitatron), u většiny výrobců je k detekci požadována stabilita VA-intervalu.
Po úspěšné detekci se u některých výrobců (Biotronik, SJM, Vitatron) provádí potvrzení. Většinou se jedná o tzv. modulaci AV-intervalu, tedy mírné prodloužení nebo zkrácení AV-intervalu s následným přeměřením VA-intervalu. Pokud je tento stabilní, je diagnóza PMT potvrzena.
Samotná terminace běžící PMT se řeší jednorázovým prodloužením PVARP (atriální refrakterní periody po komorové události). Retrográdní vlna P spadající do refrakterní periody nespouští AV delay a následuje sekvenční stimulace síní a komor (obr. 4). Druhou možností je přepnutí do režimu s časováním nezávislým na vlně P (tzv. non-tracking režim) a poté jeho ukončení. Jako prevence opětovného vzniku PMT v případě, že síňový stimulus padne do doby refrakterity síně způsobené retrográdní vlnou P, je síňová stimulace vydána až po bezpečnostním intervalu zvaném NCAP (Non Competitive Atrial Pacing Interval firmy Medtronic), resp. ASP (Atrial Synchronisation Pace Interval firmy Vitatron) [48].
Řešení špatného vnímání
Biotronik: VES Locked-in Protection, 2 : 1 Locked-in Protection
Medtronic: Blanked Flutter Search
Dlouhá atriální refrakterní perioda může způsobit, že fyziologická vlna P při sinusové tachykardii spadne právě do této doby a nespustí AV-interval. Při současné AV-blokádě 1. st. se může stát, že před plánovanou stimulací základní frekvencí bude fyziologická vlna P spontánně převedena na komory a vnímaná vlna R, které z pohledu PM nepředcházela vlna P, bude označena jako komorová extrasystola. Jako taková může nastartovat prodloužení atriální refrakterní periody (pokud je toto nastaveno jako prevence vzniku PMT). Následuje různě dlouhý úsek vlastního sinusového rytmu s AV-blokádou 1. st. Klinicky je stav většinou zcela asymptomatický, ale na náhodně pořízeném EKG-záznamu může imponovat jako porucha PM. Kromě toho PM detekuje úsek konsekutivních komorových stahů bez předcházející vlny P a hodnotí stav jako „komorovou tachykardii“. Tento jev je nazýván funkční atriální undersensing neboli VES Locked-In. Firma Biotronik vyvinula algoritmus testující jeho přítomnost a upravující parametry programování k ukončení epizody (obr. 5) [49].
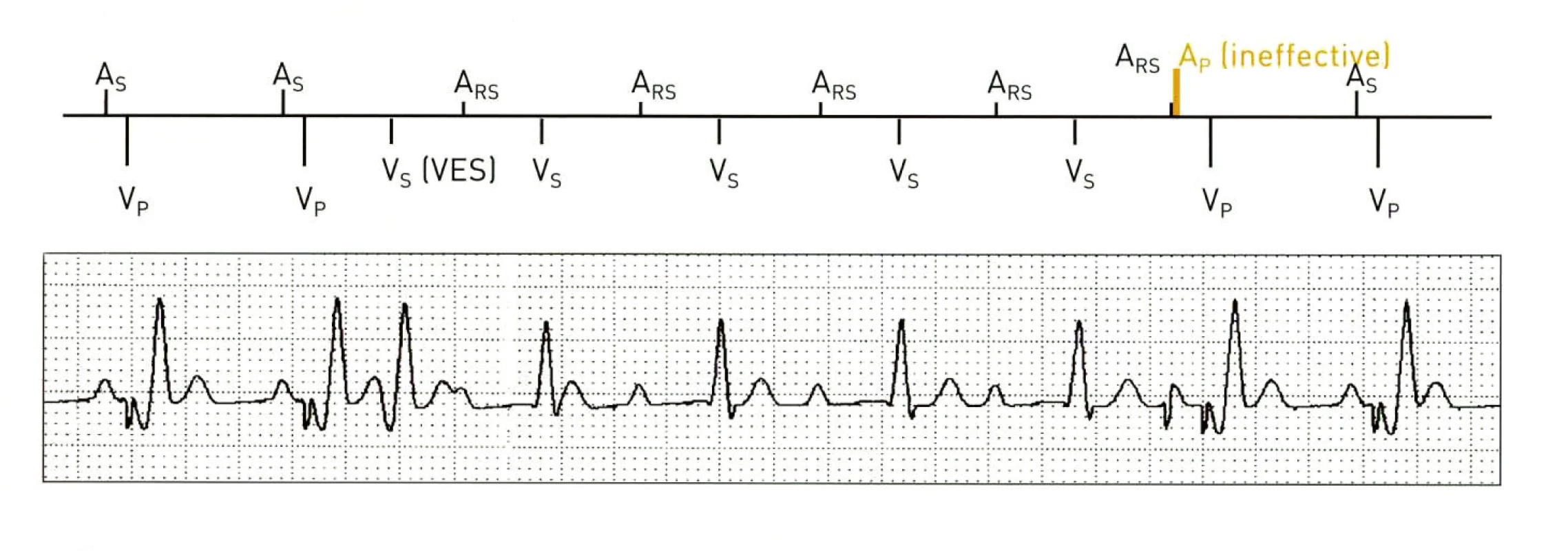
Klinicky významnější je možnost převádění síňového flutteru na komory s převodem 2 : 1. Každá druhá flutterová vlnka spadá do doby refrakterity. Algoritmus stav detekuje, ověřuje jednorázovým prodloužením AV-intervalu a při pozitivní detekci spustí Mode Switch [50].
Řešení nadměrného vnímání (rušení)
Biotronik: EMI Response
Guidant: Noise Response
SJM: Ventricular Noise Reversion Mode
Vitatron: Pacing mode during interference, Pacing rate during interference
Všichni výrobci ošetřili možnost interference se zdroji elektromagnetického vlnění. Při detekci rušení (detekci frekvence spontánních signálů s frekvencí cca nad 480/min, tj. 8 Hz [51]) dojde ke změně stimulačního modu a rušený kanál je po dobu interference vyřazen z vnímání. Stimulace v tomto kanále probíhá poté asynchronně [52].
Jednorázové vnímání spontánní komorové události krátce po síňové stimulaci vyvolá vydání bezpečnostního komorového pulzu ve zkráceném AV-intervalu. Účelem je zabránění inhibice komorové stimulace v případě oversensingu síňové stimulace v komorovém kanále (tzv. AV-crosstalk). Funkce je implementována u všech 2dutinových PM a nazývá se AV safety delay (Biotronik), Ventricular Safety Standby (SJM), Ventricular Safety Pace (Medtronic, Guidant, Vitatron) [53].
Ukládání informací o vlastní činnosti a o srdečním rytmu, jejich analýza a upozornění pacienta/lékaře na závažnou událost
Současné kardiostimulátory jsou vybaveny schopností uchovávat informace o vlastní činnosti (tzv. system-related diagnostics) i o detekované srdeční činnosti (tzv. patient-related diagnostics) [54].
System related diagnostics
Z informací o vlastní činnosti systému je důležitý trend impedance s grafem změn impedance elektrod v čase. Výrazné změny mohou detekovat poruchu elektrody, např. infrakci.
Trendy amplitud vln P a R mohou odhalit nestabilitu vnímání. Četnost výskytu stimulace v síňokomorovém bezpečnostním intervalu (viz kapitola Řešení nadměrného vnímání, rušení) může svědčit pro přítomný AV crosstalk (komorovou detekci síňové stimulace). Modely s automatickou kontrolou úspěšnosti stimulace poskytují informaci o četnosti nutnosti záložního pulzu svědčícího o možném vzestupu stimulačního prahu či jeho nestabilitě (tzv. jumping na elektrodě) nebo nevhodnosti algoritmu u daného pacienta.
Automatické měření impedance a napětí baterie odhalí dosažení stavu s doporučovanou elektivní reimplantací (ERI, elective reimplantation indication).
Patient related diagnostics
Vlastní srdeční elektrická činnost a výskyt arytmií jsou zobrazeny v řadě dílčích trendů a histogramů. Pro lékaře je důležitá informace o četnosti stimulace a vnímání na všech elektrodách. Na základě těchto informací může přeprogramovat nastavení základní frekvence, hystereze a AV-intervalů k optimalizaci stimulační léčby pacienta.
Histogram amplitud vln P a histogram VA-intervalů může odhalit přítomnost vnímání signálů farfield (komorové události vnímané v síňovém kanále a interpretované jako síňová událost) nebo oversensingu vlny T. S rozvojem digitální technologie (digitální vnímání PM vyvinuté firmou Vitatron) lze očekávat i využití různé morfologie vln P.
O četnosti síňových arytmií poskytuje informaci histogram síňové frekvence (vysoké frekvence svědčí o výskytu fibrilace síní či jiných síňových dysrytmií), histogram četnosti SVES, procentuální vyjádření zátěže fibrilací síní (tzv. AF burden) či četnost aktivace Mode Switch.
Komorové dysrytmie lékař posoudí podle histogramu četnosti a časnosti KES a výskytu komorových rytmů bez předchozí vlny P.
Podrobnější informace podá záznam intrakardiálního elektrogramu epizod zaznamenaných kardiostimulátorem [55] včetně uvedení interpretace rytmu ve formě markerového označení stimulovaných a vnímaných událostí [56].
Do biventrikulárních přístrojů nově implementované funkce se soustřeďují na hodnocení kardiální kompenzace. Firma Medtronic vyvinula algoritmus zvaný OptiVolTM. Měřením transtorakální impedance algoritmus aproximuje míru plicního zavodnění [57]. Firma Guidant vybavila biventrikulární PM automatickým měřením variability srdeční frekvence [58]. Firma Ela vyvinula senzor umístěný ve speciální elektrodě, zvaný PEA (Peak Endocardial Acceleration), umožňující automatickou optimalizaci nastavení biventrikulárního přístroje.
Předhodnocení a vyvození návrhů a doporučení řešení
ELA: AIDA (Automatic Interpretation for Data Analysis), AIDA+ (Automatic Interpretation for Diagnosis Assistance)
Guidant: Expert Ease
Medtronic: Observations, TherapyGuide
SJM: QuickOpt™ Timing Cycle Optimization
Vitatron: Therapy Advisor
Modely z posledních let mají implementovány algoritmy, které výše uvedené informace automaticky předhodnocují a vyvozují z nich závěry a doporučení pro úpravu programování. Tato doporučení se zobrazí lékaři při ambulantní kontrole. Příkladem je Therapy Advisor (Vitatron) (obr. 6) [59], Observations nebo Therapy Guide (Medtronic). Lékař na základě doporučení po ověření pravdivosti závěrů může upravit programování či farmakoterapii.
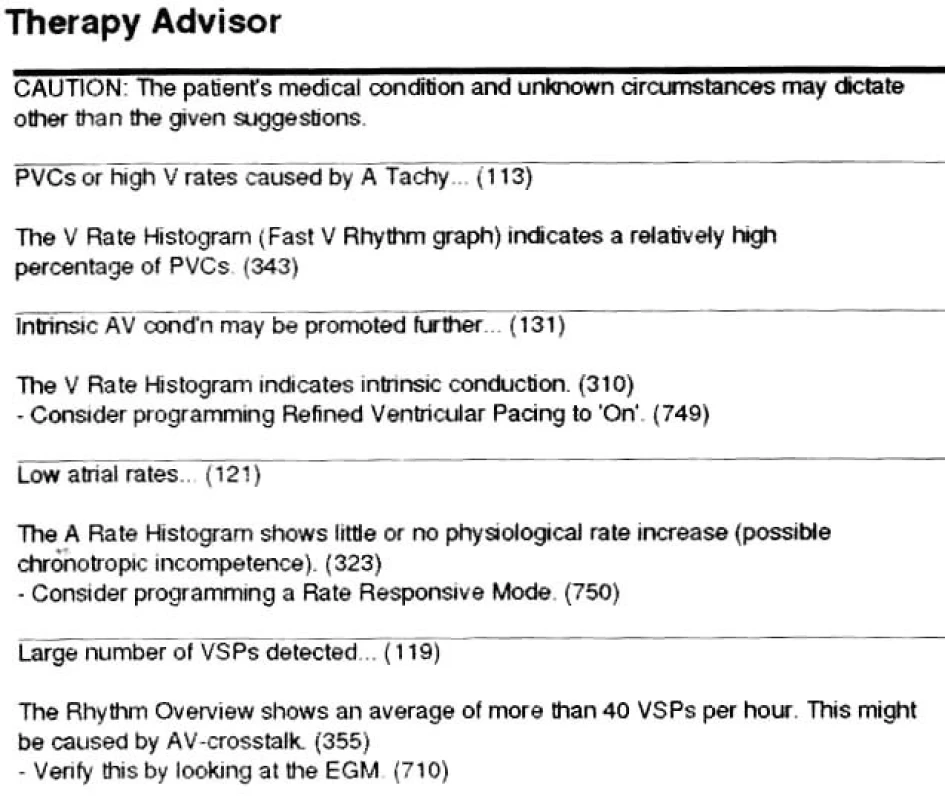
K optimalizaci nastavení AV delay u biventrikulárních přístrojů vyvinula firma Guidant funkci Expert Ease. Funkce je aktivována přes programátor při ambulantní kontrole a vyhodnotí optimální AV-interval na principu měření šířky stimulovaného QRS [60]. Podobnou funkci vyvinula firma SJM (QuickOpt™ Timing Cycle Optimization).
Upozornění lékaře nebo pacienta při závažné události či problému
Biotronik: HomeMonitoring
Medtronic: Conexus Wireless Telemetry, Alarm
SJM: Vibratory Patient Notifier
Výše uvedené informace z diagnostických záznamů přístroje byly pro lékaře dosud dostupné jen v průběhu ambulantní kontroly. V posledních letech se rozvíjejí technologie k upozornění na významnou událost už při jejím vzniku. Firma Medtronic vybavila některé své modely akustickým alarmem. V případě detekce významné události přístroj vydává pípavý zvuk upozorňující pacienta na vhodnost kontroly přístroje v implantačním centru. Funkci firma implementovala dosud jen do ICD. Podobnou funkci využívající vibraci implementovala do nového modelu biventrikulárního ICD i firma SJM.
Možnost dálkového monitorování prožívá v současné době čas rozkvětu. Od roku 2002 je prakticky celosvětově funkční systém Home Monitoring firmy Biotronik, využívající telemetrický přenos informací z implantátu do pacientské jednotky a poté SMS-přenos přes analyzační centrum k lékaři. Podobný systém nyní uvádí na trh firma Medtronic.
Závěr
Automatizace činnosti kardiostimulátoru je naprosto nezbytná. Novodobé přístroje jsou vybaveny desítkami algoritmů, které se mohou svou činností navzájem ovlivňovat. Rovněž mnohotvárnost možných arytmií je obrovská a „chytrý kardiostimulátor“ musí umět všechny situace správně analyzovat a řešit.
Ač se zdá, že automatických funkcí kardiostimulátorů je nesmírná řada, jistě je další vývoj ještě čeká. Už nyní se objevují komplexní funkce hodnotící stav kardiální kompenzace a na tomto poli můžeme čekat další inovace a zdokonalování.
V budoucnu lze očekávat, že lékař bude kardiostimulátorem jen slovně informován o kardiálním stavu pacienta a veškerá nastavení provede přístroj dokonale a optimalizovaně pro každého pacienta sám.
Závěrem se autoři omlouvají za možné neúmyslné vynechání některých analogických algoritmů jiných výrobců.
Doručeno do redakce 21. 7. 06
Přijato k otištění po recenzi 28. 8. 06
MUDr. Jolana Lipoldová
as. MUDr. Miroslav Novák, CSc.
I. interní kardioangiologická klinika LF MU a FN U sv. Anny, Brno
Zdroje
1. Saoudi N, Appl U, Anselme F et al. How smart should pacemakers be? Am J Cardiol 1999; 83(5B): 180D-186D.
2. Kam R. Automatic Capture Verification in Pacemakers (Autocapture). Indian Pacing Electrophysiol J 2004; 4(2): 73-78.
3. Luria D, Gurevitz O, Bar Lev D et al. Use of automatic threshold tracking function with non-low polarization leads: risk for algorithm malfunction. Pacing Clin Electrophysiol 2004 Apr; 27(4): 453-459.
4. Lau C, Nishimura SC, Yee Raymond, Lefeuvre C et al. Intraoperative Study of Polarization and Evoked response Signals in Different Endocardial Electrode Designs. PACE 2001; 24; 1055-1060.
5. Clarke M, Liu B, Schuller H et al. Automatic Adjustment of Pacemaker Stimulation Output Correlated with Continuously Monitored Capture Thresholds: A Multicentre Study. PACE 1998; 21 : 1567-1575.
6. Schubert A, Ventura R, Meinertz T. Automatic Threshold Tracking Activation Without the Intraoperative Evaluation of the Evoked Response Amplitude. AUTOCAP Investigators. PACE 2000; 23 : 321-324.
7. Kam R, Tan CS, Teo WS. Initial Experience with an Autocapture Pacemaker System. Ann. Acad Med Singapore 2000; 29 : 732-734.
8. Ching L, Cameron DA, Nishimura SC et al. A Cardiac Evoked Response Algorithm Providing Threshold Tracking: A North American Multicentre Study. PACE 2000; 23 : 953-959.
9. Chen R, Chen K, Wang F et al. Impact of automatic threshold capture on pulse generator longevity. Chin Med J 2006; 119(11): 925-929.
10. Boriani G, Rusconi L, Biffi M et al. Role of ventricular Autocapture function in increasing longevity of DDDR pacemakers: a prospective study. Europace 2006; 8(3): 216-220.
11. Marenco JP, Greenfield RA, Massumi A et al. Use of the AutoCapture Pacing System with implantable defibrillator leads. Pacing Clin Electrophysiol. 2003; 26(1 Pt 2): 471-473.
12. Biffi M, Boriani G, Bertini M, Silvestri P et al. Pacing with capture verification in candidates for resynchronisation therapy: A feasibility study. Europace 2005; 7 : 255-265.
13. Curtis AB, Vance F, Wuist SM et al. A new algorithm for minimizing polarization artifact: universally applicable in permanent pacing systems. PACE 1991; 14 : 1803-1808.
14. Sperzel J, Binner L, Boriani G et al. Evaluation of the atrial evoked response for capture detection with high-polarization leads. Pacing Clin Electrophysiol. 2005; 28(Suppl 1): 57-62.
15. Sperzel J, Milasinovic G, Smith TW et al. Automatic measurement of atrial pacing thresholds in dual-chamber pacemakers: clinical experience with atrial capture management. Heart Rhythm. 2005; 2(11): 1203-1210.
16. Biotronik GmbH & Co. KG. Lexos VR, VR-T, Lexos DR, DR-T, Lexos A+, A+/T. Technická příručka. S. 7.
17. Medtronic, Inc. EnRhytmTM P1501DR. Dvoudutinový kardiostimulátor s frekvenční odpovědí s telemetrií RapidReadTM (OAE-DDDR). Referenční příručka: S. 62.
18. Biotronik GmbH & Co. KG. Philos II. Technical Manual.:. 41.
19. Barold SS, Stroobandt RX, Sinnaeve AF. Cardiac Pacemakers Step by Step. New York: Blackwell Publishing 2004 : 206-212.
20. Bonnet JL, Pioger G, Vai F. A physiological curvilinear minute ventilation vs heart rate relationship can be reproduced by a minute ventilation sensor driven pacemaker. PACE 1999; 22(6); 103.
21. Bonnet JL, Geroux L, Cazeau S. Evaluation of a dual sensor rate responsive pacing system based on a new concept. PACE 1998; 21(11); 2193-2203.
22. Occhetta E, Bortnik M, Audoglio R, Vassanelli C, INVASY Study Investigators. Closed loop stimulation in prevention of vasovagal syncope. Inotropy Controlled Pacing in Vasovagal Syncope (INVASY): a multicentre randomized, single blind, controlled study. Europace 2004; 6(6): 538-547.
23. Cron TA, Hilti P, Schächinger H, Pouskoulas CD et al. Rate Response of a Closed-Loop Stimulation Pacing System to Changing Preload and Afterload Conditions. PACE 2003; 26 : 1504–1510.
24. Finch D et al. Protos CLS Emotional Response (ER) study. Biotronik Inc. 2004.
25. Puglisi A et al. Impact of Closed-Loop Stimuation, overdrive pacing, DDDR pacing mode on atrial tachyarrhythmia burden in Brady-Tachy Syndrome. EHJ 2003; 24 : 1952-1961.
26. Biotronik GmbH & Co. KG. Philos II. Technical Manual. s. 30.
27. Sweeney MO, Hellkamp AS, Ellenbogen KA et al; MOde Selection Trial Investigators. Adverse effect of ventricular pacing on heart failure and atrial fibrillation among patients with normal baseline QRS duration in a clinical trial of pacemaker therapy for sinus node dysfunction. Circulation 2003; 107(23): 2932-2937.
28. Wilkoff BL, Cook JR, Epstein AE et al. Dual-chamber pacing or ventricular backup pacing in patients with an implantable defibrillator: The Dual Chamber and VVI implantable defibrillator (DAVID) trial. JAMA 2002; 288 : 3115–3123.
29. Lamas GA, Sweeney M, Leon A et al. The mode selection trial (MOST) in sinus node dysfunction: Design, rationale, and baseline characteristics of the first 1000 patients. Am Heart J 2000; 140 : 541–551.
30. Lamas GA, Orav EJ, Stambler BS. Quality of life and clinical outcomes in elderly patients treated with ventricular pacing as compared with dual-chamber pacing. Pacemaker selection in the elderly investigators. N Engl J Med 1998; 338 : 1097–1104.
31. ClinicalTrials.gov. Beluga - Clinical Observations of Automatic Algorithms for Cardiac Pacing 2006. <http://www.clinicaltrial.gov/ct/show/NCT00286858;jsessionid=951BE6AE3800407B559C143971CDE1D3?order=20>
32. Savouré A, Fröhlig G, Galley D et al. A New Dual-Chamber Pacing Mode to Minimize Ventricular Pacing. PACE 2005; 28 : 43.
33. Sweeney MO, Ellenbogen KA, Casavant D et al for The Marquis MVP Download Investigators. Multicenter, Prospective, Randomized Safety and Efficacy Study of a New Atrial-Based Managed Ventricular Pacing Mode (MVP) in Dual Chamber ICDs. J Cardiovasc Electrophysiol 2005; 16(8): 811-817.
34. Saksena S, Prakash A, Krol RB et al. Organized and reproducible atrial activation is present globally and regionally during phases of human atrial fibrillation [abstract]. J Am Coll Cardiol 2000; 35 : 139.
35. Israel CW, Barold SS (eds). Advances in the Treatment of Atrial Tachyarrhythmias: Pacing, Cardioversion and Defibrillation. Armonk. New York: Futura Publishing Co 2002 : 139-171.
36. Coumel P, Friocourt P, Mugica J et al. Long-term prevention of vagal atrial arrhythmias by atrial pacing at 90/minute: experience with 6 cases. PACE 1983; 6 : 552–560.
37. Attuel P, Pellerin D, Mugica J et al. DDD pacing: an effective treatment modality for recurrent atrial arrhythmias. PACE 1988; 11 : 1647–1654.
38. Carlson M, Ip J, Messenger J, Beau S et al. A New Pacemaker Algorithm for the Treatment of Atrial Fibrillation. Results of the Atrial Dynamic Overdrive Pacing Trial (ADOPT). J Am Coll Cardiol 2003; 42 : 627–633.
39. Lee MA, Weachter R, Pollak S et al. The Effect of Atrial Pacing Therapies on Atrial Tachyarrhythmia Burden and Frequency. J Am Coll Cardiol 2003; 41 : 1926 –1932.
40. Camm AJ. AF therapy study: Preventive pacing for paroxysmal atrial fibrillation. (Abstract) Pacing Clin Electrophysiol 2002; 25 : 125.
41. Lau C, Leung S, Tse HF, Barold S. Automatic mode switching of implantable pacemakers: I. Principles of instrumentation, clinical, and hemodynamic considerations. Pacing Clin Electrophysiol 2002; 25 : 967-985.
42. Dulk K, Dijkman B, Wellens HJJ. Dual Chamber Pacemakers In Patients With Paroxysmal Atrial Fibrillation. HeartWeb 1996; 2(1): Article 96110041.
43. Passman RS, Weinberg KM, Freher M et al. Accuracy of Mode Switch Algorithms for Detection of Atrial Tachyarrhythmias. J Cardiovasc Electrophysiol 2004; 15(7): 773-777.
44. Pitney MR, Max CD, Davis MJ. Undesirable mode switching with a dual camber rate responsive pacemaker. PACE 1993; 16 : 729-737.
45. Limousin M, Bonnet JL and the investigators of the multicenter study. A new algorithm to solve endless loop tachyardia in DDD pacing: A multi-center study in 91 patient. PACE 1990; 13 : 1711-1718.
46. Fontaine JW, Maloney JD, Castle LW et al. Noninvasive assessment of ventriculoatrial conduction and early experience with the tachycardia termination algorithm in pacemaker-mediated tachycardia. PACE 1986; 9 : 212.
47. Duncan JL, Clark MF. Prevention and termination of pacemaker-mediated tachycardia in a new DDD pacing system (Siemens-Pacesetter Model 2010T). PACE 1988; 11 : 1679.
48. Cameron DA et al. Initial Cliical Experience with a New Automatic PMT Detection and Termination Algorithm to Discriminate Between Pacemaker Mediated Tachycardia Due to Ventriculo-atrial Conducrion and Normal Sinus Tachycardia. HeartWeb 1996; 2(1): Article 96110035.
49. Biotronik GmbH & Co. KG. Philos II. Technical Manual.:. 60.
50. Biotronik GmbH & Co. KG. Philos II. Technical Manual.:. 54.
51. Biotronik GmbH & Co. KG. Philos II. Technical Manual.:. 38.
52. Irnich W. Interference in pacemakers. PACE 1984; 7 : 1021.
53. Cardiac Rhythm Management. Guidant pacemaker noise rejection feature to prevent inappropriate pacing inhibition due to cross-chamber sensing. Guidant Corp 2003; 33.
54. Nowak B. Taking Advantage of Sophisticated Pacemaker Diagnostics. Am J Cardiol 1999; 83 : 172D-179D.
55. Charles R, Rauscha F, Waucquez JL et al. Storage of intracardiac electrograms in pacing systems: a new tool in arrhythmia diagnosis. Arch Mal Coeur 1998; 91 : 230.
56. Nowak B, Middeldorf T, Housworth CM et al. Holter recordings with continuous marker annotations: a new tool in pacemaker diagnostics. PACE 1996; 19 : 1791-1795.
57. Abraham WT, Foreman B, Fishel R et al. Fluid Accumulation Status Trial (FAST). Heart Rhythm 2005; (Suppl 2): S65. Abstract AB33-4.
58. Studie Mona Lisa (MONitoring of Arrhythmias and HRV in Patients With Heart Failure Treated With the CRT Pacemaker Renewal TR2) 2004. <http://www.clinicaltrials.gov/ct/show/NCT00180531>
59. Schuchert A, Brunekreeft W on behalf of T-STAR investigators. T-STAR interim results: Therapy Advisor for optimising the pacemaker AF therapy. Europace Supplements 2005; 7 : 106.
60. Guidant Corp. Contak Renewal TR2 CRT-P. Models H145/H140. System Guide. Guidant 2003 : 3/18-3/20.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie KardiologieČlánek vyšel v časopise
Kardiologická revue – Interní medicína

2006 Číslo 4
-
Všechny články tohoto čísla
- Nobelova cena za lékařství a fyziologii 2006
- Vyšetřování srdeční stability
- Historie trvalé kardiostimulace
- Automatické funkce kardiostimulátorů
-
Jsou moderní automatické kardiostimulátory skutečně automatické?
Medtronic Adapta a jeho automatické funkce - Nová antiarytmika v léčbě fibrilace síní
- Akutní infarkt myokardu u žen
- Léčba hypertenze u chronické renální insuficience
- Studie SPARCL – the Stroke Prevention by Aggressive Reduction in Cholesterol Levels: komentář
- Defekt septa komor (obrazový text)
- Klinické studie ukončené, přednesené nebo publikované v poslední době
- Přehled studií citovaných v článcích tohoto čísla Kardiologické revue
- Galerie autorů
- Rejstřík k ročníku 8 (2006)
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Automatické funkce kardiostimulátorů
- Vyšetřování srdeční stability
- Léčba hypertenze u chronické renální insuficience
- Nová antiarytmika v léčbě fibrilace síní
